Практическое значение температуры самовоспламенения как показателя пожарной опасности. От каких факторов зависит температура самовоспламенения? Процесс горения и его виды
Различие между возгоранием и самовозгоранием поясняются следующим образом. Представим, что образец твердого материала помещается в воздушный термостат, устанавливаемый на различные заданные температуры. На рис. 1.5 представлены получаемые в этих испытаниях развиваемые во времени в материале температуры. При весьма умеренном нагреве (кривая 1) в материале не происходят изменения. За время, определяемое разностью температур в термостате и окружающей среды, а также теплоемкостью и массой материала температура материала достигнет температуры термостата, а после отключения термостата материал вернется в начальное состояние. Такая картина будет наблюдаться при размещении материала в термостате и с более» высокой температурой до тех пор, пока не будет достигнута некоторая начальная температура самонагревания Тсн, при которой начнутся экзотермические превращения в_материале (разложение, окисление и
Температура самонагревания - самая низкая температура вещества, при которой в нем возникают практически различимые экзотермические процессы. Температуру самонагревания используют при выборе безопасных условий нагрева вещества. Безопасной температурой длительного нагрева вещества считают ту, которая не превышает 90% температуры самонагревания.
Примечание. К6 - коэффициент безопасности; КбВ - коэффициент к верхнему Пределу воспламенения; Кбз - коэффициент к энергии зажигания; К6н - коэффициент к нижнему пределу воспламенения; К6О - коэффициент к концентрации кислорода в смесях; К6с - коэффициент к температурам самовоспламенения, самонагревания, тления; Кбф ~ коэффициент к минимальной флегматизирующей концентрации инертного разбавителя в воздухе; КИ - кислородный индекс; КИД - допустимый кислородный индекс; ДЯ°Г - потенциал горючести 1 г-моль горючего вещества; ДЯ°ф - потенциал горючести 1 г-моль флегматизатора; t6i3 - безопасная температура, "С; *всп - температура вспышки, °С; (всп д - допустимая температура вспышки, "С; (с - минимальная температура среды, при которой наблюдается самовозгорание образца, °С; гсв - температура самовоспламенения, °С; tca - температура самонагревания, °С; trl[ - температура тления, °С; ""min ~ минимальная энергия зажигания, Дж; W6e3 - безопасная энергия зажигания, Дж; ^г - число молей горючего в смеси; Vф - число молей флегматизатора в смеси;
Температуры самонагревания и тления. Температура самонагревания характеризует склонность ряда веществ и материалов к самовозгоранию, т. е. возникновению горения в результате самонагревания.
Температура самонагревания - самая низкая температура, при которой в веществе или материале, находящемся в атмосфере воздуха, возникают различные экзотермические процессы окисления, разложения и др.
Температура самонагревания - самая низкая температура вещества, нагревание до которой может привести к его самовозгоранию. Температуру самонагревания учитывают при определении условий безопасного длительного (или постоянного) нагрева вещества.
тем медленнее процесс горения. Температура при горении развивается до 1000° С. При длительном хранении в бунтах влажные семена самовозгораются. Температура при этом, как правило, не превышает 50-70° С, однако в отдельных случаях температура самонагревания достигает значительных величин и заканчивается загоранием семян. Самонагревание семян происходит за счет биологических и физико-химических процессов, активизированных повышенным содержанием влаги в семенах. Так, например, самонагревание низкомасленичных семян подсолнечника, содержащих 26-29% масла и имеющих влажность 18-30%, до опасных пределов не наблюдается. Однако семена подсолнечника, содержащие масла 40-44%, при влажности более 18% самовозгораются весьма интенсивно и нередко самовоспламеняются.
В статье рассмотрены методы определения пожаровзрывоопасных показателей углеродных порошков (диспергированных твердых веществ и материалов с частицами размером менее 850 мкм): группа горючести, температура воспламенения, нижний и верхний концентрационные пределы распространения пламени, температура самонагревания, температура тления, минимальная энергия зажигания, способность взрываться и гореть при взаимодействии с водой и кислородом воздуха, минимальное взрывоопасное содержание кислорода и минимальная флегматизирующая концентрация флегматизатора, максимальное давление взрыва и скорость нарастания давления при взрыве.
Температура самонагревания. Эксперименты проводили в течение 1 месяца одновременно в четырех воздушных термостатах вместимостью по 4 дм3, отрегулированных на 60, 80, 100 и 120°С. За температуру самонагревания исследуемых образцов №1-5 была принята наиболее низкая температура в сушильном шкафу - 80°С, при которой в образцах возникали практически различимые экзотермические процессы окисления и разложения (см. таблицу).
Температура самонагревания, °С 80 80 80 80 80
Температура самонагревания - - 4- +
2) в результате самонагревания будет достигнута температура самовозгорания Тсв, начиная с которой произойдет спонтанный рост скорости реакции и температуры и обязательно возникнет горение (кривая 3).
Температура вспышки - минимальная температура горючего вещества, при которой над его поверхностью образуются газы и пары, способные вспыхивать (вспыхивать - быстро сгорать без образования сжатых газов) в воздухе от источника зажигания (горящего или раскаленного тела, а также электрического разряда, обладающих запасом энергии и температурой, достаточными для возникновения горения вещества). Температура самовозгорания -самая низкая температура, при которой происходит резкое увеличение скорости экзотермической реакции (при отсутствии источника зажигания), заканчивающееся пламенным горением. Концентрационные пределы воспламенения - минимальная (нижний предел) и максимальная (верхний предел) концентрации, которые характеризуют области воспламенения.
Пресспорошок - горючий материал; его пыль образует с воздухом смеси, нижний предел воспламенения которых составляет 10- 50 т/и3; температура самовозгорания 655-900 °С.
Для образца с линейным размером 15 мм плотностью 0,7 г-см-3 критическая температура самовозгорания на 6-7 град, ниже, чем для образца плотностью 0,4 г-см-3. Дальнейшее увеличение плотности приводит к снижению активности самовозгорания. В опытах Г. П. Сапрыгина и Я. С. Киселева образец (15 мм) при плотности 1,0г-см~3 не загорался вплоть до 495 К, тогда как образцы с плотностью 0,6 - 0,7 г-см-3 имели критическую температуру самовозгорания ниже 467 К. Эти эксперименты показали влияние интенсивности поступления кислорода на условия самовозгорания. При небольшом уплотнении продукта, когда экзотермический процесс лимитируется кинетическими факторами, с увеличением плотности активность самовозгорания растет. При больших уплотнениях образца кислорода, содержащегося в его объеме, оказывается недостаточно для поддержания максимальной скорости окисления. Поскольку при этих условиях затруднен приток кислорода извне, экзотермический процесс тормозится.
Самовозгоранием считается повышение температуры образца до 400 - 500 °С. Временем до самовозгорания считают промежуток от момента выравнивания показаний термопар до начала резкого подъема температуры в образце. Время до самовозгорания определяют с точностью до 0,05 г. В течение всего опыта температура воздуха в термостате не должна изменяться более чем на 2,5 град. После фиксации явных признаков горения или после окончания выдержки образца при отсутствии самовозгорания термостат выключают. Следующие испытания проводят в зависимости от результатов первого испытания при температуре на 10 - 20 град ниже или выше температуры первого испытания. Эти опыты повторяют до тех пор, пока не будут найдены две температуры среды, отличающиеся на 5 град, при одной из которых наблюдается самовозгорание образца, а при другой - отказ. Среднюю арифметическую этих значений, округленную до 1 град, принимают за температуру самовозгорания образца данных размеров. Опыты начинают с образцов меньших размеров. Для обработки экспериментальных данных в логарифмических координатах «температура самовозгорания - удельная поверхность» и «температура самовозгорания - время до самовозгорания» строят соответствующие зависимости.
В зависимости от внутреннего импульса процессы самовозгорания делятся на химические, микробиологические и тепловые. Химическое самовозгорание от воздействия на вещества кислорода воздуха, воды или от взаимодействия веществ. Часто пожары возникают вследствие самовозгорания промасленных тряпок, спецодежды, ваты и даже металлических стружек. О склонности масла или жира ко самовозгоранию можно судить по его йодному числу. Йодным числом называется количество йода в граммах, поглощенное 100 г испытываемого масла или жира. Чем выше йодное число, тем ниже температура самовозгорания.
температура самовозгорания
77 /27 /77 221 ZV 327 Температура самовозгорания, °с
В зависимости от характера возникновения процесс горения называют возгоранием или самовозгоранием. Различие между ними видно из приводимой ниже схемы (где t^ - температура источника нагрева; ti - температура самонагревания; ti - температура самовозгорания, самовоспламенения):
Температура самовозгорания, "С
К числу температурных показателей пожарной опасности пылей, подлежащих определению, относятся температура воспламенения, температура самовозгорания (тления и самовоспламенения) и температура самонагревания (см. гл. 2).
Теоретические вопросы.. 3
1. Практическое значение температуры самовоспламенения как показателя пожарной опасности. От каких факторов зависит температура самовоспламенения?. 3
2. Какое горение называется тлением? Обязателен ли приток кислорода для тления? Перечислить показатели пожарной опасности твердых горючих материалов. 5
Расчетная часть задания. 10
1. Общие сведения. 10
2. Физико-химические свойства. 10
3. Расчет характеристик горения. 12
Вещество. 17
Список использованной литературы.. 18
Теоретические вопросы
1. Практическое значение температуры самовоспламенения как показателя пожарной опасности. От каких факторов зависит температура самовоспламенения?
Основными показателями пожарной опасности являются температура самовоспламенения и концентрационные пределы воспламенения.
Температура самовоспламенения - самая низкая температура технологической среды, при которой в условиях специальных испытаний происходит резкое увеличение скорости экзотермических реакций, заканчивающихся пламенным горением.
Применяемость показателя в зависимости от агрегатного состояния вещества | Область применения |
||||
Температура самовоспламенения |
Самовоспламенение - резкое увеличение скорости экзотермических объемных реакций, сопровождающееся пламенным горением и/или взрывом.
Значение температуры самовоспламенения следует применять при определении группы взрывоопасной смеси по ГОСТ 12.1.011 для выбора типа взрывозащищенного электрооборудования, при разработке мероприятий по обеспечению пожаровзрывобезопасности технологических процессов в соответствии с требованиями ГОСТ. 12.1.004 и ГОСТ 12.1.010, а также необходимо включать в стандарты или технические условия на вещества и материалы.
Сущность метода определения температуры самовоспламенения заключается во введении определенной массы вещества в нагретый объем и оценке результатов испытания. Изменяя температуру испытания, находят ее минимальное значение, при котором происходит самовоспламенение вещества.
Температура самовоспламенения зависит от фракционного состава и от преобладания углеводородов того или иного класса. Чем ниже пределы кипения той или иной фракции, т. е. чем она легче, тем она менее опасна с точки зрения самовоспламенения, т. к. температура самовоспламенения уменьшается с увеличением средней молекулярной массы нефтепродукта. Тяжелые нефтяные остатки сомавоспламеняются при С, а бензины при температуре выше 500 0С.
В производственных условиях самовозгораются каменный уголь, торф, опилки, некоторые горючие жидкости, обычно в виде тонких пленок, получающихся при нанесении жидкости на ворсистые поверхности (хлопок, вата и т. п.). К этим жидкостям относятся растительные масла, скипидар. На предприятиях имеются случаи самовозгорания обтирочных материалов, промасленной спецодежды, поэтому спецодежду необходимо развешивать так, чтобы обеспечить доступ воздуха, промасленные обтирочные материалы собираются в несгораемую тару с крышками и ежесменно удаляются, сжигаются или уничтожаются.
Самовозгорание угля и торфа обнаруживается по белому налету на их поверхности, по появлению пара и дыма, по оседанию слоя угля или торфа в месте их складирования, а зимой - по таянию снега. Опасные по самовозгоранию угли хранятся в штабелях высотой не более 2.5 м (в подвале 1 м) и шириной до 20 метров. При укладке уголь послойно уплотняется катками.
2. Какое горение называется тлением? Обязателен ли приток кислорода для тления? Перечислить показатели пожарной опасности твердых горючих материалов.
Тление - беспламенное горение твердого вещества (материала) при сравнительно низких температурах (°С), часто сопровождающееся выделением дыма.
Горение - экзотермическая реакция окисления вещества, сопровождающаяся, по крайней мере, одним из трех факторов: пламенем, свечением, выделением дыма.
Температура тления - температура вещества, при которой происходит резкое увеличение скорости экзотермических реакций окисления, заканчивающихся возникновением тления.
Значение температуры тления следует применять при экспертизах причин пожаров, выборе взрывозащищенного электрооборудования и разработке мероприятий по обеспечению пожарной безопасности технологических процессов, оценке пожарной опасности полимерных материалов и разработке рецептур материалов, не склонных к тлению.
Сущность метода определения температуры тления заключается в термостатировании исследуемого вещества (материала) в реакционном сосуде при обдуве воздухом и визуальной оценке результатов испытания. Изменяя температуру испытания, находят ее минимальное значение, при котором наблюдается тление вещества (материала).
Тление не может происходить без притока кислорода и оттока продуктов горения. У тления есть своя конвективная газовая струя.
Перечень показателей пожарной опасности технологических сред
Показатель пожарной опасности технологической среды | Для твердых материалов | Область применения |
Группа горючести | Для определения способности технологических сред к горению |
|
Температура вспышки | ||
Температура воспламенения | При определении группы горючести и оценки пожарной опасности технологических сред |
|
Температура самовоспламенения | При определении группы взрывоопасной смеси для выбора типа взрывозащищенного электрооборудования |
|
Концентрационные пределы распространения пламени (воспламенения) | При определении концентраций горючих газов, паров и пылей, при которых возможно распространение пламени |
|
Температурные пределы распространения пламени (воспламенения) | При определении пожаробезопасных температурных режимов работы оборудования. Для расчетной оценки концентрационных пределов распространения пламени |
|
Температура тления | При разработке мероприятий по обеспечению пожарной безопасности технологических сред, склонных к тлению |
|
Условия теплового самовозгорания | При выборе безопасных условий хранения и переработки технологических сред, склонных к самовозгоранию |
Продолжение таблицы
Минимальная энергия зажигания | При разработке мероприятий по обеспечению пожарной безопасности и электростатической искробезопасности технологических сред |
|
Кислородный индекс | При обеспечении безопасности технологических сред, связанных с обращением полимерных материалов |
|
Способность взрываться и гореть при взаимодействии с водой, кислородом воздуха и другими веществами | При определении категории помещений по взрывопожарной и пожарной опасности. При выборе безопасных условий совместного хранения и транспортирования технологических сред. При выборе средств пожаротушения |
|
Нормальная скорость горения смеси (для пылей - эффективная нормальная скорость распространения пламени) | При разработке и создании огнепреградителей, предохранительных мембран и других разгерметизирующих устройств |
|
Удельная скорость выгорания | При определении продолжительности горения жидких технологических сред в резервуарах, интенсивности тепловыделения и подачи огнетушащих веществ |
|
Коэффициент дымообразования | Для классификации технологических сред по дымообразующей способности |
|
Индекс распространения пламени | Для классификации технологических сред по способности распространять пламя по поверхности |
|
Показатель токсичности продуктов горения полимерных материалов | Для оценки токсичности технологических сред, содержащих полимеры |
Продолжение таблицы
Минимальное содержание кислорода | При разработке мероприятий по обеспечению пожарной безопасности технологических сред с пониженным содержанием кислорода |
|
Минимальная флегматизирующая концентрация флегматизатора | При разработке мероприятий по обеспечению пожарной безопасности технологических сред с наличием разбавителя (флегматизатора, ингибитора) |
|
Максимальное давление взрыва | ||
Скорость нарастания давления взрыва | При разработке мероприятий по взрывозащите технологического оборудования (расчет предохранительных клапанов, мембран и т. п.) |
|
Критическая поверхностная плотность теплового потока | При разработке мероприятий по снижению способности технологических сред воспламеняться под действием теплового излучения пламени и определении категорий помещений по пожарной опасности |
|
Длина распространения пламени по струе аэрозоля | Для оценки пожарной опасности жидких технологических сред в распыленном состоянии |
|
При оценке пожарной опасности аварийного истечения технологических сред |
Продолжение таблицы
Минимальная концентрация негорючего разбавителя в воздухе, при которой существует диффузионное пламя | При оценке последствий аварийного истечения парогазовых технологических сред |
|
Удельная теплота сгорания | При оценке пожарной опасности технологических сред и определении категорий помещений и наружных установок по взрывопожарной и пожарной опасности |
|
Индекс пожаро-взрывоопасности | Для оценки пожарной опасности технологических сред в технологическом оборудовании |
|
Способность к экзотермическому разложению | Для термодинамически нестабильных технологических сред, способных вызвать резкий рост температуры и давления при разложении |
|
Способность к воспламенению при адиабатическом сжатии | Параметр, характеризующий способность технологической среды к воспламенению при адиабатическом сжатии в смеси с воздухом или другим окислителем |
|
Излучающая способность пламени | Для оценки плотности теплового потока от пламени при горении технологических сред |
|
Безопасный экспериментальный максимальный зазор | При выборе степени взрывозащиты электрооборудования |
Примечание. Знак “+” обозначает применяемость, знак “-” - неприменяемость показателя пожарной опасности для технологической среды.
Расчетная часть задания
1. Общие сведения
Название вещества.
СН3ОН – Метиловый спирт, метанол, древесный спирт, гидроксильное произведение метана СН4.
2. Физико-химические свойства
Агрегатное состояние; внешний вид, цвет, запах; плотность;. температура плавления; температура кипения; растворимость в воде; коэффициент молекулярной диффузии пара; удельное электрическое сопротивление; диэлектрическая проницаемость; предельно допустимая концентрация ПДК (справочные данные).
Свойства водных растворов метилового спирта в зависимости от его концентрации
Показатель | Концентрация, % по массе |
|||||
Плотность, г/см3 | ||||||
Температура замерзания, 0С |
2.1. Расчет относительной плотности паров по воздуху (Dвозд)
(при К < 0 жидкость не горит, при К > 0 жидкость не горит).
3. Расчет характеристик горения
3.1. Определение характера свечения пламени.
Метанол служит растворителем и промежуточным продуктом в производстве красителей. Но главным потребителем его является производство пластмасс, для которого нужны большие количества метаналя (формальдегида). Метаналь же получается при окислении метанола кислородом воздуха. В промышленности смесь паров метанола и воздуха при 400 0С пропускают над медным или серебряным катализатором.
Чтобы смоделировать этот процесс, согнем в спираль кусочек медной проволоки диаметром 0,5 - 1 мм и щипцами внесем его в несветящуюся зону пламени горелки Бунзена. Проволока раскаляется и покрывается слоем оксида меди (II). Поместим полученный нами раньше метанол (10 капель) в достаточно широкую пробирку и опустим в него раскаленную медную спираль. Вследствие нагревания метанол испаряется и под влиянием катализатора - меди - соединяется с кислородом с образованием метаналя (мы узнаем его по характерному резкому запаху). При этом поверхность медной проволоки восстанавливается. Реакция происходит с выделением тепла. При больших количествах паров метанола и воздуха медь остается разогретой до тех пор, пока реакция не завершится.
![]()
3.5. Объем и состав продуктов горения (теоретический)
По уравнению реакции горения (для 1 кг горючего вещества при нормальных условиях).
МО2 = 32 кг/моль, МСН2О = 30 кг/моль, МН2О = 18 кг/моль.
Из 64 кг СН2ОН получается 60 кг СН2О
Из 1 кг СН2ОН х кг СН2О
х = 0,94 кг СН2О
При получении 60 кг СН2О образуется 36 кг Н2О
При получении 0,94 кг СН2О у кг Н2О
у = 0,56 кг Н2О
3.6. Стехиометрическая концентрация в паровоздушной смеси
3.6.1. Объемная концентрация (%).
Стехиометрическая концентрация (об. %) определяется по формуле:
![]()
3.6.2. Массовая концентрация (кг/м3, г/м3).
Массовое стехиометрическое отношение дает отношение массы воздуха к массе топлива.
![]()
3.7. Концентрационные пределы распространения пламени
Нижний (верхний) концентрационный предел распространения пламени - минимальное (максимальное) содержание горючего вещества в однородной смеси с окислительной средой, при котором возможно распространение пламени по смеси на любое расстояние от источника зажигания.
Значения концентрационных пределов распространения пламени необходимо включать в стандарты или технические условия на газы, легковоспламеняющиеся индивидуальные жидкости и азеотропные смеси жидкостей, на твердые вещества, способные образовывать взрывоопасные пылевоздушные смеси (для пылей определяют только нижний концентрационный предел). Значения концентрационных пределов следует применять при определении категории помещений по взрывопожарной и пожарной опасности в соответствии с требованиями норм технологического проектирования ; при расчете взрывобезопасных концентраций газов, паров и пылей внутри технологического оборудования и трубопроводов, при проектировании вентиляционных систем, а также при расчете предельно допустимых взрывобезопасных концентраций газов, паров и пылей в воздухе рабочей зоны с потенциальными источниками зажигания в соответствии с требованиями ГОСТ 12.1.010, при разработке мероприятий по обеспечению пожарной безопасности объекта в соответствии с требованиями ГОСТ 12.1.004.
Допускается использовать экспериментальные и расчетные значения концентрационных пределов распространения пламени.
Сущность метода определения концентрационных пределов распространения пламени заключается в зажигании газо-, паро - или пылевоздушной смеси заданной концентрации исследуемого вещества в объеме реакционного сосуда и установлении факта наличия или отсутствия распространения пламени. Изменяя концентрацию горючего в смеси, устанавливают ее минимальное и максимальное значения, при которых происходит распространение пламени.
Нижний предел (jн) в % об. вычисляют по формулам
http://pandia.ru/text/78/079/images/image024_25.gif" width="440" height="24">
Верхний предел распространения пламени (jв) в % об. вычисляют в зависимости от величины стехиометрического коэффициента кислорода (b) по формулам:
http://pandia.ru/text/78/079/images/image026_26.gif" width="145" height="20 src=">при b ³ 8
где hj, qs- коэффициенты, учитывающие химическое строение вещества;
т j - число связей j -го элемента;
mC, mH, mCl , mO - число атомов соответственно углерода, водорода, хлора и кислорода в молекуле вещества.
b = m С + m S + 0,25(m H - m X) - 0,5m O + 2,5m p, (36)
где m С, m S, m H, m X, m O, m p - число атомов соответственно углерода, серы, водорода, галоида, кислорода и фосфора в молекуле жидкости.
hi: hC-H = 1,39, hC-O = 1,40, hO-H = 1,25
681 " style="width:511.05pt;border-collapse:collapse;border:none">
Вещество
Константы уравнения Антуана
Диэлектр. прониц.
tКИПЕНИЯ, 0С
DН образ. кДж/моль
DН исп. кДж/моль
Метанол СН3ОН
lgр = 7,3,454/(245,818 + t)
Список использованной литературы
1. ГОСТ 12.1.044-89. Пожаровзрывоопасность веществ и материалов.
2. Номенклатура показателей НПБ 23-2001. Пожарная опасность технологических сред.
3. Глинка и упражнения по общей химии. Учеб. пособ. для вузов / Под ред. и Х. М. рубинов. – 23-е изд., испр. – Л.: Химия, 1985. – 264 с.
4. Глинка химия: Учеб. пособ. для вузов. – 24-е изд., испр. / Под ред. . – Л.: Химия, 1985. – 704 с.
5. Химия: Справ. материалы / , ; Под. ред. . – 2-е изд., перераб. – М.: Просвещение, 1988. – 223 с.
6. Хомченко задач по химии. – М.: Новая волна, 2002. – 256 с.
7. Хомченко по химии для поступающих в вузы. – 4-е изд., испр. и доп. – М.: Новая волна, 2004. – 480 с.
Следует иметь в виду, что увеличение содержания кислорода в веществах и уменьшение содержания углерода снижают температуру самовоспламенения.
Для горения и воспламенения важное значение имеет концентрация газов и паров в воздухе. Диапазон горения и воспламенения характеризуется нижним и верхним пределами взрываемости. Они являются важнейшей характеристикой взрывоопасности горючих веществ. Нижний предел взрыва характеризуется наименьшей концентрацией газов и паров воздуха, при котором возможен взрыв, а верхний - наибольшей их концентрацией, при которой еще возможен взрыв.
Все горючие жидкости пожароопасны. Они горят в воздухе при определенных условиях, зависящих от концентрации их паров. Горючие жидкости постоянно испаряются, образуя над поверхностью насыщенные взрывоопасные пары.
По температуре вспышки горючие жидкости делятся на два класса. К первому классу относятся жидкости (бензин, керосин, эфир и др.), вспыхивающие при температуре менее 45°С, ко второму классу - жидкости (масла, мазуты и др.), имеющие температуру вспышки выше 45°С. В практике первый класс жидкостей принято называть легковоспламеняющимися (ЛВЖ), второй - горючими (ГЖ).
Пыли и пылевоздушные смеси горючих веществ пожароопасны. В воздухе они могут образовывать взрывоопасные смеси. Увеличение влажности воздуха и сырья, из которого образуется пыль, а также повышение скорости движения воздуха уменьшают концентрацию пыли в воздухе и снижают пожароопасность.
Взрывоопасными являются пыль сахара, крахмала, нафталина при концентрации в воздухе до 15 г/м э; торфа, красителей и т. п. при концентрации от 15 до 65 г/м 3 .
Пожара- и взрывоопасные объекты. (ПВОО) - предприятия, на которых производятся, хранятся, транспортируются взрывоопасные продукты или продукты, приобретающие, при определенных условиях, способность к возгоранию или взрыву.
К ним прежде всего относятся производства, где используются взрывчатые и имеющие высокую степень возгораемости вещества, а также железнодорожный и трубопроводный транспорт, как несущий основную нагрузку при доставке жидких, газообразных пожаро- и взрывоопасных грузов. По взрывной, взрывопожарной и пожарной опасности ПВОО подразделяются на пять категорий: А, Б, В, Г, Д. Особенно опасны объекты, относящиеся к категории А, Б, В.
Все строительные материалы и конструкции из них делятся на три группы: несгораемые, трудносгораемые и сгораемые.
Несгораемые - это материалы, которые под воздействием огня или высокой температуры не воспламеняются, не тлеют и не обугливаются.
Трудносгораемые - это материалы, которые под воздействием огня или высокой температуры с трудом воспламеняются, тлеют или обугливаются и продолжают гореть при наличии источника огня.
Сгораемые - это материалы, которые под воздействием огня или высокой температуры воспламеняются или тлеют и продолжают гореть и тлеть после удаления источника огня.
Пожары на крупных промышленных предприятиях и в населенных пунктах подразделяются на отдельные и массовые. Отдельные - пожары в здании или сооружении.
Массовые - совокупность отдельных пожаров, охвативших более 25% зданий. Сильные пожары при определенных условиях могут перейти в огненный шторм.
По степени огнестойкости все здания и сооружения подразделяются на 5 степеней:
1степени - все конструктивные элементы здания несгораемые или с высокой сте
пенью огнестойкости (1,5-3 ч);
2степени - все конструктивные элементы несгораемые, но с меньшей степенью
огнестойкости (1,5-2,5 ч);
3степени - основные несущие конструкции несгораемые (1-2 ч), а междуэтажные,
чердачные перекрытия и внутренние стены - трудносгораемые (0,25-0,75 ч);
4степени - все конструкции трудносгораемые (0,25- 0,5 ч);
5степени - все конструкции сгораемые.
Характеристика аварий на пожаро- и взрывоопасных объектах. К авариям на ПВОО относятся: пожары с последующим взрывом газообразных (сжиженных) углеводородных продуктов, топливно - воздущных смесей и других взрывоопасных веществ и, взрывы, чаще всего, в результате свободного истечения легко воспламеняющихся взрывоопасных жидкостей или газов, приводящие к возникновению многочисленных очагов пожаров.
Особым случаем взрыва является объемный взрыв, когда подрывается газообразная или аэрозольная смесь, занимающая значительный объем. Характерный пример такого взрыва - взрыв при утечке газа. При этом взрывоопасное облако способно проникать в закрытые помещения через окна, люки и т. п, и взрыв может поражать людей и причинять разрушения в местах, защищенных стенами.
Чрезвычайные ситуации, создающиеся на ПВОО, часто осложняются том, что многие взрывоопасные вещества ядовиты или образуют при сгорании химически опасные вещества (ХОВ).
Поражающие факторы при авариях на пожаро- и взрывоопасных объектах.
Каждый пожар характеризуется наличием опасных факторов.
Опасный фактор пожара - фактор, воздействие которого приводит к травме, отравлению или гибели человека, а также к материальному ущербу. В соответствии с ГОСТ 12.01.004-85 «Пожарная безопасность» опасными факторами пожара являются: открытый огонь и искры, повышенная температура окружающей среды, предметов и т. п., токсичные продукты горения, дым, пониженная концентрация кислорода, падающие части строительных конструкций, агрегатов, установок, взрывы.
Горение всех жидких, газообразных и большинства твердых горючих веществ, которые, разлагаясь или испаряясь, выделяют газообразные продукты, сопровождается образованием пламени. Таким образом, пламя представляет собой газовый объем, в котором происходит процесс горения паров и газов.
Без пламени горят твердые вещества: графит, антрацит, кокс, сажа, древесный уголь. Эти вещества не разлагаются и но образуют при нагревании газов, либо образует их в количествах, недостаточных для горения.
Пламя бывает светящимся и несветящимся. Свечение пламени при горении органических веществ зависит от наличия в нем раскаленных твердых частиц углерода, которые успевают сгорать. Несветящееся (синее) пламя обычно бывает при сгорании газообразных продуктов: окиси углерода, водорода, метана, аммиака, сероводорода.
Температура пламени при горении на воздухе некоторых горючих веществ составляет: древесины - 850-1400°С, нефтепродуктов в резервуаре - 1100-1300°С, сероуглерода - 2195°С, стеарина - 640-940°р, электрона - около 3000°С.
Все тепло в процессе горения выделяется из пламени. Часть этого тепла расходуется на нагревание продуктов горения и становится источником для поддержания дальнейшего горения. Вторая часть его уносится в пространство в виде тепловых лучей, которые нагревают окружающие предметы, а некоторые из них - даже поджигают.
Открытый огонь очень опасен, т.к. воздействие пламени на тело человека вызывает ожоги. Еще большую опасность представляет тепловое излучение огня, которое может вызвать ожоги тела, глаз и др. При горении технологических установок интенсивность излучения тепла настолько велика, что человек без специальных средств защиты подойти к ним ближе, чем на 10 м, не может.
Температура.
Вдыхание нагретого воздуха приводит к поражению и некрозу верхних дыхательных путей, удушью и смерти человека. При воздействии температуры свыше 100°С человек теряет сознание и гибнет через несколько минут.
Опасны для человека ожоги кожи. Несмотря на большие успехи медицины в их лечении, у пострадавшего, получившего ожоги второй степени на 30% поверхности тела, мало шансов выжить. Время же, за которое человек получает ожоги второй степени, невелико: при температуре среды 7ГС - 26 сек., 15 сек. - при 100°С. Исследованиями установлено, что во влажной атмосфере, типичной для пожара, вторую степень ожога вызывает температура значительно ниже указанной. Таким образом, температура окружающей среды 60-70°С опасна для жизни человека, причем не только в горящем, но и смежных с ним помещениях, в которые попали продукты горения и нагретый воздух.
Но чаще всего люди на пожарах гибнут не от огня и высокой температуры, а из-за понижения концентрации кислорода в воздухе и отравления токсичными продуктами горения.
В обычных условиях человек дышит атмосферным воздухом с содержанием кислорода 20,9%. В условиях пожара при сгорании веществ и материалов уровень кислорода в воздухе помещения уменьшается. Понижение концентрации кислорода всего лишь на 3% вызывает ухудшение двигательных функций организма человека, а до 14%° - считается очень опасным.
В зависимости от того, каким количеством кислорода окисляется горючее вещество, различают два вида горения: полное и неполное. При наличии достаточного количества кислорода происходит полное горение. При этом основным продуктом горения является углекислый газ, неспособный к дальнейшему горению. Если же кислорода не хватает, происходит неполное сгорание, основным продуктом которого является окись углерода, или так называемый угарный газ. Окись углерода способна гореть и в соединении с воздухом образовывать взрывчатые смеси. Кроме того, она обладает отравляющими свойствами.
Кроме углекислого газа или окиси углерода, продуктом горения почти каждого горючего вещества является дым. Он состоит, в основном, из паров воды, газов, образовавшихся при горении, и множества мельчайших твердых несгоревших частил (угля, смолистых продуктов и т.п.) Дым делает воздух непрозрачным и вредно действует на глаза и дыхательные пути.
Большую опасность для жизни людей представляют дымовые газы. Так, диоксид углерода СО 2 в концентрации 3-4,5% становится опасным для жизни при вдыхании в течение нескольких минут. Обычно при пожарах в помещениях концентрация СО, значительно превышает смертельную. Основным механизмом токсического воздействия СО г на человека является блокирование гемоглобина крови, при этом нарушается поступление кислорода из легких в ткани, что приводит к кислородному голоданию. Человек теряется способность рассуждать, становится равнодушным, не стремится избежать опасности, у него наступает оцепенение, головокружение, депрессия, нарушение координации движений, а при остановке дыхания - смерть.
Во многих случаях дымовые газы содержат окислы азота, синильную кислоту, сероводород и другие токсичные вещества, действие которых даже в небольших концентрациях (окислы азота -0,025%, синильная кислота - 0,002%) приводит к смерти.
Дымовые газы особенно опасны, если при отделке помещений и изготовлении изделий применялись полимерные материалы и пластмассы. Например, при горении линолеума «Релин» выделяется сероводород и сернистый газ, при горении мягкой мебели, в которой использован пенополиуретан (поролон), - цианистый водород, который поражает нервную систему и оказывает смертельное действие при содержании его в воздухе более 0,03 %; при горении винипласта - хлористый водород (при его концентрации 4,5 мг/л смерть наступает через 5-10 мин) и оксид углерода; при горении капроновых тканей - цианистый водород. Очень опасно одновременное воздействие на органы дыхания различных токсичных веществ, даже если их концентрация (в отдельности) значительно ниже предельно допустимой.
Насколько опасны токсичные продукты горения, наглядно показывает пример пожара, происшедшего в магазине одежды в г. Токио. Пожар вспыхнул не на 3 этаже, а в баре, расположенном на 7 этаже этого же здания, погибли 118 человек, из них 96 - от отравления токсичными продуктами горения, 22 человека выпрыгнули из окон. Многие люди потеряли сознание в течение первых 2-3 мин., а смерть наступила через 4-5 мин. после этого.
Снижение видимости.
Еще один опасный фактор пожара - это снижение видимости вследствие задымления, что затрудняет, а порой делает практически невозможной эвакуацию людей из опасного помещения. Чтобы быстро выйти в безопасное место, люди должны четко видеть эвакуационные выходы или их указатели.
При потере видимости организованное движение (особенно в незнакомом здании, на объектах с массовым пребыванием людей) нарушается, становится хаотичным, каждый двигается в произвольно выбранном направлении. Возникает паника. Это тоже опасный фактор пожара. Людьми овладевает страх, подавляющий сознание, волю. В таком состоянии человек теряет способность ориентироваться, правильно оценивать обстановку.
Одним из видов мгновенного горения является взрыв специальных взрывчатых веществ, а также смеси горючих газов, паров или пыли с воздухом. Это взрывы химического характера.
Взрывы физического характера - это разрывы различных емкостей и аппаратов (котлов, резервуаров, баллонов и т.п.), происходящие в результате развития газами или парами чрезмерного давления, превышающего давление, которое могут выдержать стенки емкостей и аппаратов.
В момент взрыва химического характера вещество сгорает с большой скоростью, а образующиеся газы и пары сильно расширяются и создают большое давление на окружающую среду. Этим и объясняется громадная сила разрушения; вызываемая взрывом. При взрыве обычно появляется пламя, от которого могут загораться находящиеся вблизи горючие вещества.
Большинство взрывчатых веществ на открытом воздухе сгорает спокойно и медленно. В замкнутых же пространствах скорость сгорания значительно увеличивается. Поэтому любое взрывчатое вещество, находящееся в оболочке, представляет большую опасность.
Прямая угроза жизни людей возникает при взрывах различных аппаратов, баллонов, находящихся в производственных и жилых помещениях, при обрушении конструкций здания в результате потери ими несущей способности от воздействия высокой температуры.
Характер воздействия аварии на пожаро- и взрывоопасном объекте на население и окружающую среду. При взрыве на ПВОО поражение людей и повреждения различной степени могут происходить, как от прямого воздействия ударной волны, так и косвенно - от летящих обломков, камней, осколков стекла и т. п. Характер и степень поражения людей зависят от степени их защищенности. При избыточном давлении травмы и контузии людей могут быть: тяжелыми - при давлении 60-100 кПа, средними - при давлении 40-60 кПа и легкими - при давлении 20-40 кПа.
Тяжелые травмы выражаются сильной контузией, потерей сознания и многочисленными сложными переломами костей; средние - вывихами конечностей, контузией головного мозга, повреждением органов слуха; легкие - быстро проходящими функциональными нарушениями.
Избыточное давление, не превышающее 10 кПа, считается безопасным, для расположенных на открытой местности людей, однако косвенные поражения за счет летящих камней и стекла могут наблюдаться даже при избыточном давлении 2 кПа.
Возникающие, в результате взрывов, пожары приводят к ожогам, а горение пластмасс и некоторых синтетических материалов - к образованию различных концентраций ХОВ, цианистых соединений, фосгена, сероводорода и др. Чаще всего на пожарах людей поражают окиси углерода (при содержании в воздухе 1% окиси углерода, наступает почти мгновенная потеря сознания и смерть), реже - цианистые соединения, бензол, окислы азота, углекислота и другие токсичные продукты. К поражающим факторам пожаров относят также задымление, затрудняющее ориентирование, и сильный морально-психологический эффект.
Наиболее опасны пожары в административных зданиях, так как внутренние стены облицованы панелями из горючего материала, а потолочные плиты выполнены из горючих древесных плит. Часто возникновению возгорания способствует неудовлетворительная огнестойкость древесины и других строительных материалов, особенно пластиков.
Чрезвычайно опасен в пожарном отношении применяемый при изготовлении мебели поролон, который при горении выделяет ядовитый дым, содержащий цианистые соединения. Кроме того, в условиях стесненного производства становятся опасными вещества, считающиеся негорючими.
Так, взрывается и горит древесная, угольная, торфяная, алюминиевая, мучная, зерновая и сахарная пыль, а также пыль хлопка, льна, пеньки, джута. Самовозгораются такие обычные химикаты, как скипидар, камфара, барий, пирамидон и многие другие.
Аварии на объектах нефтегазодобывающей промышленности всегда приносят большие бедствия. Так, вырвавшийся нефтяной или газовый фонтан при воспламенении перебрасывает огонь на резервуары с нефтью, компрессорные установки и нефтепроводы, мастерские, гаражи, жилые дома и лесные массивы.
Бушующее пламя горящего фонтана поднимается огромным смерчем к небу, тяжелый дым застилает окрестности. Температура внутри такого смерча настолько велика, что плавятся стальные буровые вышки и другие конструкции.
Нередки пожары от возгорания горючего, при перевозках. Во время пожаров на железнодорожном транспорте, как правило, обрываются провода, парализуя все движение.
4.3.2. Мероприятия по защите населения и территории при пожарах и взрывах на объектах инфраструктуры
Противопожарная профилактика в зданиях и на территории предприятий
обеспечивается: правильным выбором степени огнестойкости объекта и пределов огнестойкости отделочных элементов и конструкций, ограничением распространения огня в случае возникновения очага пожара; применением систем противодымной зашиты; безопасной эвакуацией людей; применением средств пожарной сигнализации, извещения и пожаротушения; организацией пожарной охраны.
Противопожарная профилактика - комплекс организационных и технических мероприятий по предупреждению, локализации и ликвидации пожаров, а также по обеспечению безопасной эвакуации людей и материальных ценностей в случае пожара.
Наиболее частыми причинами пожаров являются нарушения правил пожарной безопасности и технологических процессов, неправильная эксплуатация электросети и оборудования, грозовые разряды.
Основные вопросы пожарной безопасности объектов (предприятий) изложены в Правилах пожарной безопасности в Российской Федерации.
Противопожарная защита зданий имеет важное значение для борьбы с пожарами и недопущением распространения огня. Распространение огня может быть линейным и объемным. При линейном, пламя перемещается по поверхности горючих веществ.
Под объемным распространением пожара понимают возникновение новых очагов огня на расстоянии от первоначального его появления. Причиной такого распространения огня является передача его различными способами (теплопроводностью, излучением и т. д.).
Эффективная мера против распространения пожаров - противопожарные разрывы (табл.19) и преграды, а также продуманная внутренняя планировка зданий и устройство различных противопожарных преград и отсеков, изолированных несгораемыми конструкциями.
Температурой самовоспламенения называется самая низкая температура вещества, при которой происходит резкое увеличение скорости экзотермических реакций, заканчивающееся пламенным горением.[ ...]
Сложность непосредственного измерения температуры самовоспламенения газовой смеси и условия практического использования этого показателя привели к тому, что в качестве температуры самовоспламенения принимают температуру стенки реакционного сосуда, при которой наблюдается самовоспламенение смеси. Для одной и той же пары веществ горючее - окислитель эта температура непостоянна. Она зависит от объема сосуда, условий тепло- и массообмена внутри реакционного сосуда с окружающей средой, от объема вводимой в реакционный сосуд смеси и концентраций реагирующих веществ, от присутствия в реакционном сосуде положительных и отрицательных катализаторов самовоспламенения. Поэтому для получения воспроизводимых данных методика измерения температуры самовоспламенения стандартизована.[ ...]
Измеренная стандартным методом самая низкая температур3, До которой должна быть нагрета наиболее легко воспламеняющаяся смесь горючего газа (или пара) с воздухом для того, чтобы она воспламенялась без внесения в нее постороннего источника зажигания, называется стандартной температурой самовоспламенения.[ ...]
При температуре самовоспламенения вещества горение еще не возникает. Оно возникает и развивается при температуре горения (пламени), значительно превышающей температуру самовоспламенения. Так, температура самовоспламенения бензина 260 °С, а его пламени- 1200-1300 °С. Для того чтобы смесь достигла такой высокой температуры, необходимо время для самонагревания смеси паров бензина с воздухом. Это время носит название периода индукции. Чем ниже температура нагрева горючего вещества при самовоспламенении, тем больше период индукции.[ ...]
Период индукции зависит от температуры, давления, состава и объема смеси. Особенно большое значение имеет период индукции при действии маломощных источников поджигания. При воспламенении от электрической искры объем смеси газа или паров нагревается, а сама искра охлаждается. Если период индукции мал, то за это время может произойти воспламенение, а если он велик, то искра успеет погаснуть и воспламенения не произойдет. Период индукции для газо- и паровоздушных смесей колеблется от сотых долей секунды до десятков секунд. Для твердых веществ этот период может измеряться часами и больше.[ ...]
Большое влияние на температуру самовоспламенения оказывает давление. С увеличением давления число соударений частиц возрастает, и процесс их активации идет более интенсивно. При этом тепловой эффект реакции повышается, и температура самовоспламенения понижается.[ ...]
С увеличением объема сосуда скорость теплоотвода уменьшается, и в соответствии с этим температура самовоспламенения понижается. Однако увеличение объема (форма сосуда не изменяется) не бесконечно снижает температуру самовоспламенения, и выше некоторого предела (более 12 л) температура остается постоянной. Это объясняется тем, что самовоспламенение горючей смеси происходит не во всем объеме, а в одном каком-то благоприятном месте. Поэтому в малом объеме горючего вещества изменение теплоотвода через стенки сосуда влияет на изменение температуры самовоспламенения, а в большем объеме не влияет.
Рассмотрев вопрос возникновения горения в результате нагрева горючей смеси до их температуры самонагревания стоит обратить внимание на то, что в природе существует большое количество горючих веществ и материалов, температура самонагревания которых равна или ниже обычной температуры в помещениях. Так, алюминевая пудра при соприкосновении с воздухом способна окисляться и при этом самонагреваться до возникновения пламенного горения даже при температуре окружающего воздуха 10 0 С.
Такой процесс возгорания веществ и материалов получил название самовозгорание.
Согласно стандартам ГОСТ и СЭВ самовозгорание - это:
1) резкое увеличение скорости экзотермических процессов в веществе, приводящее к возникновению очага горения;
2) возгорание в результате самоинициируемых экзотермических процессов.
Самовозгорание как начальная стадия горения принципиально не отличается от самовоспламенения (см. рис. 2.4). Склонность веществ и материалов к самовозгоранию можно охарактеризовать как функцию теплоты сгорания соединения, скорости реакции окисления, теплопроводности, теплоёмкости, влажности, наличия примесей, объёмной плотности, удельной поверхности, теплопотерь и т. д. Самовозгоранием считается, если процесс самонагревания веществ и материалов происходит в интервале температур от 273 К до 373 К, т. е. при более низких температурах, чем при самовоспламенении.
Рис. 2.4. Схема возникновения горения
Температурой самонагревания называется самую низкую температуру вещества, при которой возникает его самонагревание, заканчивающееся самовоспламенением. Самовозгорающиеся вещества делят на три группы: масла, жиры и другие продукты растительного происхождения; самовозгорающиеся химические вещества; ископаемые горючие материалы.
Причиной самонагревания, приводящей к воспламенению, может быть ряд факторов: микробиологический процесс, адсорбция , полимиризация, теплота химических реакций. Условно самовозгорание классифицируют по начальным причинам самонагревания и различают: тепловое самовозгорание, микробиологическое и химическое самовозгорания (см. рис. 2.5).
Рассмотрим более подробно каждый вид самовозгорания .
Тепловое самовозгорание. Тепловым называется самовозгорание, вызванное самонагреванием, возникшим под воздействием внешнего нагрева вещества, материала, смеси выше температуры самонагревания. Тепловое самовозгорание возникает при нагревании вещества до температуры, обеспечивающей его термическое разложение идальнейшее самоускоряющееся самонагревание за счет тепла экзотермических реакций в объеме горючего.
При этом большую роль играют реакции окисления продуктов термического разло-жения. Сам процесс протекает в форме тления в глубине мате-риала, которое затем переходит в пламенное горение на поверх-ности. К тепловому самовозгоранию имеют склонность многие вещества и материалы, в частности масла и жиры, каменные угли и некоторые химические вещества. Самонагревание масел и жиров растительного, животного и минерального происхождения возникает в результате окислительных процессов под действием кислорода воздуха при развитой поверхности контакта с ними.
Минеральные масла - машинное, трансформаторное, соляровое и другие, которые получают при переработке нефти. Они представляют собой главным образом смесь предельных углеводородов и окисляются на воздухе только при высоких температурах. Отработанные минеральные масла, подвергавшиеся нагреву до высокой температуры, могут содержать непредельные соединения, которые способны к саморазогреву, т. е. могут самовозгораться.

Рис. 2.5. Схема развития процесса самовозгорания твердых веществ и материалов. Импульсы самонагревания (самовозгорания): 1 - тепловой, 2 - химический, 3 - микробиологический.
Растительные масла (хлопковое, льняное, подсолнечное и др.) и животные (сливочное, рыбий жир) по своему составу отличаются от минеральных. Они представляют собой смесь глицеридов жирных кислот: пальмитиновой С 15 Н 31 СООН, стеариновой C 17 Н 35 СООН, олеиновой С 17 Н 33 СООН, линолевой С 17 Н 31 СООН, линоленовой С 17 Н 29 СООН и др. Пальмитиновая и стеариновая кислоты являются предельными, олеиновая, линолевая и линоленовая - непредельными.
Глицериды предельных кислот, а следовательно, масла и жиры, содержащие их в большом количестве, окисляются при температурах свыше 150 0 С, что означает следующее: они не способны самовозгораться (см. табл. 2.3). Масла, содержащие большое количество глицеридов непредельных кислот, начинают окисляться при температурах значительно ниже 100 0 С, следовательно, они способны самовозгораться.
Таблица 2.3.
Состав жиров и масел
Масла и жиры самовозгораются только при определённых условиях:
а) при наличии в составе масел и жиров значительного количества глицеридов непредельных кислот;
б) при наличии большой поверхности их окисления и малой теплоотдачи;
в) если жирами и маслами пропитаны какие-либо волокнистые горючие материалы;
г) промасленные материалы имеют определённую уплотнённость.
Различная способность растительных масел и животных жиров к самовозгоранию объясняется тем, что они содержат глицериды различного состава, строения и не в одинаковом количестве.
Глицериды непредельных кислот способны окисляться на воздухе при обычной температуре помещений за счёт наличия в их молекулах двойных связей:
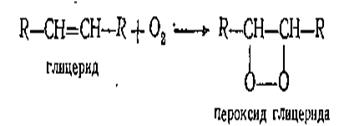
Пероксиды легко разлагаются с образованием атомарного кислорода , который очень реакционноспособен:

Атомарный кислород взаимодействует даже с трудноокисляющимися компонентами масел.
Одновременно с окислением протекает и реакция полимеризации непредельных соединений:
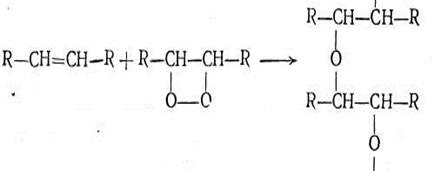
Процесс идёт при низкой температуре с выделением тепла. Чем больше глицерид имеет двойных связей, тем больше он присоединяет молекул кислорода, тем больше выделяется тепла в процессе реакции, тем больше его способность к самовозгоранию.
О количестве глицеридов непредельных кислот в масле и жире судят по йодному числу масла, т. е. по количеству йода, поглощённому 100 г масла. Чем выше йодное число, тем большая способность этого жира или масла к самовозгоранию (см. табл. 2.4).
Самое большое йодное число имеет льняное масло. Волокнистые материалы, пропитанные льняным маслом, при всех прочих одинаковых условиях самовозгораются быстрее, чем материалы, пропитанные другими маслами. Олифы, приготовленные на основе растительных масел, имеют меньшее йодное число, чем основа, но способность к самовозгоранию у них выше.
Это объясняется тем, что в олифу добавляется сиккатив, ускоряющий её высыхание, т. е. окисление и полимеризацию. Полунатуральные олифы, представляющие собой смеси окисленного льняного или других растительных масел с растворителями, имеют небольшие йодные числа и мало способны к самовозгоранию. Синтетические олифы совершенно не способны самовозгораться.
Таблица 2.4.
Иодные числа жиров и масел
Жиры рыб и морских животных имеют высокое йодное число, но обладают незначительной способностью к самовозгоранию. Это объясняется тем, что в их составе присутствуют продукты, замедляющие процесс окисления.
Способность промасленных материалов к самовозгоранию увеличивается с присутствием в них катализаторов, ускоряющих процесс окисления и полимеризацию масел. Повышение температуры окружающей среды также способствует ускорению этих процессов. Катализаторами для самовозгорания масел являются соли различных металлов: марганца, свинца, кобальта. Наиболее низкая температура, при которой на практике наблюдали самовозгорание масел и жиров, составляла 10-15 0 С.
Индукционный период самовозгорания промасленных материалов может составлять от нескольких часов до нескольких дней. Это зависит от объёма промасленного материала, степени его уплотнения, вида масла или жира и их количества, температуры воздуха и других факторов.
Ископаемые угли (каменный, бурый), которые хранятся в кучах или штабелях, способны самовозгораться при низких температурах. Основными причинами самовозгорания является способность углей окисляться и адсорбировать пары и газы при низких температурах. Процесс окисления в угле при низких температурах идёт достаточно медленно и тепла выделяется мало. Но в больших скоплениях угля теплоотдача затруднена, и самовозгорание угля всё же происходит. Самонагревание в штабеле угля первоначально происходит во всём объёме, исключая только поверхностный слой толщиной 0,3-0,5 м, но по мере повышения температуры оно приобретает очаговый характер.
Рост температуры в очаге самовозгорания до 60 0 С идёт медленно и может прекратиться при проветривании штабеля. Начиная с 60 0 С, скорость самонагревания резко увеличивается, такая температура угля называется критической . Склонность углей к самовозгоранию в штабелях различна, она зависит от количества выхода из них летучих веществ, от степени измельчения, присутствия влаги и пирита. Согласно нормам хранения все ископаемые угли по их склонности к самовозгоранию делятся на две категории: А - опасные, Б - устойчивые.
К категории А относят бурые и каменные угли, за иск-лючением марки Т, а также смеси разных категорий. Наиболее опасны в отношении самовозгорания уг-ли марок ОС (кузнецкие), Ж (ткварчельские), Г (ткибульские), Д (печерские, кузнецкие и донецкие), Б (райчихинские, украинские, ленировские, ангренские и др.). Эти угли нельзя хранить долго. К категории Б относят антрацит и каменные угли мар-ки Т. Устойчивы при длительном хранении все антрациты и угольные брикеты, угли марок Т (донецкие, кузнецкие), Ж (печерские и сучанские), Г (сучанские), Д (чернеховские).
Для предотвращения самовозгорания углей при хранении нормами установлено:
1) ограничение высоты штабелей угля;
2) уплотнение угля в штабеле с целью ограничения доступа воздуха во внутренний объём штабеля.
Выполнение этих мероприятий сводит к минимуму скорость процессов окисления и адсорбции, рост температуры в штабеле, препятствует проникновению в штабель атмосферных осадков и естественно снижает возможность самовозгорания.
Также к тепловому самовозгоранию имеют склонность многие химические вещества . Сульфиды железа FeS, FeS 2 , Fe 2 S 3 способны самовозго-раться, поскольку могут реагировать с кислородом воздуха при обычной температуре с выделением большого количест-ва тепла:
FeS 2 + О 2 → FeS + SO 2 + 222,3 кДж.
Отмечены случаи самовозгорания пирита или серного колчедана (FeS 2) на складах сернокислотных заводов, а также в рудниках. Самовозгоранию пирита способствует влага.
Предпо-лагается, что реакция в этом случае протекает по сле-дующему уравнению:
2FeS 2 + 7,5О 2 + Н 2 О → Fe 2 (SO 4) 3 + K 2 SO 4 + 2771 кДж.
При образовании железного купороса объем увеличива-ется и происходит растрескивание пирита и его измель-чение, что благоприятствует процессу самовозгорания.
Сульфиды FeS и Fe 2 S 3 образуются в емкостях для хранения нефтепродуктов, горючих газов и в аппарату-ре различных производств, где имеются примеси серо-водорода. В зависимости от температуры образование сульфидов железа протекает различно. Если температу-ра выше температуры диссоциации сероводорода, т. е. выше 310 0 С, сульфиды железа образуются при взаимо-действии железа с элементарной серой, получившейся в результате разложения сероводорода или других серни-стых соединений.
Элементарная сера может также по-лучиться в результате окисления сероводорода , и тогда образование сернистого железа происходит по следую-щим реакциям:
2H 2 S + О 2 →2Н 2 О + 2S,
При температурах ниже 310 0 С сульфиды железа в производственной аппаратуре образуются в результате воздей-ствия сероводорода не на железо, а на продукты его коррозии:
2Fe(OH) 3 + 3H 2 S → Fe 2 S 2 + 6Н 2 О.
Все пожары в производственной аппаратуре, возник-шие в результате самовозгорания сульфидов железа, происходили после освобождения аппаратуры от храни-мого или обрабатываемого в ней продукта.
Например, на нефтеперегонном заводе, перерабатывающем сернистую нефть, была поставлена на ремонт бензиновая ректификационная колонна. При вскрытии люка на стенках колонны и тарелках был обнаружен слой сульфида железа. Быстрая подача пара в колонну позволила предотвратить окисление и самовозгорание сульфида же-леза. Как видно, сульфид железа в колонне образовался уже давно, но из-за отсутствия воздуха окисление не протекало.
Самовозгорание сульфидов железа в производствен-ной аппаратуре предотвращают следующими методами: очисткой от сероводорода обрабатываемого или хранимого продукта, антикоррозийным покрытием внутренней поверхности аппаратуры, продуванием аппаратуры па-ром или продуктами сгорания для удаления горючих паров и газов, заполнением аппаратуры водой и медленным спуском ее, что ведет к окислению сульфида без ус-корения реакции.
Фосфор белый (желтый), фосфористый водород (фосфин), водородистый кремний (силан), цинковая пыль, алюминиевая пудра, карбиды щелочных металлов, суль-фиды металлов - рубидия и цезия, арсины, стибины, фосфины, сульфоуголь и другие вещества также способны окисляться на воздухе с выделением тепла, за счет ко-торого реакция ускоряется до горения. Некоторые из перечисленных веществ способны самовозгораться очень быстро после соприкосновения с воздухом, другие же - через длительный промежуток времени.
Например, фосфор белый (желтый) интенсивно окисляется при температуре помещений, поэтому быстро самонагревает-ся и загорается с образованием белого дыма:
4Р + 5О 2 → 2Р 2 О 5 + 3100,6 кДж.
При смачивании раствором фосфора в сероуглероде горючих веществ происходит испарение сероуглерода ; остающийся на поверхности тонкий слой фосфора быстро окисляется и самовозгорается. В зависимости от кон-центрации раствора смоченные им вещества самовозго-раются через различные промежутки времени.
Хранить и резать фосфор следует под водой, так как на воздухе он может воспламениться от теплоты трения, причем белый фосфор очень ядовит.
Некоторые металлы, металлические порошки, пудры способны самовозгораться на воздухе за счет тепла, вы-деляющегося при реакции окисления. Из металлов в компактном состоянии этой способностью обладают ру-бидий и цезий, из металлических пудр - алюминиевая пудра и др. Для предотвращения самовозгорания алю-миниевой пудры ее приготовляют в среде инертного газа и затем перетирают с жирами, пленка которых предох-раняет пудры от окисления. Известны случаи, когда алюминиевая пудра под действием растворителя или на-гревания обезжиривалась и самовозгоралась.
Карбиды щелочных металлов К 2 С 2 , Na 2 C 2 , Li 2 С 2 са-мовозгораются не только на воздухе, но даже и в ат-мосфере СО 2 и SO 2 .
К самовозгоранию на воздухе способны также диэтиловый эфир и скипидар. Диэтиловый эфир при длитель-ном соприкосновении с воздухом на свету способен об-разовывать перекись диэтила (С 2 Н 5)О 2 , которая при ударе или нагревании до 75 0 С разлагается со взрывом и воспламеняет эфир. Скипидар также может самовозго-раться, если им смочены волокнистые материалы. При-чина самовозгорания - способность скипидара окислять-ся на воздухе при низких температурах. Известен случай самовозгорания ваты, смоченной скипидаром. Такой ва-той смывали масляную краску с декорации. Ночью вата, собранная в одном месте, самовозгорелась. Известны также случаи самовозгорания мха, смоченного скипида-ром.
Сульфоуголь, находясь в бумажных мешках, уложен-ных в штабель, способен самовозгораться. Были случаи его самовозгорания в первые 2-3 дня после укладки мешков в штабель.
Микробиологическое самовозгорание. Микробиологическим называется самовозгорание, возникающее в результате самонагревания под воздействием жизнедеятельности микроорганизмов в массе вещества, материала, смеси. К таким веществам относятся торф (в основном, фрезерный), растительные материалы: сено, клевер, силосная масса, солод, зерновые культуры, хлопок, скопление древесных опилок и подобные им материалы.
Особенно подвержены самовозгоранию недосушенные материалы. Влага и тепло способствуют размножению микроорганизмов в массе этих материалов уже при 10-18 0 С. Вследствие плохой теплопроводности растительных материалов выделяющееся при гниении тепло идёт на разогрев гниющего материала, температура его повышается и может достичь 70 0 С. Микроорганизмы при такой температуре погибают, однако повышение температуры в материале не прекращается, так как некоторые органические соединения в это время уже обугливаются.
Образующийся при этом пористый уголь имеет свойство адсорбировать пары и газы, что сопровождается выделением тепла. В случае малой теплоотдачи уголь нагревается до начала процесса окисления и температура растительных материалов повышается, достигая 200 0 С. Это приводит к разложению клетчатки и дальнейшему обугливанию массы. Процесс окисления пористого угля интенсифицируется, в результате чего температура растёт и возникает горение.
При увлажнении растительного сырья как при нормальной, так и повышенной температурах выделяются газы, в том числе и горючие. Так, при промачивании растительного сырья водяным паром или водой, при тушении горящего продукта начинается выделение СО, СН 4 , Н 2 в количествах, значительно превышающих НКПРП для каждого из этих газов. Поэтому использование для подавления очагов горения растительного сырья в силосах и бункерах только воды или пара может привести к взрыву хранилищ.
Химическое самовозгорание. Химическим называется самовозгорание, возникающее в результате химического взаимодействия веществ. Химическое самовозгорание возникает в месте контакта взаимодействующих веществ, реагирующих с выделением тепла. В этом случае самовозгорание наблюдается обычно на поверхно-сти материала, а затем распространяется вглубь. Процесс самонагревания начинается при температурах ниже 50 0 С. Некоторые химические соединения склонны к самонагреванию в результате контакта с кислородом воздуха и другими окислителями, друг с другом и водой. Причиной самонагревания является их высокая реакционная способность.
Вещества, самовозгорающиеся при контакте с окис-лителями . Многие вещества, в основном органические, при смешении или соприкосновении с окислителями спо-собны самовозгораться. К окислителям, вызывающим самовозгорание таких веществ, относятся: кислород воздуха, сжатый кисло-род, галогены , азотная кислота , перекись натрия и ба-рия, перманганат калия, хромовый ангидрид, двуокись свинца, селитры, хлораты, перхлораты, хлорная известь и др. Некоторые из смесей окислителей с горючими ве-ществами способны самовозгораться только при воздей-ствии на них серной или азотной кислоты или при ударе и слабом нагревании.
Самовозгорание на воздухе. Некоторые химические соединения склонны к самонагреванию в результате контакта с кислородом воздуха. Причиной самовозгорания служит их высокая реакционная способность в контакте с другими соединениями. Поскольку этот процесс происходит большей частью при комнатных температурах, его также относят к самовозгоранию. На самом деле, заметный процесс взаимодействия компонентов наблюдается при значительно более высоких температурах, и поэтому в качестве температурного показателя пожарной опасности таких веществ приводят их температуру самовоспламенения. Например, алюминиевая пудра самовозгорается на воздухе. Однако реакция образования окиси алюминия протекает при 913 К.
Сжатый кислород вызывает самовозгорание веществ (минерального масла), которые не самовозгораются в кислороде при нормальном давлении.
Хлор, бром, фтор и йод чрезвычайно активно соеди-няются с некоторыми горючими веществами, причем реакция сопровождается выделением большого количества тепла, что приводит к самовозгоранию веществ. Так, ацетилен , водород , метан и этилен в смеси с хлором самовозгораются на свету или от света горящего магния.
Если указанные газы присутствуют в момент выделения хлора из любого вещества, самовозгорание их происходит даже в темноте:
С 2 Н 2 + С1 2 → 2НС1 +2С,
СН 4 + 2С1 2 → 4НС1 + С и т. д.
Нельзя хранить галогены вместе с легко воспламе-няющимися жидкостями. Известно, что скипидар, рас-пределенный в каком-либо пористом веществе (в бумаге, ткани, вате), самовозгорается в хлоре.
Пары диэтилового эфира могут также самовозгораться в атмосфере хлора:
С 2 Н 5 ОС 2 Н 5 + 4С1 2 → Н 2 О + 8НС1 + 4С.
Красный фосфор моментально самовозгорается при соприкосновении с хлором или бромом.
Не только галогены в свободном состоянии, но и их соединения энергично вступают в реакцию с некоторыми металлами. Так, взаимодействие четыреххлористого эта-на C 2 H 2 CI 4 с металлическим калием происходит со взры-вом:
С 2 Н 2 С1 4 + 2К → 2КС1 + 2НС1 + 2С.
Смесь четыреххлористого углерода СС1 4 или четырех-бромистого углерода со щелочными металлами при на-гревании до 70 0 С взрывается.
Азотная кислота, разлагаясь, выделяет кислород, по-этому является сильным окислителем, способным выз-вать самовозгорание ряда веществ.
4HNO 8 → 4NO 2 + О 2 + 2Н 2 О.
При соприкосновении с азотной кислотой самовозго-раются скипидар и этиловый спирт.
Растительные материалы (солома, лен, хлопок, древесные опилки и стружки) самовозгораются, если на них попадет концентрированная азотная кислота.
При соприкосновении с перекисью натрия способны самовозгораться следующие горючие и легковоспламе-няющиеся жидкости: метиловый, этиловый, пропиловый, бутиловый, изоамиловый и бензиловый спирты, этиленгликоль, диэтиловый эфир, анилин, скипидар и уксусная кислота. Некоторые жидкости самовозгорались с перекисью натрия после введения в них небольшого количества воды. Так ведут себя уксусноэтиловый эфир (этилацетат), ацетон , глицерин и изобутиловый спирт.
Началом реакции служит взаимодействие воды с пере-кисью натрия и выделение при этом атомарного кисло-рода и тепла:
Na 2 O 2 + Н 2 О → 2NaOH + О.
Атомарный кислород в момент выделения окисляет горючую жидкость, и она самовозгорается. Порошок алюминия, опилки, уголь, сера и другие вещества в смеси с перекисью натрия моментально самовозгораются от попадания на них капли воды.
Сильным окислителем является перманганат калия КМnО 4 . Его смеси с твердыми горючими веществами крайне опасны. Они самовозгораются от действия кон-центрированных серной и азотной кислот, а также от удара и трения. Глицерин С 3 Н 5 (ОН) 3 и этиленгликоль С 2 Н 4 (ОН) 2 самовозгораются в смеси с перманганатом калия через несколько секунд после смешения.
Сильным окислителем является также хромовый ангидрид. При попадании на хромовый ангидрид самовозгораются следующие жидкости: метиловый, этиловый, бутиловый, изобутиловый и изоамиловый спирты; уксус-ный, масляный, бензойный, пропионовый альдегиды и паральдегид; диэтиловый эфир, этилацетат , амилацетат, метилдиоксан, диметилдиоксан; уксусная, пеларгоновая, нитрилакриловая кислоты; ацетон.
Смеси селитр, хлоратов, перхлоратов способны само-возгораться при действии на них серной, а иногда азот-ной кислоты. Причиной самовозгорания является выде-ление кислорода под действием кислот.
При действии серной кислоты на бертолетову соль происходит следу-ющая реакция :
H 2 SO 4 + 2КСlO 3 → K 2 SO 4 + 2НСlO 3 .
Хлорноватая кислота малоустойчива и при образова-нии распадается с выделением кислорода:
2НСlO 3 → 2НС1 + 3О 2 .
Карбиды щелочных металлов К 2 С 2, Na 2 C 2 , Li 2 C 2 самовозгораются не только на воздухе, но даже и в атмосфере СО 2, SO 2 .
Например, карбид кальция Са 2 С при контакте с водой выделяет горючий газ ацетилен С 2 Н 2, который в смеси с воздухом возгорается в результате того, что нагревается теплом, выделившимся в ходе реакции, Т св ацетилена равна 603 К.
Вещества, самовозгорающиеся при контакте с водой. К этой группе материалов относятся калий, натрий, ру-бидий, цезий, карбид кальция и карбиды щелочных ме-таллов, гидриды щелочных и щелочноземельных метал-лов, фосфиды кальция и натрия, силаны, негашеная из-весть, гидросульфид натрия и др.
Щелочные металлы - калий, натрий, рубидий и це-зий - взаимодействуют с водой с выделением водорода и значительного количества тепла:
2Na + 2Н 2 О → 2NaOH + Н 2 ,
2К + 2Н 2 О → 2КОН + Н 2 .
Выделяющийся водород самовоспламеняется и горит сов-местно с металлом только в том случае, если кусок ме-талла по объему больше горошины. Взаимодействие ука-занных металлов с водой иногда сопровождается взры-вом с разбрызгиванием расплавленного металла. Так же ведут себя гидриды щелочных и щелочноземельных металлов (КН, NaH, CaH 2) при взаимодействии с не-большим количеством воды:
NaH + Н 2 О → NaOH + Н 2 .
При взаимодействии карбида кальция с небольшим количеством воды выделяется столько тепла, что в при-сутствии воздуха образующийся ацетилен самовозгора-ется. При большом количестве воды этого не происходит. Карбиды щелочных металлов (например, Na 2 C 2 , K 2 C 2) при соприкосновении с водой взрываются, причем метал-лы сгорают, а углерод выделяется в свободном состоя-нии:
2Na 2 C 2 + 2Н 2 О + О 2 → 4NaOH + 4С.
Фосфид кальция Са 3 Р 2 при взаимодействии с водой об-разует фосфористый водород (фосфин):
Са 3 Р 2 + 6Н 2 О → 3Са(ОН) 2 + 2РН 3 .
Фосфин РН 3 является горючим газом, но самовозгорать-ся не способен. Совместно с РН 3 выделяется некоторое количество жидкого Р 2 Н 4 , который способен самовозго-раться на воздухе и может быть причиной воспламене-ния РН 3 .
Силаны, т. е. соединения кремния с различными ме-таллами, например Mg 2 Si, Fe 2 Si, при действии воды вы-деляют водородистый кремний, самовозгорающийся на воздухе:
Mg a Si + 4Н 2 О → 2Mg(OH) 2 + SiH 4 ,
SiH 4 + 2О 2 → SiO 2 + 2Н 2 О.
Перекись бария и перекись натрия хотя и взаимо-действуют с водой, но горючих газов при данной реакции не обра-зуется. Горение может возникнуть, если перекиси сме-шаны или соприкасаются с горючими веществами.
Оксид кальция (негашеная известь), реагируя с не-большим количеством воды, разогревается до свечения и может поджечь соприкасающиеся с ней горючие ма-териалы.
Гидросульфит натрия, являясь влажным, энергично окисляется с выделением тепла. В результате этого происходит самовозгорание серы, образующейся при распа-де гидросульфита.
Таким образом, самовозгорание и самонагревание горючих смесей, веществ и материалов, которые протекают при низких температурах, имеют ту же природу, что и самовоспламенение, но вследствие своей большей распространенности служат причиной пожаров гораздо чаще, чем самовоспламенение.
Вопросы для самоконтроля
1. В чем особенности тепловой теории горения?
2. В чем особенности цепной теории горения?
3. От чего зависит скорость выделения тепла при горении?
4. Каким уравнением описывается скорость горения?
5. От каких параметров зависит количество отводимого тепла?
6. При каком условии возможно самовоспламенение?
7. Что называется температурой самовоспламенения?
8. Что представляет собой индукционный период самовоспламенения?
9. От каких факторов зависит температура самовоспламенения?
10. Что называется воспламенением?
11. Что может служить источником воспламенения?
12. В чем отличие тления и пламенного горения?
13. Что называется температурой самовозгорания?
14. Каковы особенности теплового самовозгорания?
15. Каковы особенности химического самовозгорания?
16. Как происходит самовозгорание жиров и масел?
17. Что характеризует йодное число?
18. Каковы особенности микробиологического самовозгорания?
19. Что необходимо для предотвращения самовозгорания угля?
20. В чем сходство и отличие развитие процесса воспламенения и процесса самовоспламенения?


 Если вы решили заключить брак с гражданами кубы София хелльквист и принц карл филипп
Если вы решили заключить брак с гражданами кубы София хелльквист и принц карл филипп Игры друзья ангелов онлайн
Игры друзья ангелов онлайн Реальный расход топлива Опель Антара: все модификации бензиновых и дизельных двигателей Antara 2
Реальный расход топлива Опель Антара: все модификации бензиновых и дизельных двигателей Antara 2 Реальный расход горючего на Opel Antara по отзывам автовладельцев Опель антара 2
Реальный расход горючего на Opel Antara по отзывам автовладельцев Опель антара 2