Metódy spaľovania zemného plynu. Zemný plyn. Proces horenia
8.1. REAKCIE HORENIA
Všeobecne platí, že rýchla chemická reakcia kombinujúca horľavé zložky s kyslíkom, sprevádzaná intenzívnym uvoľňovaním tepla a prudkým zvýšením teploty produktov spaľovania. Spaľovacie reakcie sú opísané v tzv. stechiometrické rovnice charakterizujúce kvalitatívne a kvantitatívne reagujúce a vyplývajúce z jeho podstaty (Stechiometrické zloženie horľavej zmesi (z gréckeho základu, prvku Stoicheion a gréckeho prvku - merané metreom) - zloženie zmesi, v ktorej je okysličovadlo také množstvo, aké je potrebné na úplnú oxidáciu paliva), Všeobecná rovnica reakcie spaľovania akéhokoľvek uhľovodíka
CmHn + (m + n / 4) 02 = mCO2 + (n / 2) H20 + Q (8,1)
kde m, n je počet atómov uhlíka a vodíka v molekule; Q je tepelný účinok reakcie alebo spaľovacie teplo.
Spaľovacia reakcia niektorých plynov je uvedená v tabuľke. 8.1. Tieto rovnice sú vyvážené a nie je možné z nich súdiť ani reakčnú rýchlosť, ani mechanizmus chemických transformácií.
Tabuľka 8.1. Spaľovacia reakcia a teplo spaľovania suchých plynov (pri 0 ° C a 101,3 kPa)
| plynový | Horiaca reakcia | Spaľovacie teplo | |||||
|---|---|---|---|---|---|---|---|
| Molar, kJ / kmol | Hmotnosť, kJ / kg | Objem, kJ / m3 | |||||
| najvyššiu | dolná | najvyššiu | dolná | najvyššiu | dolná | ||
| vodík | H2 + 0,502 = H20 | 286,06 | 242,90 | 141 900 | 120 080 | 12 750 | 10 790 |
| Oxid uhoľnatý | CO + 0,5O2 = C02 | 283,17 | 283,17 | 10 090 | 10 090 | 12 640 | 12 640 |
| metán | CH4 + 2O2 = C02 + 2H20 | 880,90 | 800,90 | 55 546 | 49 933 | 39 820 | 35 880 |
| etán | C2H6 + 0,502 = 2CO2 + 3H20 | 1560,90 | 1425,70 | 52 019 | 47 415 | 70 310 | 64 360 |
| propán | C3H8 + 5H20 = 3CO2 + 4H20 | 2221,40 | 2041,40 | 50 385 | 46 302 | 101 210 | 93 180 |
| n-bután | 2880,40 | 2655,00 | 51 344 | 47 327 | 133 800 | 123 570 | |
| izobután | C4H10 + 6,5 02 = 4CO2 + 5H20 | 2873,50 | 2648,30 | 51 222 | 47 208 | 132 960 | 122 780 |
| pentán | C5H12 + 8O2 = 5CO2 + 6H20 | 3539,10 | 3274,40 | 49 052 | 45 383 | 169 270 | 156 630 |
| etylén | C2H4 +302 = 2CO2 + 2H20 | 1412,00 | 1333,50 | 50 341 | 47 540 | 63 039 | 59 532 |
| propylén | C3H6 + 4,5O2 = 3CO2 + 3H20 | 2059,50 | 1937,40 | 48 944 | 46 042 | 91 945 | 88 493 |
| butylén | C4H8 + 6O2 = 4CO2 + 4H20 | 2720,00 | 2549,70 | 48 487 | 45 450 | 121 434 | 113 830 |
T epl ov á f e k k t (teplo spaľovania) Q je množstvo tepla uvoľneného počas úplného spaľovania 1 kmol, 1 kg alebo 1 m3 plynu za normálnych fyzikálnych podmienok. Rozlišujte vyššiu výhrevnosť Q a nižšiu výhrevnosť Q n: vyššia výhrevnosť zahŕňa teplo kondenzácie vodnej pary v spaľovacom procese (v skutočnosti pri spaľovaní plynu vodná para kondenzuje, ale je odstránená spolu s inými produktmi spaľovania). Obvykle sa technické výpočty obvykle uskutočňujú pri najnižšom spaľovacom teple bez toho, aby sa zohľadňovalo kondenzačné teplo vodnej pary (≈ 2400 kJ / kg).
Účinnosť vypočítaná na základe nižšej výhrevnosti je formálne vyššia, ale kondenzačné teplo vodnej pary je dosť veľké a jeho použitie je viac ako rozumné. Potvrdzuje to aktívne používanie kontaktných výmenníkov tepla v technológii vykurovania, ktoré sú svojím dizajnom veľmi rozmanité.
Pre zmes horľavých plynov je najvyššie (a najnižšie) teplo spaľovania plynov určené pomerom
Q = r 1 Q 1 + r 2 Q 2 + ... + r n Q n (8,2)
kde r 1, r 2, ..., r n sú objemové (molárne, hmotnostné) podiely zložiek v zmesi; Q 1, Q 2, ..., Q n - teplo spaľovania komponentov.
Pomocou tabuľky. 8.1. Najvyššia a najnižšia výhrevnosť komplexného plynu kJ / m 3 sa môže určiť podľa týchto vzorcov:
Q = 127,5 Н 2 + 126,4 СО + 398 СН 4 + 703 С 2 Н 6 + 1012 8 8 Н 8 + 1338 C 4 H 10 + 1329 C 4 H 10 +
+ 1693 C5H12 + 630 C2H4 + 919 C3H6 + 1214 C4H8 (8.3)
Qn = 107,9 H2 + 126,4 CO + 358,8 CH4 + 643 C2H6 + 931,8 C8H8 + 1235 C4H10 + 1227 C4H10 +
+ 1566 C5H12 + 595 C2H4 + 884C8H6 + 1138C4H8 (8.4)
kde H2, CO, CH4 atď. - obsah jednotlivých zložiek v plynnom palive, približne. %.
Spaľovací proces je omnoho komplikovanejší ako proces podľa vzorca (8.1), pretože spolu s vetviacimi reťazcami sa prerušujú v dôsledku tvorby medziproduktov stabilných zlúčenín, ktoré podliehajú ďalším transformáciám pri vysokej teplote. Pri dostatočnej koncentrácii kyslíka sa vytvárajú konečné produkty: vodná para H20 a oxid uhličitý C02. S nedostatkom oxidačného činidla, ako aj ochladením reakčnej zóny sa môžu medziprodukty stabilizovať a preniknúť do životného prostredia.
Intenzita výroby tepla a zvýšenie teploty vedú k zvýšeniu množstva aktívnych častíc v reakčnom systéme. Táto vzájomná súvislosť reťazovej reakcie a teploty, charakteristická pre takmer všetky spaľovacie procesy, viedla k zavedeniu koncepcie reťazovo-tepelnej explózie - samotné chemické spaľovacie reakcie majú reťazový charakter a ich zrýchlenie nastáva v dôsledku uvoľnenia tepla a zvýšenia teploty v reakčnom systéme.
Rýchlosť chemickej reakcie v homogénnej zmesi je úmerná súčinu koncentrácií reagujúcich látok:
w = k 1 С 2 (8,5)
kde С 1 a С 2 - koncentrácie reagujúcich zložiek, kmol / m 3; k je rýchlostná konštanta reakcie v závislosti od povahy reaktantov a teploty.
Keď je plyn horený, koncentrácie reakčných zložiek sa môžu podmienečne považovať za nezmenené, pretože v spaľovacej zóne dochádza k nepretržitému prísunu čerstvých zložiek jednoznačného zloženia.
Konštanta rýchlosti reakcie (podľa Arrheniovej rovnice):
K = K0e-E / RT (8,6)
kde K 0 je preexponenciálny faktor akceptovateľný pre biometrické homogénne zmesi, -1,0; Е - aktivačná energia, kJ / kmol; R je univerzálna plynová konštanta, J / (kg K); T je absolútna teplota, K (° C); e - základ prirodzených logaritmov.
Preexponenciálny faktor Ko môže byť interpretovaný ako konštanta odrážajúca úplnosť kolízie molekúl a E ako minimálna energia prerušenia väzieb molekúl a tvorba aktívnych častíc zabezpečujúcich účinnosť kolízií. Pre bežné horľavé zmesi je to v rozmedzí (80 ÷ 150) 103 kJ / km.
Rovnica (8.6) ukazuje, že rýchlosť chemických reakcií dramaticky stúpa so zvyšujúcou sa teplotou: napríklad zvýšenie teploty z 500 na 1 000 K spôsobuje zvýšenie horiacej reakcie o 2 104 4 5 10 8 krát (v závislosti od aktivačnej energie).
Rýchlosť spaľovacích reakcií je ovplyvnená ich reťazovým charakterom. Atómy a radikály pôvodne generované reakciou vstupujú do zlúčenín s východiskovými materiálmi a medzi sebou, vytvárajú finálne produkty a nové častice, opakujú rovnaký reťazec reakcií. Zvyšujúca sa tvorba takýchto častíc vedie k „zrýchleniu“ chemických reakcií - v skutočnosti k výbuchu celej zmesi.
Spaľovanie uhľovodíkov pri vysokej teplote je komplexné a je spojené s tvorbou aktívnych častíc vo forme atómov a radikálov, ako aj medziproduktov molekulárnych zlúčenín. Ako príklad uvádzame reakciu spaľovania najjednoduchšieho uhľovodíka - metánu:
- H + 02- ›OH + O
СН 4 + ОН - ›СН 3 + Н 2 О
СН 4 + О - ›СН 2 + Н 2 О - СН 3 + О 2 - ›НСНО + ОН
СН 2 + О 2 - ›НСНО + О - НСНО + ОН - ›НСО + Н 2 О
NSNO + O - ›CO + H20
NSO + 02- ›CO + O + OH - CO + O - ›CO 2
CO + HE - ›CO 2 + H
Výsledok jedného cyklu:
2СН 4 + 4О 2 - ›2СО 2 + 4Н 2 О
8.2. VÝPOČTY BURNINGU
Kyslík na spaľovanie pochádza zo vzduchu ako jeho súčasť. Pri výpočtoch sa predpokladá, že zloženie objemu suchého vzduchu je takéto:
kyslík - 21,0%, dusík - 79,0%.
Podľa uvedených informácií je 1 m3 kyslíka obsiahnuté v 100/21 = 4,76 m3 vzduchu alebo 79/21 = 3,76 m3 dusíka na 1 m3 kyslíka. Vzhľadom na to, že 1 kmol plynu za normálnych podmienok zaberá objem 22,4 litra, spaľovacia reakcia (pozri rovnicu 8.1) akéhokoľvek uhľovodíka vo vzduchu sa dá písať vo všeobecnej forme:
CmHn + (t + n / 4) (02 + 3,76N2) = tCO2 + (n / 2) H20 + (t + n / 4) 3,76N2
Požiadavky na kyslík a vzduch počas spaľovania rôznych plynov, vypočítané z vyššie uvedených spaľovacích reakcií, sú uvedené v tabuľke č. 8.2.
Tabuľka 8.2. Teoretická potreba suchého kyslíka a vzduchu, m 3 a objem produktov spaľovania plynu pri spaľovaní plynu 1 m 3
| plynový | Teoretická potreba | Produkty spaľovania | ||||
|---|---|---|---|---|---|---|
| kyslík | vzduchu | oxid uhličitý | vodná para | dusík | iba | |
| Vodík H2 | 0,5 | 2,38 | – | 1,0 | 1,88 | 2,88 |
| Oxid uhoľnatý CO | 0,5 | 2,38 | 1,0 | – | 1,88 | 2,88 |
| Metán CH4 | 2,0 | 9,52 | 1,0 | 2,0 | 7,52 | 10,52 |
| Etán C2H6 | 3,5 | 16,66 | 2,0 | 3,0 | 13,16 | 18,16 |
| Propán C3H8 | 5,0 | 23,80 | 3,0 | 4,0 | 18,80 | 25,80 |
| Bután C4H10 | 6,5 | 30,94 | 4,0 | 5,0 | 24,44 | 33,44 |
| Pentán C5H12 | 8,0 | 38,08 | 5,0 | 6,0 | 30,08 | 41,08 |
| Etylén C2H4 | 3,0 | 14,28 | 2,0 | 2,0 | 11,28 | 15,28 |
| Propylén C3H6 | 4,5 | 21,42 | 3,0 | 3,0 | 16,92 | 22,92 |
| Butylén C4H8 | 6,0 | 28,56 | 4,0 | 4,0 | 22,56 | 30,56 |
| Pentilný C5H10 | 7,5 | 35,70 | 5,0 | 5,0 | 28,20 | 38,20 |
| Acetylén C2H2 | 2,5 | 11,90 | 2,0 | 1,0 | 9,40 | 12,40 |
Pri zložitých plynoch sa prietok suchého vzduchu V c, m 3 / m3 vypočíta podľa vzorca, ktorý zohľadňuje spotrebu kyslíka jednotlivých zložiek zmesi:
Vc = 4,76 / 100 (0,5H2 + 0,5SO + 2CH4 + 3,5С2H6 + 5С3H8 + 6,5 С4 Н 10 + 3С2H4 + 4,5 Ä3N 6 + 6C4H8-02) (8.7)
Teoretický prietok vlhkého vzduchu Vl, m / m 3, je väčší, ako je určené vzorcom (8.7) pre objem obsiahnutej vodnej pary:
Vl = V s + 0,001244d vo V s (8,8)
kde d - vlhkosť, g / m 3.
S neznámym chemickým zložením plynov, ale so známou nižšou výhrevnou hodnotou Q n, kJ / m 3, teoretickým prietokom vzduchu V t, m 3 / m 3,
V t ≈ Q n / 3770 (8,9)
Skutočný prietok vzduchu Vf, m 3 / m 3 sa vždy považuje za dosť veľký:
V Fe = Vt a (8,10)
kde α je koeficient prebytočného vzduchu, ktorý spĺňa požiadavky GOST. Na úplné spálenie paliva musí byť hodnota a vyššia ako 1. Zloženie a objem produktov spaľovania vypočítaných zo spaľovacích reakcií určitých plynov v suchom vzduchu sú uvedené v tabuľke 1. 8.2.
8.3. TEPLOTA POŽIARU
V tepelnej technike sú nasledujúce teploty horenia plynov rôzne: výroba tepla, kalorimetrická, teoretická a skutočná (vypočítaná). Produktivita tepla t W - maximálna teplota produktov úplného spaľovania plynu v adiabatických podmienkach s súčiniteľom prebytku vzduchu α = 1,0 a pri teplote plynu a vzduchu rovnej 0 ° C:
t ж = Q n / (∑Vc p) (8.11)
kde Qn - výhrevnosť plynu, kJ / m3; ∑Vc p je súčet súčinov objemov oxidu uhličitého, vodnej pary a dusíka vytvoreného počas spaľovania 1 m 3 plynu (m 3 / m 3) a ich priemerných objemových tepelných kapacít pri konštantnom tlaku v teplotnom rozsahu od 0 ° C do t Ж (kJ / (m3 o ° C).
V dôsledku nestálosti tepelnej kapacity plynov je tepelný výkon určený metódou postupných aproximácií. Ako počiatočný parameter sa berie do úvahy jeho hodnota pre zemný plyn (~ 2 000 ° С), pričom α = 1,0 sa podľa tabuľky určujú objemy zložiek spalín. 8.3 sa zistí ich priemerná tepelná kapacita a potom sa podľa vzorca (8.11) zohľadní tepelný výkon plynu. Ak sa v dôsledku výpočtu ukáže, že je nižšia alebo vyššia ako použitá teplota, nastaví sa iná teplota a výpočet sa opakuje.
Tabuľka 8.3. Priemerný objemový tepelný výkon plynov, kJ / (m 3 ° С)
Teplota, ° С |
C02 | N 2 | 02 | CO | CH4 | H2 | H20 (vodná para) | vzduchom | |
|---|---|---|---|---|---|---|---|---|---|
| sucho | mokrý pri 1 m 3 suchý plyn |
||||||||
| 0 | 1,5981 | 1,2970 | 1,3087 | 1,3062 | 1,5708 | 1,2852 | 1,4990 | 1,2991 | 1,3230 |
| 100 | 1,7186 | 1,2991 | 1,3209 | 1,3062 | 1,6590 | 1,2978 | 1,5103 | 1,3045 | 1,3285 |
| 200 | 1,8018 | 1,3045 | 1,3398 | 1,3146 | 1,7724 | 1,3020 | 1,5267 | 1,3142 | 1,3360 |
| 300 | 1,8770 | 1,3112 | 1,3608 | 1,3230 | 1,8984 | 1,3062 | 1,5473 | 1,3217 | 1,3465 |
| 400 | 1,9858 | 1,3213 | 1,3822 | 1,3356 | 2,0286 | 1,3104 | 1,5704 | 1,3335 | 1,3587 |
| 500 | 2,0030 | 1,3327 | 1,4024 | 1,3482 | 2,1504 | 1,3104 | 1,5943 | 1,3469 | 1,3787 |
| 600 | 2,0559 | 1,3453 | 1,4217 | 1,3650 | 2,2764 | 1,3146 | 1,6195 | 1,3612 | 1,3873 |
| 700 | 2,1034 | 1,3587 | 1,3549 | 1,3776 | 2,3898 | 1,3188 | 1,6464 | 1,3755 | 1,4020 |
| 800 | 2,1462 | 1,3717 | 1,4549 | 1,3944 | 2,5032 | 1,3230 | 1,6737 | 1,3889 | 1,4158 |
| 900 | 2,1857 | 1,3857 | 1,4692 | 1,4070 | 2,6040 | 1,3314 | 1,7010 | 1,4020 | 1,4293 |
| 1000 | 2,2210 | 1,3965 | 1,4822 | 1,4196 | 2,7048 | 1,3356 | 1,7283 | 1,4141 | 1,4419 |
| 1100 | 2,2525 | 1,4087 | 1,4902 | 1,4322 | 2,7930 | 1,3398 | 1,7556 | 1,4263 | 1,4545 |
| 1200 | 2,2819 | 1,4196 | 1,5063 | 1,4448 | 2,8812 | 1,3482 | 1,7825 | 1,4372 | 1,4658 |
| 1300 | 2,3079 | 1,4305 | 1,5154 | 1,4532 | – | 1,3566 | 1,8085 | 1,4482 | 1,4771 |
| 1400 | 2,3323 | 1,4406 | 1,5250 | 1,4658 | – | 1,3650 | 1,8341 | 1,4582 | 1,4876 |
| 1500 | 2,3545 | 1,4503 | 1,5343 | 1,4742 | – | 1,3818 | 1,8585 | 1,4675 | 1,4973 |
| 1600 | 2,3751 | 1,4587 | 1,5427 | – | – | – | 1,8824 | 1,4763 | 1,5065 |
| 1700 | 2,3944 | 1,4671 | 1,5511 | – | – | – | 1,9055 | 1,4843 | 1,5149 |
| 1800 | 2,4125 | 1,4746 | 1,5590 | – | – | – | 1,9278 | 1,4918 | 1,5225 |
| 1900 | 2,4289 | 1,4822 | 1,5666 | – | – | – | 1,9698 | 1,4994 | 1,5305 |
| 2000 | 2,4494 | 1,4889 | 1,5737 | 1,5078 | – | – | 1,9694 | 1,5376 | 1,5376 |
| 2100 | 2,4591 | 1,4952 | 1,5809 | – | – | – | 1,9891 | – | – |
| 2200 | 2,4725 | 1,5011 | 1,5943 | – | – | – | 2,0252 | – | – |
| 2300 | 2,4860 | 1,5070 | 1,5943 | – | – | – | 2,0252 | – | – |
| 2400 | 2,4977 | 1,5166 | 1,6002 | – | – | – | 2,0389 | – | – |
| 2500 | 2,5091 | 1,5175 | 1,6045 | – | – | – | 2,0593 | – | – |
Produktivita tepla bežných jednoduchých a zložitých plynov pri spaľovaní v suchom vzduchu je uvedená v tabuľke. 8.4. Pri spaľovaní plynu v atmosférickom vzduchu, ktorý obsahuje asi 1% hm. % vlhkosti, tepelný výkon je znížený o 25–30 ° C.
Tabuľka 8.4. Výroba tepla v plynoch v suchom vzduchu
| Jednoduchý plyn | Produktivita tepla, ° С | Ťažký plyn priemerné zloženie |
Približný tepelný výkon, ° C |
|---|---|---|---|
| vodík | 2235 | Polia na zemný plyn |
2040 |
| Oxid uhoľnatý | 2370 | Polia z prírodného oleja |
2080 |
| metán | 2043 | koks |
2120 |
| etán | 2097 | Destilácia bridlíc pri vysokej teplote |
1980 |
| propán | 2110 | Výbuch parou a kyslíkom pod tlakom |
2050 |
| bután | 2118 | Generátor z tukov |
1750 |
| pentán | 2119 | Vyfukovanie pary generátora zo štíhlych palív |
1670 |
| etylén | 2284 | Skvapalnené (50% Ä 3 Н 4 + 50% С 4 Н 10) |
2115 |
| acetylén | 2620 | 2210 |
Kalorimetrická teplota horenia t - teplota, stanovená bez zohľadnenia disociácie vodnej pary a oxidu uhličitého, ale so zohľadnením skutočnej počiatočnej teploty plynu a vzduchu. Od tepelného výkonu t sa líši tým, že teplota plynu a vzduchu, ako aj koeficient prebytku vzduchu a, sa merajú podľa ich skutočných hodnôt. Určite, že to môže byť vzorec:
t k = (Qn + q nat) / (ΣVc p) (8,12)
kde q nat je tepelný obsah (fyzikálne teplo) plynu a vzduchu, meraný od 0 ° С, kJ / m 3.
Zemný plyn a skvapalnené uhľovodíkové plyny sa zvyčajne pred spaľovaním nezohrievajú a ich objem je malý v porovnaní s objemom vzduchu spaľovaného. Preto pri určovaní kalorimetrickej teploty možno ignorovať tepelný obsah plynov. Pri spaľovaní plynov s nízkou výhrevnosťou (generátor, vysoké pece, atď.) Má ich tepelný obsah (najmä zahrievaný pred spaľovaním) veľmi významný vplyv na kalorimetrickú teplotu.
Závislosť kalorimetrickej teploty zemného plynu s priemerným zložením na vzduchu s teplotou 0 ° C a vlhkosťou 1% koeficientu prebytku vzduchu α je uvedená v tabuľke 1. 8.5, pre skvapalnený uhľovodíkový plyn pri spaľovaní na suchom vzduchu - v tabuľke č. 8.7. Tabuľka údajov. 8.5 - 8.7 je možné s dostatočnou presnosťou sledovať kalorimetrickú teplotu spaľovania iných prírodných plynov, ktorých zloženie je relatívne blízke, a uhľovodíkových plynov prakticky akéhokoľvek zloženia. Ak je potrebné pri spaľovaní plynov s malými koeficientmi prebytku vzduchu dosiahnuť vysokú teplotu, ako aj zvýšiť účinnosť pecí, v praxi ohrievajú vzduch, čo vedie k zvýšeniu kalorimetrickej teploty (pozri tabuľku 8.6).
Tabuľka 8.5. Kalorimetrické a teoretické teploty spaľovania zemného plynu vo vzduchu s t = 0 ° C a vlhkosťou 1%, v závislosti od súčiniteľa prebytku vzduchu α
| Teoretická teplota horenia t t, ° С | Koeficient prebytku vzduchu α | Kalorimetrická teplota horenia t к, ° С | ||
|---|---|---|---|---|
| 1,0 | 2010 | 1920 | 1,33 | 1620 |
| 1,02 | 1990 | 1900 | 1,36 | 1600 |
| 1,03 | 1970 | 1880 | 1,40 | 1570 |
| 1,05 | 1940 | 1870 | 1,43 | 1540 |
| 1,06 | 1920 | 1860 | 1,46 | 1510 |
| 1,08 | 1900 | 1850 | 1,50 | 1470 |
| 1,10 | 1880 | 1840 | 1,53 | 1440 |
| 1,12 | 1850 | 1820 | 1,57 | 1410 |
| 1,14 | 1820 | 1790 | 1,61 | 1380 |
| 1,16 | 1800 | 1770 | 1,66 | 1350 |
| 1,18 | 1780 | 1760 | 1,71 | 1320 |
| 1,20 | 1760 | 1750 | 1,76 | 1290 |
| 1,22 | 1730 | – | 1,82 | 1260 |
| 1,25 | 1700 | – | 1,87 | 1230 |
| 1,28 | 1670 | – | 1,94 | 1200 |
| 1,30 | 1650 | – | 2,00 | 1170 |
Tabuľka 8.6. Kalorimetrická teplota horenia zemného plynu t к, ° С, v závislosti od súčiniteľa prebytku suchého vzduchu a jeho teploty (zaokrúhlené hodnoty)
| Koeficient prebytku vzduchu α | Teplota suchého vzduchu, ° С | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 20 | 100 | 200 | 300 | 400 | 500 | 600 | 700 | 800 | |
| 0,5 | 1380 | 1430 | 1500 | 1545 | 1680 | 1680 | 1740 | 1810 | 1860 |
| 0,6 | 1610 | 1650 | 1715 | 1780 | 1840 | 1900 | 1960 | 2015 | 2150 |
| 0,7 | 1730 | 1780 | 1840 | 1915 | 1970 | 2040 | 2100 | 2200 | 2250 |
| 0,8 | 1880 | 1940 | 2010 | 2060 | 2130 | 2200 | 2260 | 2330 | 2390 |
| 0,9 | 1980 | 2030 | 2090 | 2150 | 2220 | 2290 | 2360 | 2420 | 2500 |
| 1,0 | 2050 | 2120 | 2200 | 2250 | 2320 | 2385 | 2450 | 2510 | 2560 |
| 1,2 | 1810 | 1860 | 1930 | 2000 | 2070 | 2140 | 2200 | 2280 | 2350 |
| 1,4 | 1610 | 1660 | 1740 | 1800 | 2870 | 1950 | 2030 | 2100 | 2160 |
| 1,6 | 1450 | 1510 | 1560 | 1640 | 1730 | 1800 | 1860 | 1950 | 2030 |
| 1,8 | 1320 | 1370 | 1460 | 1520 | 1590 | 1670 | 1740 | 1830 | 1920 |
| 2,0 | 1220 | 1270 | 1360 | 1420 | 1490 | 1570 | 1640 | 1720 | 1820 |
Tabuľka 8.7. Kalorimetrická teplota horenia t na technický propán v suchom vzduchu pri t = 0 ° C, v závislosti od súčiniteľa prebytku vzduchu α
| Koeficient prebytku vzduchu α | Kalorimetrická teplota horenia t к, ° С | Koeficient prebytku vzduchu α | Kalorimetrická teplota horenia t к, ° С |
|---|---|---|---|
| 1,0 | 2110 | 1,45 | 1580 |
| 1,02 | 2080 | 1,48 | 1560 |
| 1,04 | 2050 | 1,50 | 1540 |
| 1,05 | 2030 | 1,55 | 1500 |
| 1,07 | 2010 | 1,60 | 1470 |
| 1,10 | 1970 | 1,65 | 1430 |
| 1,12 | 1950 | 1,70 | 1390 |
| 1,15 | 1910 | 1,75 | 1360 |
| 1,20 | 1840 | 1,80 | 1340 |
| 1,25 | 1780 | 1,85 | 1300 |
| 1,27 | 1750 | 1,90 | 1270 |
| 1,30 | 1730 | 1,95 | 1240 |
| 1,35 | 1670 | 2,00 | 1210 |
| 1,40 | 1630 | 2,10 | 1170 |
Teoretická teplota horenia t T je maximálna teplota stanovená podobne ako kalorimetrická t K, ale upravená pre endotermické (vyžadujúce teplo) reakcie disociácie oxidu uhličitého a vodnej pary, dosahujúce so zvýšením objemu:
CO 2 ‹-› CO + 0,5O 2 - 283 mJ / mol (8.13)
H20 ‹-› H 2 + 0,5O 2 - 242 mJ / mol (8.14)
Pri vysokých teplotách môže disociácia viesť k tvorbe atómových atómov vodíka, kyslíka a hydroxylových skupín OH. Okrem toho sa pri spaľovaní plynu vždy vytvára určité množstvo oxidu dusnatého. Všetky tieto reakcie sú endotermické a vedú k zníženiu teploty spaľovania.
Teoretická teplota horenia sa môže určiť podľa tohto vzorca:
t T = (Q n + q fiz - q dis) / (ΣVc p) (8,15)
kde q dis - celkové náklady na tepelnú disociáciu CO2 a H20 v produktoch spaľovania, kJ / m3; ΣVc p - súčet súčinu objemu a priemernej tepelnej kapacity produktov spaľovania vzhľadom na disociáciu na 1 m3 plynu.
Tabuľka 8.8. Stupeň disociácie vodnej pary H20 a oxidu uhličitého CO2 v závislosti od parciálneho tlaku
| Teplota, ° С | Parciálny tlak, MPa | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 0,004 | 0,006 | 0,008 | 0,010 | 0,012 | 0,014 | 0,016 | 0,018 | 0,020 | 0,025 | 0,030 | 0,040 | |
| Vodná para H20 | ||||||||||||
| 1600 | 0,85 | 0,75 | 0,65 | 0,60 | 0,58 | 0,56 | 0,54 | 0,52 | 0,50 | 0,48 | 0,46 | 0,42 |
| 1700 | 1,45 | 1,27 | 1,16 | 1,08 | 1,02 | 0,95 | 0,90 | 0,85 | 0,8 | 0,76 | 0,73 | 0,67 |
| 1800 | 2,40 | 2,10 | 1,90 | 1,80 | 1,70 | 1,60 | 1,53 | 1,46 | 1,40 | 1,30 | 1,25 | 1,15 |
| 1900 | 4,05 | 3,60 | 3,25 | 3,0 | 2,85 | 2,70 | 2,65 | 2,50 | 2,40 | 2,20 | 2,10 | 1,9 |
| 2000 | 5,75 | 5,05 | 4,60 | 4,30 | 4,0 | 3,80 | 3,55 | 3,50 | 3,40 | 3,15 | 2,95 | 2,65 |
| 2100 | 8,55 | 7,50 | 6,80 | 6,35 | 6,0 | 5,70 | 5,45 | 5,25 | 5,10 | 4,80 | 4,55 | 4,10 |
| 2200 | 12,3 | 10,8 | 9,90 | 9,90 | 8,80 | 8,35 | 7,95 | 7,65 | 7,40 | 6,90 | 6,50 | 5,90 |
| 2300 | 16,0 | 15,0 | 13,7 | 12,9 | 12,2 | 11,6 | 11,1 | 10,7 | 10,4 | 9,6 | 9,1 | 8,4 |
| 2400 | 22,5 | 20,0 | 18,4 | 17,2 | 16,3 | 15,6 | 15,0 | 14,4 | 13,9 | 13,0 | 12,2 | 11,2 |
| 2500 | 28,5 | 25,6 | 23,5 | 22,1 | 20,9 | 20,0 | 19,3 | 18,6 | 18,0 | 16,8 | 15,9 | 14,6 |
| 3000 | 70,6 | 66,7 | 63,8 | 61,6 | 59,6 | 58,0 | 56,5 | 55,4 | 54,3 | 51,9 | 50,0 | 47,0 |
| Oxid uhličitý CO 2 | ||||||||||||
| 1500 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,4 | 0,4 | 0,4 | 0,4 | 0,4 | – |
| 1600 | 2,0 | 1,8 | 1,6 | 1,5 | 1,45 | 1,4 | 1,35 | 1,3 | 1,25 | 1,2 | 1,1 | |
| 1700 | 3,8 | 3,3 | 3,0 | 2,8 | 2,6 | 2,5 | 2,4 | 2,3 | 2,2 | 2,0 | 1,9 | |
| 1800 | 6,3 | 5,5 | 5,0 | 4,6 | 4,4 | 4,2 | 4,0 | 3,8 | 3,7 | 3,5 | 3,3 | |
| 1900 | 10,1 | 8,9 | 8,1 | 7,6 | 7,2 | 6,8 | 6,5 | 6,3 | 6,1 | 5,6 | 5,3 | |
| 2000 | 16,5 | 14,6 | 13,4 | 12,5 | 11,8 | 11,2 | 10,8 | 10,4 | 10,0 | 9,4 | 8,8 | |
| 2100 | 23,9 | 21,3 | 19,6 | 18,3 | 17,3 | 16,5 | 15,9 | 15,3 | 14,9 | 13,9 | 13,1 | |
| 2200 | 35,1 | 31,5 | 29,2 | 27,5 | 26,1 | 25,0 | 24,1 | 23,3 | 22,6 | 21,2 | 20,1 | |
| 2300 | 44,7 | 40,7 | 37,9 | 35,9 | 34,3 | 32,9 | 31,8 | 30,9 | 30,0 | 28,2 | 26,9 | |
| 2400 | 56,0 | 51,8 | 48,8 | 46,5 | 44,6 | 43,1 | 41,8 | 40,6 | 39,6 | 37,5 | 35,8 | |
| 2500 | 66,3 | 62,2 | 59,3 | 56,9 | 55,0 | 53,4 | 52,0 | 50,7 | 49,7 | 47,3 | 45,4 | |
| 3000 | 94,9 | 93,9 | 93,1 | 92,3 | 91,7 | 90,6 | 90,1 | 89,6 | 88,5 | 87,6 | 86,8 | |
Ako je zrejmé z tabuľky. 8.8 pri teplotách do 1600 ° C možno stupeň disociácie ignorovať a teoretická teplota spaľovania sa môže považovať za rovnú kalorimetrickej. Pri vyšších teplotách môže stupeň disociácie významne znížiť teplotu v pracovnom priestore. V praxi to tak nie je potrebné, teoretická teplota horenia by sa mala určovať iba pre vysokoteplotné pece, ktoré pracujú s predhriatym vzduchom (napríklad pece s otvoreným ohňom). Pre kotolne to nie je potrebné.
Tabuľka 8.9. maximálna
vznikajúca teplota
vo voľnom ohni, ° С
Skutočná (vypočítaná) teplota spalín t d - teplota, ktorá sa dosiahne v reálnych podmienkach v najteplejším bode horáka. Je nižšia ako teoretická a závisí od tepelných strát do životného prostredia, stupňa uvoľňovania tepla zo spaľovacej zóny žiarením, dĺžky spaľovacieho procesu v priebehu času atď. o teplote v peci so zavedením experimentálne stanovených korekčných faktorov v nich:
t d = t t η (8.16)
kde η je tzv pyrometrický koeficient v rámci limitov:
- pre vysoko kvalitné tepelné a vykurovacie pece s tepelnou izoláciou - 0,75–0,85;
- pre uzavreté pece bez tepelnej izolácie - 0,70–0,75;
- pre tienené kotlové pece - 0,60–0,75.
V praxi by sme mali poznať nielen vyššie uvedené adiabatické teploty spaľovania, ale aj maximálne teploty vyskytujúce sa v plameňoch. Ich približné hodnoty sú obvykle stanovené experimentálne spektrografickými metódami. Maximálne teploty, ktoré sa vyskytujú vo voľnom plameni vo vzdialenosti 5 - 10 mm od vrcholu prednej časti kónického spaľovania, sú uvedené v tabuľke. 8.9. Analýza údajov ukazuje, že maximálna teplota v plameni je menšia ako tepelný výkon (kvôli nákladom na teplo pri disociácii H20 a CO2 a odstraňovaní tepla z plameňovej zóny).
8.4. TEPLOTA SAMOSTATNÝCH INFORMÁCIÍ
Na spustenie spaľovacích reakcií sú potrebné podmienky vznietenia zmesi paliva a oxidačného činidla. Zapaľovanie môže byť spontánne a nútené (zapaľovanie).
Teplota samovznietenia - minimálna teplota, pri ktorej sa v zahrievanej zmesi plyn-vzduch začína procesom spontánneho (t.j. bez vonkajšieho prívodu tepla) v dôsledku uvoľňovania tepla spaľovaním častíc plynu.
Teplota samovznietenia nie je pre daný plyn ustálená a závisí od mnohých parametrov: jeho obsah v zmesi plynu a vzduchu, stupeň homogenity zmesi, tvar a veľkosť nádoby, v ktorej sa zmes zahrieva, jej rýchlosť a spôsob zahrievania, katalytický účinok stien nádoby, tlak, pod ktorým zmes. Presné zváženie týchto faktorov je veľmi ťažké, takže v praxi napríklad pri hodnotení nebezpečenstva výbuchu používajte experimentálne údaje (pozri tabuľku. 8.10).
Tabuľka 8.10. Najnižšie namerané teploty samovznietenia určitých plynov a pár zmiešané so vzduchom pri atmosférickom tlaku.
Teplota samovznietenia horľavých plynov v kyslíku je o niečo nižšia ako vo vzduchu. Zavedenie zloženia plynov z balastných nečistôt (dusík a oxid uhličitý) vedie k zvýšeniu teploty samovznietenia. Prítomnosť komponentov s nízkou teplotou samovznietenia v zložitých plynoch vedie k zníženiu teploty samovznietenia zmesi.
Nútené zapálenie (zapálenie) sa vykonáva zapálením zmesi v jednom alebo vo viacerých bodoch zdrojom vysokej teploty - otvoreným plameňom alebo elektrickou iskrou v bode, kde plyn uniká z požiarnych kanálov horákov do objemu pece. Zapálenie sa líši od samovznietenia tým, že horľavá zmes nevytvára plameň v celom objeme, ale iba v malej časti. Chladič zo zahrievanej zóny vyžaduje, aby tepelná intenzita zdroja zapálenia prekročila toto odvádzanie tepla. Po zapálení sa odstráni zdroj zapálenia a dôjde k horeniu v dôsledku šírenia prednej časti plameňa.
8.5. LIMITY HORĽAVOSTI A VÝBUCHU
Zmesi plynu a vzduchu sa môžu vznietiť (explodovať) iba vtedy, ak je obsah plynu v zmesi v rámci určitých limitov (pre každý plyn). Z tohto hľadiska existujú horné a dolné koncentračné limity horľavosti. Spodná hranica zodpovedá minimu a horná hranica maximálnemu množstvu plynu v zmesi, v ktorej sa vznietia (počas zapálenia) a spontánne (bez prílivu tepla z vonkajšej strany) šírenie plameňa (samovznietenie). Rovnaké limity zodpovedajú podmienkam výbušných zmesí plynu a vzduchu.
Ak je obsah plynu v zmesi plyn-vzduch nižší ako dolný limit horľavosti, takáto zmes nemôže horieť a explodovať, pretože teplo uvoľnené v blízkosti zdroja zapálenia nestačí na zahriatie zmesi na teplotu vznietenia. Ak je obsah plynu v zmesi medzi dolnou a hornou medzou horľavosti, zapálená zmes sa vznieti a horí v blízkosti zdroja vznietenia a keď je odstránená. Takáto zmes je výbušná. Čím širší je rozsah limitov horľavosti (nazývaný tiež výbušné limity) a dolný limit, tým výbušnejší je plyn. Nakoniec, ak obsah plynu v zmesi prekročí horný limit horľavosti, potom množstvo vzduchu v zmesi nestačí na úplné spálenie plynu.
Existencia limitov horľavosti je spôsobená tepelnými stratami počas spaľovania. Ak sa horľavá zmes zriedi vzduchom, kyslíkom alebo plynom, zvýšia sa tepelné straty, rýchlosť šírenia plameňa sa zníži a horenie sa zastaví po odstránení zdroja zapálenia.
Tabuľka 8.11. Limity horľavosti plynov zmiešaných so vzduchom (pri t = 20 ° C a p = 101,3 kPa)
| plynový | Obsah plynu v plynnej zmesi asi. % | maximum |
Prebytok vzduchu α v medziach vznietenia | ||||
|---|---|---|---|---|---|---|---|
| S limitmi horľavosti | Keď stechiometrické zloženie zmesi | Keď je zloženie zmesi, udáva maximálny výbušný tlak | |||||
| dolná | vrchný | dolná | vrchný | ||||
| vodík | 4,0 | 75,0 | 29,5 | 32,3 | 0,739 | 9,8 | 0,15 |
| Oxid uhoľnatý | 12,5 | 74,0 | 29,5 | – | – | 2,9 | 0,15 |
| metán | 5,0 | 15,0 | 9,5 | 9,8 | 0,717 | 1,8 | 0,65 |
| etán | 3,2 | 12,5 | 5,68 | 6,28 | 0,725 | 1,9 | 0,42 |
| propán | 2,3 | 9,5 | 4,04 | 4,60 | 0,858 | 1,7 | 0,40 |
| n-bután | 1,7 | 8,5 | 3,14 | 3,6 | 0,858 | 1,7 | 0,35 |
| izobután | 1,8 | 8,4 | 3,14 | – | – | ~1,8 | 0,35 |
| pentán | 1,4 | 7,8 | 2,56 | 3,0 | 0,865 | 1,8 | 0,31 |
| etylén | 3,0 | 16,0 | 6,5 | 8,0 | 0,886 | 2,2 | 0,17 |
| propylén | 2,4 | 10,0 | 4,5 | ~5,1 | ~0,89 | 1,9 | 0,37 |
| butylén | 1,7 | 9,0 | 3,4 | ~4,0 | ~0,88 | 1,7 | 0,35 |
| acetylén | 2,5 | 80,0 | 7,75 | 14,5 | 1,03 | 3,3 | 0,019 |
Tabuľka 8.12. Limity horľavosti plynov zmiešaných s kyslíkom (pri t = 20 ° C a p = 101,3 kPa)
Limity horľavosti pre bežné plyny v zmesi so vzduchom a kyslíkom sú uvedené v tabuľke. 11.08.-12.8 .. So zvyšovaním teploty zmesi sa limity horľavosti rozširujú a pri teplote presahujúcej teplotu samovznietenia horí zmes plynu so vzduchom alebo kyslíkom pri akomkoľvek objemovom pomere.
Limity horľavosti závisia nielen od druhov horľavých plynov, ale aj od podmienok experimentov (kapacita nádoby, tepelný výkon zdroja vznietenia, teplota zmesi, šírenie plameňa nahor, nadol, horizontálne atď.). Toto vysvetľuje mierne odlišné hodnoty týchto limitov v rôznych literárnych prameňoch. Na karte. 8.11 - 8.12 ukazuje relatívne spoľahlivé údaje získané pri izbovej teplote a atmosférickom tlaku, pričom plameň sa šíri zdola nahor v skúmavke s priemerom 50 mm a viac. Keď sa plameň šíri zhora nadol alebo horizontálne, spodná hranica sa mierne zvyšuje, zatiaľ čo horná sa znižuje. Limity horľavosti komplexných horľavých plynov, ktoré neobsahujú nečistoty zo záťaže, sa určujú podľa pravidla aditívnosti:
Lg = (r 1 + r 2 +… + r n) / (r 1 / l 1 + r 2 / l 2 +… + r n / l n) (8,17)
kde Lg - dolná alebo horná hranica horľavosti komplexného plynu v zmesi plyn-plyn alebo plyn-kyslík, približne. %; r 1, r 2, ..., r n - obsah jednotlivých zložiek v komplexnom plyne, obj. %; r 1 + r 2 + ... + r n = 100%; l 1, l 2, ..., l n - dolná alebo horná hranica horľavosti jednotlivých zložiek v zmesi plyn-vzduch alebo plyn-kyslík podľa tabuľky. 8.11 alebo 8.12, približne. %.
Ak sú v plyne nečistoty zo záťaže, limity horľavosti sa môžu určiť podľa vzorca:
Lb = Lg / (8,18)
kde L b - horná a dolná hranica horľavosti zmesi s prímesou prímesou, približne 0,10%,. %; Lg - horná a dolná hranica horľavosti horľavej zmesi približne. %; B - množstvo nečistôt zo štrku, frakcií jednotky.
Pri výpočtoch je často potrebné poznať koeficient prebytočného vzduchu α pre rôzne limity horľavosti (pozri tabuľku 8.11), ako aj tlak vyplývajúci z výbuchu zmesi plynu a vzduchu. Koeficient prebytku vzduchu zodpovedajúci horným alebo dolným limitom horľavosti sa môže určiť podľa vzorca
a = (100 / l - 1) (1 / VT) (8,19)
Tlak vznikajúci pri výbuchu zmesí plynu so vzduchom sa dá určiť pomocou dostatočnej aproximácie pomocou týchto vzorcov:
pre stechiometrický pomer jednoduchého plynu k vzduchu:
Rs = Pn (1 + βt k) (m / n) (8,20)
pre akýkoľvek pomer komplexného plynu k vzduchu:
Rs = Pn (1 + βt c) V vlaps / (1 + aV m) (8,21)
kde P VC - tlak vznikajúci pri výbuchu, MPa; p n - počiatočný tlak (pred explóziou), MPa; β je koeficient objemovej expanzie plynov, číselne rovný koeficientu tlaku (1/273); t K - kalorimetrická teplota horenia, ° C; m je počet mólov po výbuchu, určený reakciou spaľovania plynu vo vzduchu; n je počet mólov pred výbuchom pri spaľovacej reakcii; V Vlaps - objem produktov mokrého spaľovania na 1 m3 plynu, m 3; Vt - teoretický prietok vzduchu, m 3 / m 3.
Tabuľka 8.13. Tlak vznikajúci v dôsledku explózie zmesi propán-vzduch v závislosti od výpustného koeficientu k sat a typu ochranného zariadenia
| Typ bezpečnostného zariadenia | Resetovací faktor k sat, m2 / m3 | ||
|---|---|---|---|
| 0,063 | 0,033 | 0,019 | |
| Jedno duté zasklenie s vonkajším upevnením skla s hrúbkou 3 mm | 0,005 | 0,009 | 0,019 |
| Dvojité duté zasklenie s vonkajším upevnením skla s hrúbkou 3 mm | 0,007 | 0,015 | 0,029 |
| Krídlové krídlo s veľkým závesom a pružinovým uzáverom pre zaťaženie 5 MPa / m 2 | 0,002 | – | – |
| Výkyvné krídlo s horným závesom a pružinovým zámkom pre zaťaženie 5 MPa / m 2 | 0,003 | – | – |
| Voľne ležiace na bremene dosky, kg / m 2: | |||
| 0,023 | |||
| 0,005 | |||
| 0,018 | |||
Výbušný tlak uvedený v tabuľke 1. \\ T 8.13 alebo definované vzorcami, môže nastať len vtedy, ak je plyn v nádrži úplne spálený a jeho steny sú navrhnuté pre tieto tlaky. V opačnom prípade sú obmedzené silou stien alebo ich najľahšie sa rozpadávajúcimi časťami - tlakové impulzy sa šíria cez nehorľavý objem zmesi rýchlosťou zvuku a dosahujú plot oveľa rýchlejšie ako predný plameň.
Táto vlastnosť - rozdiel medzi rýchlosťou šírenia plameňa a tlakovými impulzmi (rázové vlny) - sa v praxi široko používa na ochranu plynových zariadení a priestorov pred zničením počas výbuchu. Za týmto účelom sa do otvorov stien a podláh ľahko inštaluje alebo otvára rám, rámy, panely, ventily atď. Tlak vznikajúci pri výbuchu závisí od konštrukčných vlastností ochranných zariadení a od koeficientu vybíjania k sat, čo je pomer plochy ochranných zariadení k objemu miestnosti.
8.6. SPUSTENIE V STILLOM MÉDIU
Pohyb zóny plameňa - čelo plameňa - oblasť, ktorá oddeľuje nezreagovanú horľavú zmes od produktov spaľovania, je spôsobená skutočnosťou, že studená horľavá zmes pred ňou sa zahrieva na teplotu vznietenia v dôsledku vedenia tepla a difúzie horúcich produktov horenia do studenej zmesi. Nazýva sa lineárna rýchlosť, ktorou sa predná časť plameňa pohybuje pozdĺž homogénnej horľavej zmesi rovnomerná rýchlosť plameňav závislosti od typu plynu a jeho obsahu v zmesi plyn-vzduch. Minimálna rýchlosť pre všetky typy horľavých plynov zodpovedá dolnému a hornému limitu zapálenia a maximu - pomeru plynov a vzduchu.
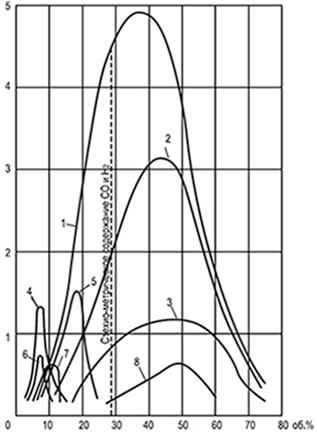
Obr. 8.1. Rovnomerné krivky rýchlosti
šírenie plameňa n n definované
v trubici s priemerom 25,4 mm
1 je vodík; 2-vodný plyn; Oxid uhoľnatý;
4-etylén; 5-koksárenský plyn; 6-etán; 7-metán;
8-generátorový plyn

Obr. 8.2. Vplyv priemeru d Tr a koncentrácie
metán zmiešaný so vzduchom pri zmene
rovnomerná rýchlosť plameňa u n
Experimenty zistili, že rýchlosť šírenia plameňa závisí od priemeru valcovej rúrky, cez ktorú sa šíri: čím väčší je priemer, tým vyššia je rýchlosť šírenia. Zvýšenie priemeru rúry redukuje účinok stien na proces spaľovania a predný pohyb plameňa a prispieva k zvýšenej konvekcii (Obr. 8.2). Z analýzy grafových údajov vyplýva, že pri veľmi malých veľkostiach trubíc je šírenie plameňa vo všeobecnosti nemožné (v dôsledku silného relatívneho chladiča). Rozmery rúrok, kanálov a štrbín, v ktorých sa plameň nerozšíri, sa nazývajú kritické.
Odlišujú sa pre rôzne plyny:
- studená zmes metánu so vzduchom - 3 mm;
- zmes vodík-vzduch - 0,9 mm;
- zahriata zmes metánu so vzduchom - 1,2 mm.
Fading v kanáloch malej časti sa v praxi používa na vytvorenie lapačov plameňa: siete na zadržiavanie plameňa, keramické porézne disky, disky z lisovaných kovových guľôčok, nádoby naplnené jemnozrnnými materiálmi atď.); požiarne kanály v konštrukcii horákov pracujúcich na zmesiach plyn-vzduch.
Pre porovnávacie charakteristiky horľavých vlastností plynov (bez ohľadu na veľkosť rúrok), pojem. \\ T "Normálna rýchlosť šírenia plameňa" - to je rýchlosť, ktorá sa vzťahuje na studenú (stále nehorľavú) zmes, s ktorou sa plameň pohybuje pozdĺž normálu k jeho povrchu. Predná časť plameňa sa považuje za plochú a rovnú priemeru rúry:
u n = w p πr 2 /S(8.22)
kde u n - normálna rýchlosť šírenia plameňa, m / s; w p - meraná rovnomerná rýchlosť plameňa, m / s; r je polomer rúry, m; S je povrchová plocha plameňa, m 2.
Tabuľka 8.14. Miera šírenia plameňa v rôznych zmesiach vzduchu a plynu (pri t = 20 ° C a p = 103,3 kPa), m / s
| plynový | Zmes s maximálnym normálom rýchlosť plameňa |
Stoichiometrická zmes | ||||
|---|---|---|---|---|---|---|
| Obsah v zmesi, asi. % | maximum normálne rýchlosť šíriť |
Obsah v zmesi, asi. % | normálne rýchlosť šíriť požiarne |
|||
| plyny | vzduchu | plyny | vzduchu | |||
| vodík | 42,0 | 58,0 | 2,67 | 29,5 | 70,5 | 1,6 |
| Oxid uhoľnatý | 43,0 | 57,0 | 0,42 | 29,5 | 70,5 | 0,30 |
| metán | 10,5 | 89,0 | 0,37 | 9,5 | 90,5 | 0,28 |
| etán | 6,3 | 93,7 | 0,40 | 5,7 | 94,3 | 0,32 |
| propán | 4,3 | 95,7 | 0,38 | 4,04 | 95,96 | 0,31 |
| n-bután | 3,3 | 96,7 | 0,37 | 3,14 | 96,86 | 0,30 |
| etylén | 7,0 | 93,0 | 0,63 | 6,5 | 93,5 | 0,5 |
| propylén | 4,8 | 95,2 | 0,44 | 4,5 | 95,5 | 0,37 |
| butylén | 3,7 | 96,3 | 0,43 | 3,4 | 96,6 | 0,38 |
| acetylén | 10,0 | 90,0 | 1,35 | 7,75 | 92,25 | 1,0 |
Ako je zrejmé z tabuľky údajov. 8.14, maximálna rýchlosť šírenia plameňa zodpovedá zmesiam plynu a vzduchu s nedostatkom oxidačného činidla (nie stechiometrického). S nadbytkom paliva zvyšuje účinnosť kolízie reagujúcich častíc a zvyšuje sa rýchlosť chemických reakcií.
Rýchlosť šírenia plameňa zmesí plynu a kyslíka je omnoho vyššia ako pri zmesiach plyn-vzduch. Maximálna normálna rýchlosť šírenia plameňa zmesi metánu a kyslíka je teda 3,3 m / s a zmes propánu a butánu s kyslíkom 3,5 - 3,6 m / s.
Maximálna normálna rýchlosť šírenia plameňa v zmesi komplexného plynu so vzduchom, m / s, je určená vzorcom: \\ t
u n max = (r 1 u 1 + r 2 u 2 +… + r n u n) / (r 1 + r 2 + ... + r n) (8,23)
kde r 1, r 2, ... r n - obsah jednotlivých zložiek v komplexnom plyne, obj. %; u 1, u 2, ... u n - maximálne normálne rýchlosti šírenia plameňa zložiek komplexného plynu zmiešaného so vzduchom, m / s.
Vyššie uvedené pomery sú vhodné pre plyny s blízkymi normálnymi rýchlosťami šírenia plameňa, napríklad pre prírodné a skvapalnené uhľovodíkové plyny. Pre zmesi plynov, ktoré majú výrazne odlišné rýchlosti šírenia plameňa (napríklad pre zmesi prírodných a umelých plynov, zmesi s vysokým obsahom vodíka), poskytujú len približné hodnoty.
Ak v zmesi existujú nečistoty nečistôt (dusík a oxid uhličitý), potom na približný výpočet rýchlosti šírenia plameňa použite vzorec: \\ t
u b = u n max (1 - 0,01 N 2 - 0,012С 2) (8.24)
Výrazne zvyšuje rýchlosť šírenia plameňa zahrievaním zmesi plyn-vzduch:
a „n = a n (T“ / T) (8,25)
kde a „n - rýchlosť šírenia plameňa vo vyhrievanej zmesi s absolútnou teplotou T“, K; a n - to isté, v studenej zmesi s teplotou T, K.
Predohriatie zmesi mení svoju hustotu nepriamo úmerne k absolútnej teplote, preto sa rýchlosť šírenia plameňa zvyšuje úmerne k tejto teplote. Táto skutočnosť sa musí brať do úvahy pri výpočtoch, najmä v tých prípadoch, keď sa vykurovacie kanály horákov nachádzajú vo vykurovanom murive alebo keď sú ovplyvnené žiarením ohniska, horúcich plynov atď.
Rovnomerné šírenie plameňa je možné, ak sú splnené nasledujúce podmienky:
- požiarna trubica má malú dĺžku;
- spaľovanie sa šíri pri konštantnom tlaku blízkom atmosférickému.
Ak je dĺžka trubice významná, potom sa môže aj šírenie plameňa pre niektoré zmesi premeniť na vibrácie a potom na detonáciu s nadzvukovou rýchlosťou horenia (2000 m / s a viac), keď sa zmes zapáli v dôsledku rázovej vlny zahrievajúcej zmes na teploty prekročenie teploty samovznietenia. K výbuchu dochádza v zmesiach s vysokou mierou šírenia plameňa. Limity koncentrácie detonácie sú už v medziach horľavosti zmesí plyn-vzduch a plyn-kyslík, obj. %: propán - 3.2 - 37, izobután - 2.8 - 31, vodík - 15 - 90. Tlak vznikajúci počas detonačného spaľovania môže prekročiť počiatočnú hodnotu desaťnásobku a viesť k zničeniu rúrok a iných nádob navrhnutých pre vysoké tlaky.
8.7. SPUSTENIE V LAMINÁRE A TURBULENTOVÝCH STREAMOCH

Obr. 8.3. Predné horenie
zmes plynov a vzduchu v
laminárny režim jazdy
Čelo plameňa môže byť zastavené, ak vytvoríte protipohyb horľavej zmesi rýchlosťou rovnajúcou sa normálnej rýchlosti šírenia plameňa. Dobrým príkladom je povrch vnútorného kužeľa horáka Bunsen. Reguláciou zloženia zmesi plynu a vzduchu, prúdiacej z horáka v laminárnom režime pohybu, je možné dosiahnuť vzhľad stabilného a ostro ohraničeného horiaceho kužeľa (obr. 8.3). Bočný povrch kužeľa (čelo plameňa), fixovaný vzhľadom na vypaľovaciu hranu kanála horáka, sa pohybuje smerom k odchádzajúcej zmesi plynu a vzduchu a v tomto prípade sa plameň šíri normálne na povrch zapálenia v každom bode. Rovnosť rýchlostí je zachovaná na povrchu čela kužeľového plameňa - priemery prietoku zmesi plyn-vzduch s normálnou hodnotou w ku generatrix kužeľa a normálnej rýchlosti šírenia plameňa u n sa riadia Michelsonovým zákonom:
w n = w pot cosφ = u n (8.26)
kde φ je uhol medzi smerom prúdenia a normálom k povrchu prednej časti kužeľového plameňa; w pot je priemerná rýchlosť prúdenia zmesi plyn-vzduch prechádzajúca horákom za jednotku času, m / s.
Konštanta normálnej rýchlosti šírenia plameňa je platná len pre hlavnú časť bočného povrchu čela kužeľového plameňa. Na vrchole kužeľa sa rýchlosť zvyšuje v dôsledku zahrievania zmesi plynu a vzduchu úzko rozmiestnenými časťami kužeľového povrchu čela plameňa a na dne kužeľa sa znižuje v dôsledku chladiaceho účinku koncovej časti požiarneho kanálu horáka.
Pre praktické výpočty sa tento rozdiel zvyčajne zanedbáva a zmes prechádzajúca cez čelo plameňa sa považuje za konštantnú na celom povrchu kužeľa a rovná sa n.
Priemerná normálna rýchlosť šírenia plameňa je
u n = V cm / S (8,27)
kde V cm je objem zmesi plynu a vzduchu prechádzajúcej horákom, S je plocha prednej časti kužeľového plameňa.
V praxi nemá čelo kužeľového plameňa pravidelný geometrický tvar, preto, aby sa presne určilo S, plameň je fotografovaný, čelo plameňa je rozdelené na sériu zrezaných kužeľov. Súčet bočných povrchov je celkový povrch prednej časti kužeľového plameňa. Hodnoty normálnych rýchlostí šírenia plameňa, stanovené metódou Bunsenovho horáka a inými metódami, sú rovnaké a rovnajú sa normálnym rýchlostiam uvedeným v tabuľke 1. \\ T 8.14.
Výška čela kónického plameňa závisí hlavne od veľkosti vypaľovacieho kanála horáka. Zníženie výšky plameňa možno dosiahnuť rozdrvením veľkých požiarnych kanálov na niekoľko menších. V prípade zmesí plyn-vzduch rovnakého zloženia sa výška kužeľových frontov plameňa malých kanálov h môže určiť približne z výšky čela plameňa jedného kanála H:
h = H / √n (8,28)
kde n je počet malých kanálov.
Pri horákoch s vysokým tepelným výkonom (horáky priemyselných kotlov, pecí atď.) Sa spaľovanie zvyčajne uskutočňuje v turbulentnom prúde - hladký kužeľový plameň v dôsledku vírivého pohybu a pulzácií eroduje a stráca jasné kužeľové obrysy. V tomto prípade sa pozorujú dva charakteristické typy spaľovania, ktoré zodpovedajú malej rozsiahlej turbulencii.
S turbulentnými váhami, ktoré neprekračujú hrúbku laminárnej spaľovacej zóny, si predná časť kónického plameňa zachováva svoj tvar a zostáva hladká, aj keď sa horiaca zóna zvyšuje. Ak stupnica turbulencie prevyšuje hrúbku zóny normálneho spaľovania, povrch čela kužeľového plameňa sa stáva nerovnomerným. To vedie k zvýšeniu celkového povrchu prednej časti spaľovania a spaľovaniu väčšieho množstva horľavej zmesi na jednotku prierezu prúdu.
Pri turbulencii vo veľkom merítku, ktorá výrazne prekračuje hrúbku laminárneho spaľovacieho pásma, vedie vzrušenie prednej plochy plameňa k oddeleniu jednotlivých častíc horúcej zmesi, ktoré sú rozdrvené následnými pulzáciami. Čelo plameňa stráca svoju integritu a mení sa na systém jednotlivých spaľovacích centier vo forme rovnomerného rozdeľovania a spaľovania v prúde častíc horľavej zmesi.

Obr. 8.4. Relatívna zmena rýchlosti
šírenie plameňa koksového plynu
zmiešané so vzduchom v závislosti od čísla
Reynolds a Mix Motion Mode
Pri veľkých turbulenciách vzrastá čelný povrch plameňa, ktorý sa skladá z plôch všetkých horiacich častíc, čo vedie k prudkému nárastu rýchlosti šírenia plameňa (obr. 8.4). V tomto prípade sa môže vyskytnúť nielen predné spaľovanie, ktoré sa šíri normálnou rýchlosťou vn, ale aj objem, ku ktorému dochádza v dôsledku turbulentných pulzácií zahrievaných produktov spaľovania do čerstvej zmesi. V dôsledku toho je celková rýchlosť šírenia plameňa počas turbulencie vo veľkom meradle určená jednou alebo druhou kombináciou predných a objemových spaľovacích prvkov.
Pri neprítomnosti pulzácií sa rýchlosť turbulentného horenia rovná normálnej rýchlosti šírenia plameňa. Naopak, ak pulzačná rýchlosť výrazne prevyšuje normálnu, rýchlosť turbulentného horenia je málo závislá od fyzikálno-chemických vlastností horľavej zmesi. Experimenty ukázali nízku závislosť rýchlosti spaľovania rôznych homogénnych zmesí plyn-vzduch s a\u003e 1 v priemyselných peciach na normálnej rýchlosti šírenia plameňa.
8.8. STABILITA POISTENIA

Obr. 8.5. Systém priamej kompenzácie
u n = w potenie s laminárnym pohybom
zmes plyn-vzduch
1 - stena horáka;
2 - predný plameň
Hlavné faktory ovplyvňujúce stabilitu spaľovania - rýchlosť prúdenia zmesi plynu a vzduchu a šírenie plameňa. Pri spaľovaní zmesí plyn-vzduch v laminárnom prúde je jeho stálou časťou prednej časti kónický plameň. V tomto bode je čelo plameňa v dôsledku expanzie zmesi plynu a vzduchu, prúdiacej do atmosféry a spomaľujúceho pôsobenia steny kanála, otočené do vodorovnej polohy a zvýšené nad okrajom kanála o hrúbku čela plameňa (obr. 8.5).
Na tejto časti prednej časti je úplná kompenzácia rýchlosti prúdenia plynu a vzduchu rýchlosťou šírenia plameňa u n = w pers. Na zvyšku kužeľovej časti čela plameňa je kompenzácia čiastočná a vykonáva sa len v smere kolmom na čelo spaľovania: u n = w je pot potu. Súčiastka zostane nevyvážená a vytiahne bod vzplanutia od základne kužeľa k jeho vrchu. Stabilita čela kužeľového plameňa je vysvetlená skutočnosťou, že prstencový pás v základni slúži ako zdroj zapálenia, bez ktorého by bol zvyšok prednej časti demolovaný prúdom zmesi plynu a vzduchu.
Ak prietoková rýchlosť zmesi prekročí rýchlosť šírenia plameňa, šírka zapaľovacieho pásu sa zmenší, až kým sa nezmení. V tomto prípade sa zlomí čelo plameňa a dôjde k oddeleniu od horáka. Ak rýchlosť šírenia plameňa v oblasti prstencovej steny (nie na stene) prekročí rýchlosť prúdenia zmesi plynu a vzduchu, plameň sa ťahá vnútri miešača horákov (prekmit).
S pozorovaným odtrhnutím:
- prerušenie plameňa z horáka a jeho zánik;
- oddelenie od okraja vypaľovacieho kanála, keď plameň dosiahne novú, pomerne stabilnú polohu v prúde nad horákom;
- narušenie zvýšeného plameňa a jeho zánik;
- horák na odpadky zvýšený na okraj kanála na vypaľovanie horáka;
- vytvorením zaveseného plameňa, keď je prúd zapálený v určitej vzdialenosti od horáka.
Všetky tieto javy sú neprijateľné, pretože vedú k akumulácii v okolitej atmosfére alebo v ohnisku nespáleného plynu.

Obr. 8.6. Závislosť rýchlosti jednotlivca
plameň v otvorenej atmosfére zmesí prírodného
plyn so vzduchom na veľkosti požiarneho kanála a
obsah primárneho vzduchu.

Obr. 8.7. Závislosť rýchlosti oddeľovania
plameň v otvorenej atmosfére
zmesi zemného plynu s veľkosťou vzduchu
požiarny kanál a obsah primárneho vzduchu.
a - diagram horáka; b - krivky prerušenia plameňa
Na obr. 8.6 sú znázornené experimentálne krivky oddeľovania plameňa od okrajov vypaľovacích kanálov horákov s jedným horákom pracujúcich na zmesi studeného plynu so vzduchom. Na hranici a nad krivkami sa plameň rozpadá a pod krivkami - stále horenie.
V praxi sú široko rozšírené viacvláknové vstrekovacie horáky s požiarnymi kanálmi s priemerom 2-6 mm (Obr. 8.7). Stanovenie rýchlosti vypaľovania w pre takéto horáky sa môže vykonať podľa nasledujúceho vzorca: \\ t
w ref = 3,510 -3 dk T2 (1 + Vt) / (1 + a 1 Vt) (8,29)
kde d k - priemer požiarnych kanálov, m; α 1 - koeficient prebytku primárneho vzduchu; T je absolútna teplota zmesi plynu a vzduchu, K.
Podľa vzorca je zrejmé, že stabilita spaľovania sa zvyšuje so zvyšujúcimi sa priemermi požiarnych kanálov a teplotou a znižuje sa so zvyšujúcim sa koeficientom prebytku primárneho vzduchu. Stabilitu horenia zvyšuje aj vzájomný vplyv plameňa.
Oddelenie plameňa od požiarnych kanálov môže nastať z iných dôvodov. Ak sú horák a výfukové kanály spaľovacieho plynu v nesprávnej polohe, môžu sa dostať do injektora horáka a spôsobiť, že sa plameň odtrhne (znížením rýchlosti šírenia plameňa v zmesi plynu a vzduchu zriedenej inertnými plynmi). Príčinou separácie môže byť aj vysoká rýchlosť sekundárneho vzduchu, ktorý plameň vyfukuje z vypaľovacích kanálov.
Tabuľka 8.15. Rýchlosť homogénnej zmesi prírodných
plyn so vzduchom, pri ktorom dochádza k prelomeniu
plameň, m / s (teplota zmesi 20 ° C)
| priemery požiarne kanály |
Prebytok primárneho vzduchu | |||||
|---|---|---|---|---|---|---|
| 0,6 | 0,7 | 0,8 | 0,9 | 1,0 | 1,1 | |
| 3,5 | 0,05 | 0,10 | 0,18 | 0,22 | 0,23 | 0,21 |
| 4,0 | 0,08 | 0,12 | 0,22 | 0,25 | 0,26 | 0,20 |
| 5,0 | 0,09 | 0,16 | 0,27 | 0,31 | 0,31 | 2,23 |
| 6,0 | 0,11 | 0,18 | 0,32 | 0,38 | 0,39 | 0,26 |
| 7,0 | 0,13 | 0,22 | 0,38 | 0,44 | 0,45 | 0,30 |
| 8,0 | 0,15 | 0,25 | 0,43 | 0,50 | 0,52 | 0,35 |
| 9,0 | 0,17 | 0,28 | 0,48 | 0,57 | 0,58 | 0,39 |
| 10,0 | 0,20 | 0,30 | 0,54 | 0,64 | 0,65 | 0,43 |
Plameň sa vháňa do horáka, zvyčajne sprevádzaný bavlnou, je tiež neprijateľný. Prielom vedie buď k zániku plameňa a uvoľneniu nespálenej zmesi do miestnosti alebo pece, alebo k horeniu zmesi v horáku. Tendencia plameňa k prelomeniu závisí od typu plynu, normálnej rýchlosti šírenia plameňa, obsahu primárneho vzduchu v zmesi plynu a vzduchu, veľkosti vypaľovacích kanálov, teploty zmesi alebo stien kanálov. Koeficient tepelnej vodivosti materiálov, z ktorých sú vypaľovacie kanály zhotovené, ich tvar, hĺbka a kvalita výroby, prítomnosť otrepov, zlomov hrán, atď. Majú tiež vplyv na prelomenie plameňa.
V tabuľke. 8.15 Rýchlosti homogénnych zmesí prírodných plynov so vzduchom, pri ktorých dochádza k prieniku, sa môžu použiť aj pre iné plyny, pričom sa zohľadňujú zmeny a doplnenia: \\ t
w "pr = w pr u" n / u n (8.30)
kde w 'je rýchlosť prieniku plameňa pre iný plyn, m / s; w ol - miera prelomenia zemného plynu (tabuľka 8.15), m / s; u 'n - normálna rýchlosť šírenia plameňa pre iný plyn, m / s; u n - rýchlosť šírenia plameňa v metáne, m / s.
Maximálnu rýchlosť prielomu možno vypočítať pomocou približného vzorca:
w ol = 0,73 10 -3 d k T 2 (8,31)
Rovnaký vzorec s dostatočnou aproximáciou pre prax môže byť použitý pre iné plyny so zavedením zmeny a doplnenia zmeny normálnej rýchlosti šírenia plameňa. Na základe mnohých experimentov je možné vyvodiť nasledujúci záver: limity ustálenej prevádzky horákov sú obmedzené rýchlosťou separácie a prelomom plameňa.

Obr. 8.8. Závislosť rýchlosti zmesi plynu a vzduchu, pri ktorej dochádza k separácii a úniku plameňa, na koeficient prebytku primárneho vzduchu
I - oddelenie plameňa; II - prielom plameňa; III - žlté okraje plameňa;
1-3 priemery požiarnych kanálov horákov, mm: 1 - 25, 2 - 25, 3 - 32
Na obr. 8.8 znázorňuje krivky, ktoré charakterizujú prietokovú rýchlosť zmesi zemného plynu so vzduchom, pri ktorom sa plameň rozbije a presakuje. Povaha kriviek ukazuje prudký pokles stability plameňa so zvyšujúcim sa obsahom zmesi primárneho vzduchu. K zvýšeniu stability plameňa dochádza pri poklese obsahu primárneho vzduchu a dosahuje maximum, keď klesá na nulu (difúzne horenie). Takéto spaľovanie uhľovodíkových plynov je však v mnohých prípadoch neprijateľné, pretože vedie k vzniku žltých klapiek, ktoré charakterizujú výskyt častíc sadzí v ňom.

Obr. 8.9. Bežné stabilizátory spaľovania
- valcový tunel s náhlym zväčšením prierezu;
b - rovnaké s vírivým prúdením;
c) kužeľovitý tunel s vírivým prúdením;
g - stabilizátor vo forme kužeľového telesa;
d - to isté, vo forme kruhovej tyče;
e - to isté, vo forme pevného prstencového plameňa
1 - trysky horákov; 2 - tunel; 3 - bočný otvor;
4 - prstencový kanál; 5 - plameň krúžku;
6 - plameň hlavného prúdu zmesi plyn-vzduch
V praxi, na rozšírenie rozsahu stability spaľovania všetkých horľavých zmesí plyn-vzduch, je prietoková rýchlosť braná niekoľkokrát väčšia ako separačná rýchlosť. Zabránenie oddeľovaniu plameňa sa dosahuje pomocou stabilizátorov spaľovania (Obr. 8.9).
Aby sa stabilizoval plameň vstrekovania a iné horáky, ktoré produkujú axiálne symetrické prúdy plynu a vzduchu, používajú sa žiaruvzdorné valcové tunely s náhlym rozšírením ich prierezu. Pôsobenie takéhoto tunela je založené na obvodovej cirkulácii časti produktov horúceho spaľovania, ktoré vznikajú v dôsledku zriedenia vytvoreného prúdom.
Na stabilizáciu plameňa horákov, vydávajúcich vírivú zmes plynu a vzduchu, sa používajú valcové aj kužeľovité tunely s uhlom otvárania 30–60 °. Pri vírivom prúdení vzniká väčší tlak na obvode tunela ako v jeho strednej časti. To vedie k axiálnej recirkulácii časti horúcich produktov horenia a zapáleniu studenej zmesi plyn-vzduch prúdiacej do tunela zvnútra.
Keď nie je možná inštalácia tunelov, na stabilizáciu plameňa sa používajú telesá s nedostatočným prúdením, ktoré sú umiestnené v prúde zmesi plynu a vzduchu na výstupe z plameňa z požiarneho kanála horáka. Zapálenie zmesi súčasne nastáva na obvode stabilizátora, po ktorom dochádza k čiastočnej recirkulácii horúcich plynov, ktoré zapaľujú horľavú zmes zvnútra. Stabilizačný účinok takýchto zariadení je nižší ako tunely.
Stabilizátory spaľovania vo forme špeciálnej požiarnej trysky sú široko používané vo vstrekovacích jednohorových horákoch. Stabilizačný účinok tohto zariadenia je založený na zabránení zriedenia hlavného prúdu v koreňoch horáka prebytočným vzduchom, ktorý obmedzuje jeho stabilitu, ako aj na zahrievanie a zapálenie hlavného prúdu prstencovým plameňom po celom jeho obvode. Stabilita prstencového plameňa pri oddeľovaní sa dosahuje v dôsledku pomeru prierezov požiarneho prstenca a bočných otvorov, v ktorom rýchlosť zmesi plynu a vzduchu v prstencovej dutine neprekračuje normálnu rýchlosť šírenia plameňa. Aby sa zabránilo prenikaniu plameňa do miešača horáka, predpokladá sa, že rozmery bočných otvorov, ktoré tvoria prstencový plameň, sú menej kritické.
8.9. POŽIARNE OKRUHY
Vzduch alebo kyslík, raz v plynovode, môže tvoriť výbušnú zmes, takže je nevyhnutné chrániť potrubia pred vniknutím vzduchu alebo kyslíka do neho. Vo všetkých zariadeniach na výrobu výbušnín by sa mali vytvoriť podmienky na vylúčenie možnosti vznietenia impulzov. Zdroje zapálenia, ktoré vedú k zmesi plynu a vzduchu k výbuchu, sú:
- otvorený plameň;
- elektrické výboje existujúcich elektrických zariadení;
- skrat v elektrických vodičoch;
- iskry v elektrických spotrebičoch;
- otvorené poistky;
- statické výboje.
Bezpečnosť proti výbuchu zabezpečujú rôzne poistky. inštalované v potrubiach, na nádržiach, na čistiacich potrubiach, sviečkach a iných systémoch, kde hrozí nebezpečenstvo výbuchu.
K zhášaniu plameňa v kanáli naplnenom horľavou zmesou dochádza len s minimálnym priemerom kanála, v závislosti od chemického zloženia a tlaku zmesi, a vysvetľuje sa tepelnými stratami z reakčnej zóny na steny kanála. Keď sa priemer kanála znižuje, jeho povrch sa zvyšuje na jednotku hmotnosti reakčnej zmesi, t.j. zvýšenie tepelných strát. Keď dosiahnu kritickú hodnotu, rýchlosť spaľovacej reakcie klesá natoľko, že ďalšie šírenie plameňa je nemožné.
Schopnosť spomaľovača horenia spomaľovača plameňa závisí najmä od priemeru kaliacich kanálov a oveľa menej na ich dĺžke a možnosť prenikania plameňa cez kaliace kanály závisí najmä od vlastností a zloženia horľavej zmesi a tlaku. Normálna rýchlosť šírenia plameňa je základná veličina, ktorá určuje veľkosť hasiacich kanálov a výber typu poistky plameňa: čím väčšia je, tým menšia je veľkosť kanála na hasenie plameňa. Rozmery kaliacich kanálov tiež závisia od počiatočného tlaku horľavej zmesi. Na posúdenie schopnosti spomaľovačov horenia použitých poistiek plameňa tzv. Kritérium Re:
Fe = w cm dc p p / (RT 0 λ 0) (8,32)
V limite zániku plameňa má Pecletovo kritérium formu:
Pe cr = w cm d cr c p p cr / (RT 0 λ 0) (8,33)
kde w cm je normálna rýchlosť šírenia plameňa; d je priemer kaliaceho kanála; d кr - kritický priemer kaliaceho kanála; с - špecifická tepelná kapacita plynu pri 0 ° С a konštantný tlak; p je tlak plynu; p - kritický tlak plynu; R je univerzálna plynová konštanta; T 0 - absolútna teplota plynu; λ 0 - tepelná vodivosť pôvodnej zmesi.
Na výpočet schopnosti retardérov horenia spomaľovačov plameňa sú potrebné nasledujúce počiatočné údaje:
- normálne rýchlosti šírenia horľavých zmesí plynov;
- skutočná veľkosť maximálnych kaliacich kanálov daného lapača plameňa.
Ak je získaná hodnota väčšia ako Pecr = 65, poistka proti plameňu neodloží šírenie plameňa tejto horľavej zmesi a naopak, ak Pe< 65, огнепреградитель задержит распространение пламени. Запас надежности огнепреградителя, который находят из отношения Ре кр к вычисленному значению Ре, должен составлять не менее 2:
P = Pe cr / Re = 65 / Fe\u003e 2,0 (8,34)
Pomocou skutočnosti konštantnosti Dcr pri limite extinkcie plameňa je možné vypočítať približný kritický priemer kanálov pre každú horľavú zmes, ak je známa rýchlosť šírenia plameňa, ako aj tepelná kapacita a tepelná vodivosť plynového systému. Odporúčajú sa tieto kritické priemery kaliaceho kanála, mm:
- spaľovaním zmesi plyn - vzduch - 2,9 pre metán a 2,2 pre propán a etán;
- pri spaľovaní zmesí kyslíka v potrubí (pri absolútnom tlaku 0,1 MPa za podmienok voľnej expanzie produktov spaľovania) - 1,66 pre metán a 0,39 pre propán a etán.

Obr. 8.10. Typy lapačov plameňa:
- tryska; b - kazeta; in - lamelárny; g - ok; d - kov-keramika
Štrukturálne sú zvodiče rozdelené do štyroch typov (obr. 8.10):
- s dýzou granulovaných materiálov;
- s priamymi kanálmi;
- z kovovej keramiky alebo kovových vlákien;
- net.
Podľa spôsobu inštalácie - do troch typov: na potrubiach na emisie plynov do atmosféry alebo na erupciu; o komunikáciách; pred zariadeniami na spaľovanie plynu.
V prípade zabaleného lapača plameňa medzi mriežkami je tryska s výplňou (sklenené alebo porcelánové guľôčky, štrk, korund a iné granule z odolného materiálu). Kazetový lapač plameňa je prípad, v ktorom je ohňovzdorná kazeta inštalovaná z vlnitých a plochých kovových pások, pevne skrútených do kotúča. V prípade lapača plameňových plameňov je k dispozícii balík rovinne rovnobežných kovových dosiek s presne definovanou vzdialenosťou medzi nimi. U lapača plameňa v puzdre je umiestnený balík pevne stlačených kovových mriežok. Zachycovač cermetového plameňa je puzdro, v ktorom je umiestnená porézna cermetová doska vo forme plochého kotúča alebo rúrky.
Najčastejšie sa používajú sieťové požiarne zvodiče (začali sa inštalovať už začiatkom 19. storočia v baníckych lampách (Deviho lampy), aby sa zabránilo výbuchom banského plynu). Tieto lapače plameňa sa odporúčajú na ochranu zariadení, ktoré spaľujú plynné palivo. Protipožiarny prvok pozostáva z niekoľkých vrstiev mosadzného drôteného pletiva s veľkosťou ôk 0,25 mm, vložených medzi dve perforované dosky. Balenie sieťoviny vystužené v odnímateľnom držiaku.
Teleso lapača plameňa je vyrobené zo zliatiny liatiny alebo hliníka a pozostáva z dvoch identických častí spojených skrutkami s odnímateľným držiakom umiestneným medzi nimi. Okrem uvažovaných suchých lapačov plameňa sú ventily na zaistenie kvapalín široko používané na ochranu plynovodov pred vniknutím vlny a plameňa počas spracovania plameňom plameňom kovov, ako aj potrubí a prístrojov naplnených plynom z prenikania kyslíka a vzduchu do nich.
Kvapalné ventily musia:
- aby sa zabránilo šíreniu vlny pri spätných otrasoch a pri vznietení plynov;
- chrániť potrubie pred kyslíkom a vzduchom;
- poskytujú minimálny hydraulický odpor prietoku plynu. Okrem toho by sa kvapalina z brány nemala odoberať vo forme kvapiek v značných množstvách.
8.10. PRINCÍPY HORENIA
Procesy spaľovania plynu sú založené na princípoch, konvenčne nazývaných kinetika a difúzia. Pokiaľ ide o princíp, pred začiatkom spaľovania vzniká rovnomerná zmes s určitým prebytkom vzduchu. Spaľovanie takejto zmesi sa uskutočňuje v krátkom transparentnom horáku bez tvorby častíc sadzí v plameni. Pri spaľovaní plynu podľa kinetického princípu sa na prípravu homogénnej zmesi plynu a vzduchu s prebytkovým koeficientom primárneho vzduchu α 1 = 1,02: 1,05 používajú špeciálne miešače alebo injektážne horáky.
Pri nižšom obsahu primárneho vzduchu, podľa kinetického princípu, prebieha len počiatočná fáza spaľovania, až do použitia kyslíka v zmesi s plynom. Zvyšné plyny a produkty neúplného spaľovania sa spaľujú v dôsledku vonkajšej difúzie kyslíka (sekundárneho vzduchu), t.j. na d a ff pri z a okolo n okolo m na princípe. Pri α1< 1 у факела есть два видимых фронта горения: внутренний, возникающий за счет первичного воздуха, и наружный, образующийся за счет диффузии кислорода из окружающей среды. Общая высота пламени при таком горении возрастает, а температура - несколько снижается. Устойчивость пламени и его прозрачность зависят от содержания первичного воздуха в смеси: чем оно выше, тем ниже устойчивость пламени, больше его прозрачность, и наоборот.
Princíp horenia plynu s α 1< 1,0 является п р о м е ж у т о ч н ы м (между кинетическим и диффузионным). С учетом этого принципа конструируются все газовые аппараты с инжекционными горелками. В таких горелках содержание первичного воздуха в смеси принимается в зависимости от вида газа таким, чтобы:
- v plameni neboli žiadne čiastočky sadzí;
- zabezpečila stabilitu spaľovania so zmenami tepelného výkonu v akýchkoľvek limitoch potrebných v praxi.
Pri princípe difúzie (α 1 = 0) sa paralelne vyvíjajú procesy spaľovania a miešania. Pretože procesy miešania prebiehajú oveľa pomalšie ako procesy spaľovania, rýchlosť a úplnosť spaľovania sú určené rýchlosťou a úplnosťou miešania plynu a vzduchu. V tomto prípade môže byť plyn zmiešaný so vzduchom difúziou (buď pomalá molekulárna alebo turbulentná, vrátane molekulárneho ako posledný stupeň). Rýchlosť horenia a štruktúra difúzneho plameňa sa teda líšia.
Vlastnosti tohto vypaľovania:
- stabilita plameňa so zmenou tepelného výkonu z nuly na maximum podľa podmienok oddelenia;
- stálosť teplôt v celej výške plameňa;
- možnosť jeho distribúcie na veľké ľubovoľné povrchy;
- kompaktné horáky a jednoduchosť výroby;
- významná výška plameňa a nevyhnutnosť pyrolytických procesov vedúcich k vytvoreniu jasného plameňového plameňa.

Obr. 8.11. Štruktúra voľných plameňov:
a - laminárny plameň; b - turbulentný plameň
Difúzne horenie sa môže preniesť na kinetiku alebo medziprodukt, ak je zmes pred procesmi spaľovania. V praxi sa to dá dosiahnuť núteným prívodom vzduchu, čo vedie k vytvoreniu kvázi homogénnej zmesi plynu a vzduchu s a\u003e 1,0, ktorá horí v priehľadnom horáku.
Na ilustráciu princípov horenia na obr. 8.11. sú uvedené schémy volných horákov: laminárne a turbulentné. Laminárny horák vzniká v dôsledku vzájomnej molekulárnej difúzie plynu a vzduchu. Vo vnútri kužeľového jadra 1 je čistý plyn prúdiaci z trubice v režime laminárneho prúdenia. V zóne 2 - zmes plynu a produktov spaľovania, v zóne 3 - zmes produktov spaľovania a vzduchu. Hranica 4 je hladká kužeľová plameňová čelo, na ktoré molekuly vzduchu difundujú zvonku a molekuly plynu zvnútra. Produkty spaľovania čiastočne difundujú do plynu a intenzívne ho ohrievajú v zóne pred plameňom. To vedie k pyrolýze uhľovodíkov a tvorbe častíc sadzí, čo dáva plameň jasnú svietivosť.
Intenzifikácia spaľovania je možná v dôsledku turbulencie zmiešaných tokov. Turbulentný horák nemá čelo kónického spaľovania, je „rozmazaný“ a rozdrobený pulzáciami na oddelené častice.
Štruktúra plameňa pozostáva z čistého plynového jadra 1, relatívne pomalej zóny 2 horenia, difúznej zóny s najintenzívnejším horením 3 s vysokým obsahom produktov horenia a zóny 4 horenia s prevládajúcim vzduchom. Medzi zónami nie sú jasne definované hranice, ktoré sa plynule posúvajú v závislosti od stupňa turbulencie prietoku. Charakteristiky turbulentného horáka sú:
- proces horenia takmer v celom objeme;
- zvýšenie intenzity spaľovania;
- väčšia transparentnosť plameňa;
- jeho menšia stabilita vzhľadom na separáciu.
Turbulentné spaľovanie plynu je široko používané v peciach rôznych kotlov a pecí. Na zintenzívnenie procesu spaľovania sa používajú ako prirodzené (v dôsledku zvýšených rýchlostí), tak aj umelá turbulencia prúdov, napríklad otáčaním prúdenia vzduchu a privádzaním tenkých plynových prúdov do rôznych uhlov.
8.11. PODMIENKY TÝKAJÚCE SA FORMÁCIE VÝROBKOV NEPLATNÉHO SPOROVANIA A ZNÍŽENIA V TÝCHTO KONCENTRÁCII ZDRAVOTNÝCH LÁTOK \\ t
Keď sa spaľujú horľavé plyny, produkty spaľovania môžu obsahovať zložky ako úplné (oxid uhličitý a vodná para), tak aj neúplné spaľovanie (oxid uhoľnatý, vodík, nenasýtené, nasýtené, aromatické uhľovodíky a sadze). Okrem toho sa v produktoch spaľovania vždy nachádzajú oxidy dusíka. Prítomnosť produktov nedokonalého spaľovania vo významných koncentráciách je neprijateľná, pretože vedie k znečisteniu ovzdušia toxickými látkami a k zníženiu účinnosti zariadení poháňaných plynom.
Hlavné dôvody ich vysokého obsahu:
- spaliny s nedostatočným vzduchom;
- slabé miešanie horľavých plynov a vzduchu pred a počas procesu spaľovania;
- nadmerné ochladzovanie plameňa na dokončenie spaľovacích reakcií.
Pre metán môžu byť reakcie horenia (v závislosti od koncentrácie kyslíka v reakčnej zmesi) opísané nasledujúcimi rovnicami:
CH4 + 2O2 = C02 + 2H20 + 800,9 MJ / mol
keď stechiometrický pomer alebo nadbytok oxidantu;
CH4 + 02 = CO + H2 + H20 + Q a CH4 + 0,5O2 = CO + 2H20 + Q
s nedostatkom oxidačného činidla.

Obr. 8.12. Produkty stredného spaľovania

Obr. 8.13. Obsah primárneho vzduchu
zabraňuje tvorbe
žlté jazyky v plameňoch
Plyn: 1 - koks;
2 - polia zemného plynu;
3 - ropné polia;
4 - propán; 5 - bután
Na obr. 8.12 ukazuje približné priemerné zloženie niektorých medziproduktov - vodíka, oxidu uhoľnatého, etylénu, acetylénu a relatívne malého počtu nasýtených a najjednoduchších aromatických zlúčenín - a oxidu uhličitého produkovaného v plameni počas difúzneho spaľovania zemného plynu (97%). Plyn bol spaľovaný v laminárnom oblaku, plyn prúdil z rúrky s priemerom 12 mm. Celková výška plameňa je 130 - 140 mm.
Maximálna koncentrácia vodíka a acetylénu je dosiahnutá približne v rovnakej výške plameňa, miznú takmer súčasne na vrchole svetelnej zóny plameňa. Zo všetkých medziproduktov vytvorených v plameni (okrem sadzových častíc), oxid uhoľnatý zmizne. To dáva dôvod posúdiť podľa svojho indexu úplnosť spaľovania plynu. Oxidy dusíka sú vždy prítomné v produktoch spaľovania, ktorých maximálna koncentrácia sa vyskytuje v zónach intenzívneho spaľovania oxidu uhoľnatého a vodíka.
Spaľovanie uhľovodíkových plynov s nedostatkom oxidačného činidla vedie k tvorbe sadzových častíc, ktoré dávajú plameň žltú farbu. Proces spaľovania sadzí prebieha postupne a relatívne pomaly. Niekedy sa spaľovanie vytvorených sadzových častíc oneskoruje a môže úplne zaniknúť pri vstupe do nízkoteplotnej oblasti horáka alebo keď sa povrchy výmenníka tepla umyjú plameňom. Prítomnosť žiariaceho plameňa teda vždy indikuje výskyt pyrolytických procesov a možnosť chemického neúplného spaľovania, najmä v malých tienených kotlových peciach.
Prevencia tvorby sadzových častíc sa dosahuje predzmiešaním uhľovodíkových plynov s dostatočným množstvom oxidačného činidla. Obsah primárneho vzduchu v zmesi, v ktorej dochádza k priehľadnému plameňu, závisí nielen od typu uhľovodíkov, ale aj od podmienok miešania so sekundárnym vzduchom (priemer vypaľovacích kanálov horákov) (Obr. 8.13). Na hraniciach a nad krivkami je plameň transparentný a pod krivkami má žlté jazýčky. Krivky ukazujú, že obsah primárneho vzduchu v zmesi sa zvyšuje so zvyšovaním počtu atómov uhlíka v molekule a priemeru vypaľovacích kanálov horákov. Pre malé požiarne kanály horákov možno určiť koeficient prebytku primárneho vzduchu α 1 v zmesi, v ktorej zmiznú žlté plamene v závislosti od špecifikovaných faktorov:
a1 = 0,12 (m + n / 4) 0,5 (d k / d0) 0,25 (8,35)
kde m a n sú počet atómov uhlíka a vodíka v molekule alebo ich priemerné číslo pre komplexný plyn; d k - priemer požiarnych kanálov horáka, mm; d ° je referenčný priemer kanála horáka (1 mm).
Zabezpečenie úplnosti spaľovania v praktických podmienkach je pomerne zložitá úloha, ktorá závisí nielen od princípu spaľovania plynu, ale aj od podmienok vývoja plameňa v objeme pece. Najvyššie požiadavky na úplnosť spaľovania sa kladú na domáce spotrebiče a iné zariadenia, ktoré vypúšťajú produkty spaľovania do atmosféry. Spaľovanie plynu v takýchto zariadeniach je najťažšie, pretože je spojené s umývaním studených teplosmenných povrchov plameňom. Na spaľovanie plynu v domácich kachliach sa používajú vstrekovacie multiflame horáky, ktoré tvoria homogénnu zmes s koeficientom prebytku primárneho vzduchu α 1< 1. Недостающий для сгорания газа воздух поступает за счет диффузии из окружающей атмосферы.

Obr. 8.14. Koncentrácia oxidu uhoľnatého
v spalinách v plynovom sporáku
a - horák s periférnym prívodom sekundárneho vzduchu;
b - s napájaním centrálneho a periférneho sekundárneho vzduchu
1 - zemný plyn, periférny horák
sekundárny vzduch, vzdialenosť od dna nádoby je 25 mm;
2 - 4 - zemný plyn, horák s perifériou a
centrálny prívod sekundárneho vzduchu, vzdialenosť
na dno misky, mm: 2 - 25, 3 - 18, 4 - 10;
5 - skvapalnený plyn, horák s centrálnym a periférnym
prívod sekundárneho vzduchu, vzdialenosť od dna hrnca je 25 mm;
6 - skvapalnený plyn, periférny horák
Na obr. 8.14 ukazuje schémy 2-horákových horákov pre domáce plynové kachle a priemernú koncentráciu oxidu uhoľnatého CO v produktoch spaľovania prírodného metánu (95 obj.%) A propánu (93 obj.%) Keď horáky pracujú s menovitým tepelným výkonom. Rozdiel medzi horákmi spočíva v tom, že sekundárny vzduch je privádzaný k jednému z nich len z okraja a na druhý - z periférie az centrálneho kanála.
Úplnosť spaľovania plynu závisí od pomeru primárneho prebytku vzduchu v zmesi, vzdialenosti od požiarnych kanálov horáka po dno nádoby, typu horľavého plynu a spôsobu dodávania sekundárneho vzduchu. Zvýšenie obsahu primárneho vzduchu v zmesi, ako aj zvýšenie vzdialenosti od horáka ku dnu riadu vedie k zníženiu koncentrácie oxidu uhoľnatého v produktoch spaľovania. Minimálna koncentrácia oxidu uhoľnatého zodpovedá koeficientu prebytku primárneho vzduchu α 1 = 0,6 a vyššiemu a vzdialenosť od horáka ku dnu riadu je 25 mm a maximum - α 1 = 0,3 a nižšie a vzdialenosť horáka od dna nádoby je 10 mm. Okrem toho, zvýšenie tepelného výkonu horákov o 15 - 20% v dôsledku zvýšenia tlaku plynu vedie k zvýšeniu koncentrácie oxidu uhoľnatého v produktoch spaľovania o 1,2 - 1,3-krát a v dôsledku horiaceho tepla plynu - o 1,5 - 2%. časy.
Osobitná pozornosť by sa mala venovať vzniku aromatických zlúčenín v procese spaľovania - benzénu, polycyklického benzpyrénu, bezantracénu atď., Pretože niektoré z nich sú karcinogénne. Proces ich formovania je veľmi zložitý a postupuje postupne. V prvej fáze sa objaví acetylén a jeho deriváty. V zóne plameňa podliehajú tieto látky procesom predlžovania reťazca s preskupením trojitých uhlíkových väzieb na dvojité väzby. V dôsledku cyklizácie a dehydratácie sa objavujú rôzne aromatické zlúčeniny, vrátane polycyklických.
Tabuľka 8.16. Priemerná koncentrácia oxidu uhoľnatého a benzo (a) pyrénu v produktoch spaľovania závisí od typu plynu, typu horáka a prebytku primárneho vzduchu (tepelné zaťaženie horáka je 1600 kcal / h, vzdialenosť horáka od dna nádoby je 24-26 mm)
| Typ horáka | Priemerná koncentrácia | |
|---|---|---|
| oxid uhoľnatý, mg / l (v zmysle α = 1,0) |
benzo (a) pyrén, mcg / 100 m3 |
|
| Zemný plyn | ||
keď α i = 0,60 ÷ 0,70 |
0,10 | Nezistené |
keď α i = 0,30 ÷ 0,35 |
1,20 | skladieb |
keď α i = 0,60 ÷ 0,70 |
0,50 | Nezistené |
keď α i = 0,30 ÷ 0,35 |
0,12 | Nezistené |
| Skvapalnený ropný plyn | ||
| Horák s periférnym prívodom sekundárneho vzduchu: | ||
keď α i = 0,60 ÷ 0,70 |
0,30 | 0,03 |
keď α i = 0,30 ÷ 0,35 |
1,20 | 1,10 |
| Horák s centrálnym a periférnym prívodom sekundárneho vzduchu: | ||
keď α i = 0,60 ÷ 0,70 |
0,07 | 0,02 |
keď α i = 0,30 ÷ 0,35 |
1,00 | 0,045 |
Tabuľka údajov. 8.16 ukazujú, že pri spaľovaní prírodných plynov s prebytkom primárneho vzduchu α 1 = 0,6 a vyšším na obidvoch typoch horákov, koncentrácia splodín oxidu uhoľnatého spĺňa požiadavky GOST 5542-87.
Tabuľka 8.17. Vzdialenosť medzi okrajmi vypaľovacích kanálov jednoradových vstrekovacích horákov v závislosti od ich veľkosti a prebytku primárneho vzduchu
| Priemer požiarnych kanálov, mm | Vzdialenosť medzi okrajmi kanálov, mm pre rôzne hodnoty prebytku primárneho vzduchu α 1 | ||||
|---|---|---|---|---|---|
| 0,2 | 0,3 | 0,4 | 0,5 | 0,6 | |
| 2,0 | 11 | 8 | 6 | 5 | 4 |
| 3,0 | 15 | 12 | 9 | 7 | 5 |
| 4,0 | 16 | 14 | 11 | 9 | 7 |
| 5,0 | 18 | 15 | 14 | 12 | 10 |
| 6,0 | 20 | 18 | 16 | 14 | 12 |
Štúdie ukázali, že vzdialenosti medzi okrajmi palebných kanálov, ktoré zabezpečujú rýchle šírenie plameňa, ktoré zabraňuje ich zlúčeniu, závisia od ich veľkosti a obsahu primárneho vzduchu v zmesi, pričom sa s jeho nárastom znižuje. Optimálna vzdialenosť medzi okrajmi kanálov, zabezpečujúca dostatočnú úplnosť spaľovania plynu a rýchle šírenie plameňa sú uvedené v tabuľke č. 8.17. Pri usporiadaní požiarnych kanálov v dvoch radoch striedavo sa môže vzdialenosť medzi okrajmi odobrať z tej istej tabuľky. V tomto prípade by vzdialenosti medzi radmi mali byť 2-3 krát dlhšie ako vzdialenosti medzi kanálmi.

Obr. 8.15. Koncentrácia oxidu uhoľnatého, acetylénu, \\ t
etán, etylén a benzo (a) pyrén v produktoch spaľovania
strednotlakový plyn vo vstrekovacom horáku
Zovšeobecnenie mnohých experimentálnych údajov nám umožnilo získať priemerné koncentračné krivky v produktoch spaľovania rôznych zložiek, ktoré kvalitatívne a kvantitatívne charakterizujú proces spaľovania (Obr. 8.15). Úplné spaľovanie homogénnej zmesi plynu a vzduchu sa dosahuje len vtedy, keď je koeficient prebytku primárneho vzduchu α = 1,05 a vyšší. Pri znižovaní obsahu vzduchu v zmesi, najmä keď α< 1,0, возрастает концентрация оксида углерода СО, ацетилена С 2 Н 2 , этилена С 2 Н 4 , пропилена С 3 Н 6 и пропана С 3 Н 8 , а также бенз(а)-пирена С 20 Н 9 . Также возрастает концентрация и других компонентов - водорода, бензола и др.
Popri uvažovaných produktoch neúplného spaľovania vznikajú pri spaľovaní plynu vždy určité oxidy dusíka, ktorých tvorba prebieha vo vysokoteplotných zónach, a to ako po ukončení hlavných spaľovacích reakcií, tak aj počas procesu spaľovania. Maximálna koncentrácia NOx sa vyskytuje v konečných stupňoch, čo zodpovedá vyblednutiu plynu a intenzívnemu spaľovaniu medziproduktov vo forme vodíka a oxidu uhoľnatého.
Primárnou zlúčeninou pri spaľovaní zmesí plyn-vzduch je oxid dusnatý. Nástup reťazovej reakcie je spojený s atómovým kyslíkom, ktorý sa vyskytuje v zónach s vysokou teplotou v dôsledku disociácie molekulárneho kyslíka:
O 2 - ›2O - 490 kJ / mol (8,36)
O + N 2 - ›NO + N - 300 kJ / mol (8,37)
N + O 2 - ›2NO + 145 kJ / mol (8,38)
Bilančná reakcia
N2 + O2 - ›2NO - 177 kJ / mol (8,39)
K tvorbe atómového kyslíka dochádza tiež počas čiastočnej disociácie produktov spaľovania: ako klesá teplota a je prítomný kyslík, časť vytvoreného oxidu dusnatého (1 - 3 obj.%) Sa oxiduje na oxid dusičitý NO2. Reakcia prebieha najintenzívnejšie po uvoľnení oxidu dusnatého do atmosféry. Hlavné ovplyvňujúce faktory:
- teplota v reakčných zónach;
- pomer prebytočného vzduchu a kontaktný čas reagujúcich zložiek.
Teplota plameňa závisí od chemického zloženia plynu, obsahu vzduchu v zmesi plynu a vzduchu, stupňa jeho homogenity a odvodu tepla z reakčnej zóny. Maximálne možné pri tejto teplote, koncentrácia oxidu dusnatého, asi. % možno vypočítať podľa vzorca
NO p = 4,6e -2150 / (RT) / 020N2 (8,40)
kde NO p je rovnovážna koncentrácia oxidu dusnatého, obj. %; R je univerzálna plynová konštanta; T je absolútna teplota, K; O 2 a N 2 - koncentrácia, asi. % kyslíka a dusíka.
Vysoká koncentrácia oxidu dusnatého, zodpovedajúca rovnováhe, nastáva, keď sa plyn spaľuje v peciach výkonných parných generátorov a vo vysokoteplotných otvorených peciach. V malých a stredných kotloch, v malých vykurovacích a tepelných peciach s výrazným chladičom a krátkym časom zotrvania zložiek vo vysokoteplotných zónach je výťažok oxidu dusnatého rádovo menší. Okrem toho čím kratší je čas zdržania reagujúcich zložiek v zóne s vysokou teplotou, tým menej oxidu dusnatého v produktoch spaľovania.
Účinné je aj spaľovanie plynu v sálavých horákoch a vo fluidnom lôžku: v týchto prípadoch dochádza k mikrosférickému spaľovaniu homogénnej zmesi plynu a vzduchu s koeficientom prebytku vzduchu a = 1,05 s veľmi intenzívnym odvodom tepla z reakčnej zóny. Koncentrácia oxidov dusíka pri spaľovaní plynu v sálavých horákoch je okolo 40 a vo fluidnom lôžku 80 až 100 mg / m3. Zmenšenie veľkosti vypaľovacích kanálov vyžarujúcich horákov a žiaruvzdorných zŕn vo fluidnom lôžku pomáha znížiť výťažok oxidov dusíka.
Nahromadené údaje umožnili vykonať niekoľko zmien v konštrukcii kotla a vykurovacích zariadení, čím sa zabezpečí nielen vysoká účinnosť a nízka koncentrácia produktov nedokonalého spaľovania, ale aj znížené uvoľňovanie oxidov dusíka do atmosféry. Tieto zmeny zahŕňajú:
- zníženie dĺžky vysokoteplotných tunelov a ich premiestnenie do pece;
- použitie namiesto keramických tunelov stabilizátorov spaľovania vo forme telies so slabo usmerneným tvarom alebo prstencového plameňa;
- usporiadanie plochého plameňa so zvýšeným povrchom prenosu tepla;
- rozptyl plameňa v dôsledku zvýšenia počtu horákov alebo použitia blokových horákov;
- postupné privádzanie vzduchu do reakčnej zóny;
- rovnomerné rozloženie tepelných tokov v peci, tienenie pecí a ich rozdelenie do priehradiek sitom;
- použitie difúzneho princípu spaľovania plynu (difúzne spaľovanie je prípustné len v prípadoch, keď je možné zabezpečiť voľný vývoj plameňa bez umytia povrchov výmenníka tepla).
Najúčinnejšie zníženie výťažku oxidov dusíka sa dosahuje súčasným použitím niekoľkých metód.
Všeobecné informácie. Ďalším dôležitým zdrojom vnútorného znečistenia, silného senzibilizujúceho faktora pre ľudí, je zemný plyn a jeho produkty spaľovania. Plyn je viaczložkový systém pozostávajúci z desiatok rôznych zlúčenín, vrátane špeciálne pridaných (tabuľka č
Existuje priamy dôkaz, že používanie zariadení, ktoré spaľujú zemný plyn (plynové sporáky a kotly) má nepriaznivý vplyv na ľudské zdravie. Okrem toho jednotlivci so zvýšenou citlivosťou na faktory prostredia reagujú nedostatočne na zložky zemného plynu a jeho produkty spaľovania.
Zemný plyn v domácnosti je zdrojom mnohých rôznych znečisťujúcich látok. Patria sem zlúčeniny, ktoré sú priamo prítomné v plyne (odoranty, plynné uhľovodíky, toxické organokovové komplexy a rádioaktívny radón), produkty neúplného spaľovania (oxid uhoľnatý, oxid dusičitý, organické častice aerosólu, polycyklické aromatické uhľovodíky a malé množstvo prchavých organických zlúčenín). Všetky tieto zložky môžu ovplyvniť ľudský organizmus, a to ako samostatne, tak v kombinácii (synergický efekt).
Tabuľka 12.3
Zloženie plynného paliva
Aromatické látky. Odoranty sú organické aromatické zlúčeniny obsahujúce síru (merkaptány, tioétery a tioaromatické zlúčeniny). Pridávajú sa do zemného plynu, aby sa zistili v prípade úniku. Aj keď sú tieto zlúčeniny prítomné vo veľmi malých, podprahových koncentráciách, ktoré nie sú považované za toxické pre väčšinu jedincov, ich vôňa môže spôsobiť nevoľnosť a bolesti hlavy u zdravých ľudí.
Klinické skúsenosti a epidemiologické údaje naznačujú, že chemicky citliví ľudia reagujú nedostatočne na chemické zlúčeniny prítomné aj pri sublimálnych koncentráciách. Jedinci s astmou často identifikujú zápach ako promótor (spúšť) astmatických záchvatov.
Medzi odoranty patria napríklad metántiol. Metán-ol, tiež známy ako metylmerkaptán (merkaptometán, tiometylalkohol), je plynná zlúčenina, ktorá sa bežne používa ako aromatická prísada do zemného plynu. Nepríjemný zápach pociťuje väčšina ľudí v koncentrácii 1 diel na 140 ppm, avšak táto látka môže byť detegovaná pri oveľa nižších koncentráciách vysoko citlivými jedincami. Toxikologické štúdie na zvieratách ukázali, že 0,16% metántiolu, 3,3% etántiolu alebo 9,6% dimetylsulfidu sú schopné stimulovať stav komatózy u 50% potkanov vystavených týmto zlúčeninám počas 15 minút.
Iný merkaptán, tiež používaný ako aromatická prísada do zemného plynu - merkaptoetanol C2H6OS) je tiež známy ako 2-tioetanol, etylmerkaptán. Silne dráždi oči a pokožku, môže mať toxický účinok cez pokožku. Je horľavý a rozkladá sa pri zahrievaní na vysoko toxické výpary SOx.
Merkaptány, ktoré sú znečisťujúcimi látkami v interiéri, obsahujú síru a sú schopné zachytávať elementárnu ortuť. Vo vysokých koncentráciách môžu merkaptány spôsobiť zhoršenú periférnu cirkuláciu a zvýšenú srdcovú frekvenciu, môžu stimulovať stratu vedomia, rozvoj cyanózy alebo dokonca smrť.
Aerosóly. Spaľovanie zemného plynu vedie k tvorbe malých organických častíc (aerosólov), vrátane karcinogénnych aromatických uhľovodíkov, ako aj niektorých prchavých organických zlúčenín. DOS - pravdepodobne senzibilizujúce činidlá, ktoré sú schopné indukovať spolu s ďalšími zložkami syndróm „chorej budovy“, ako aj viacnásobnú chemickú citlivosť (MHC).
DOS tiež zahŕňa formaldehyd, ktorý sa tvorí v malých množstvách počas spaľovania plynu. Použitie plynových spotrebičov v dome, kde žijú citliví jedinci, zvyšuje vystavenie týmto stimulom, následne zvyšuje príznaky ochorenia a prispieva k ďalšej senzibilizácii.
Aerosóly vznikajúce pri spaľovaní zemného plynu sa môžu stať centrami adsorpcie pre rôzne chemické zlúčeniny prítomné vo vzduchu. Látky znečisťujúce ovzdušie sa tak môžu koncentrovať v mikrovolách, vzájomne reagovať, najmä keď kovy pôsobia ako katalyzátory reakcií. Čím je menšia častica, tým vyššia je koncentrácia aktivity takéhoto procesu.
Okrem toho vodná para vznikajúca pri spaľovaní zemného plynu je dopravným spojením pre aerosólové častice a znečisťujúce látky, keď sa prenášajú do pľúcnych alveol.
Počas spaľovania zemného plynu vznikajú aj aerosóly obsahujúce polycyklické aromatické uhľovodíky. Majú nepriaznivý vplyv na dýchací systém a sú známe karcinogény. Okrem toho uhľovodíky môžu viesť k chronickej toxicite u citlivých osôb.
Tvorba benzénu, toluénu, etylbenzénu a xylénu pri spaľovaní zemného plynu je tiež nepriaznivá pre ľudské zdravie. Je známe, že benzén je v dávkach hlboko pod prahom karcinogénny. Expozícia benzénu koreluje so zvýšeným rizikom rakoviny, najmä leukémie. Senzibilizačné účinky benzénu nie sú známe.
ORGANOMETALOVÉ ZLÚČENINY. Niektoré zložky zemného plynu môžu obsahovať vysoké koncentrácie toxických ťažkých kovov, vrátane olova, medi, ortuti, striebra a arzénu. S najväčšou pravdepodobnosťou sú tieto kovy prítomné v zemnom plyne vo forme organokovových komplexov, ako je trimetylarsenit (CH3) 3As. Spojenie s organickou matricou týchto toxických kovov ich robí rozpustnými v lipidoch. To vedie k vysokej miere absorpcie a tendencii k bioakumulácii v ľudskom tukovom tkanive. Vysoká toxicita tetrametylplumbbitu (CH3) 4Pb a dimetylmercury (CH3) 2Hg poukazuje na účinok na ľudské zdravie, pretože metylované kompozície týchto kovov sú toxickejšie ako samotné kovy. Tieto zlúčeniny sú obzvlášť nebezpečné počas laktácie u žien, pretože v tomto prípade lipid migruje z tukových zásobníkov tela.
Obzvlášť nebezpečná organokovová zlúčenina je dimetylortuť (CH3) 2Hg vzhľadom na svoju vysokú lipofilitu. Metylortuť môže byť inkorporovaná do tela prostredníctvom inhalácie, ako aj cez kožu. Absorpcia tejto zlúčeniny v gastrointestinálnom trakte je takmer 100%. Ortuť má výrazný neurotoxický účinok a vlastnosť ovplyvňuje ľudskú reprodukčnú funkciu. Toxikológia nemá údaje o bezpečných hladinách ortuti pre živé organizmy.
Organické zlúčeniny arzénu sú tiež veľmi jedovaté, najmä s ich metabolickou deštrukciou (metabolickou aktiváciou), čo vedie k tvorbe vysoko anorganických anorganických foriem.
Produkty spaľovania zemného plynu. Oxid dusičitý je schopný pôsobiť na pľúcny systém, čo uľahčuje rozvoj alergických reakcií na iné látky, znižuje funkciu pľúc, náchylnosť na infekčné pľúcne ochorenia a potencuje bronchiálnu astmu a iné ochorenia dýchacích ciest. To sa prejavuje najmä u detí.
Existujú dôkazy, že N02 produkovaný spaľovaním zemného plynu môže vyvolať:
- zápal pľúcneho systému a zníženie vitálnych funkcií pľúc;
- zvýšené riziko príznakov podobných astme, vrátane dýchavičnosti, dýchavičnosti a záchvatov ochorenia. To je bežné najmä u žien varujúcich jedlo na plynových sporákoch, ako aj u detí;
- zníženie rezistencie na bakteriálne pľúcne ochorenia v dôsledku zníženia imunologických mechanizmov ochrany pľúc;
- vo všeobecnosti negatívne ovplyvňujú imunitný systém ľudí a zvierat;
- expozícia ako adjuvans k rozvoju alergických reakcií na iné zložky;
- zvýšená citlivosť a zvýšená alergická reakcia na nežiaduce alergény.
V produktoch spaľovania zemného plynu existuje pomerne vysoká koncentrácia sírovodíka (H2S), ktorý znečisťuje životné prostredie. Je jedovatý v koncentráciách nižších ako 50 ppm a v koncentrácii 0,1-0,2% je smrteľný, dokonca aj pri krátkej expozícii. Pretože telo má mechanizmus na detoxikáciu tejto zlúčeniny, toxicita sírovodíka je spojená skôr s jeho koncentráciou účinku ako s trvaním expozície.
Hoci sírovodík má silný zápach, jeho nepretržitý účinok s nízkou koncentráciou vedie k strate čuchu. To umožňuje mať toxický účinok pre ľudí, ktorí môžu byť podvedome vystavení nebezpečným úrovniam tohto plynu. Nevýznamné koncentrácie v ovzduší obytných priestorov vedú k podráždeniu očí a nosa a hrdla. Stredné hladiny spôsobujú bolesti hlavy, závraty, ako aj kašeľ a ťažkosti s dýchaním. Vysoké hladiny vedú k šoku, kŕčom, kóme, ktoré končia smrťou. Preživší po akútnych toxických účinkoch sírovodíka sa stretávajú s neurologickými dysfunkciami, ako je amnézia, tremor, nerovnováha a niekedy vážnejšie poškodenie mozgu.
Akútna toxicita relatívne vysokých koncentrácií sírovodíka je dobre známa, avšak, bohužiaľ, existuje len málo informácií o chronickej nízkej expozícii ROS tejto zložky.
Radón. Radón (222Rn) je tiež prítomný v zemnom plyne a môže byť dodávaný potrubím do plynových pecí, ktoré sa stávajú zdrojom znečistenia. Pretože radón sa rozkladá na olovo (polčas 210Pb je 3,8 dňa), vedie to k vytvoreniu tenkej vrstvy rádioaktívneho olova (priemerná hrúbka 0,01 cm), ktorá pokrýva vnútorné povrchy rúr a zariadení. Tvorba vrstvy rádioaktívneho olova zvyšuje hodnotu pozadia rádioaktivity o niekoľko tisíc rozpadov za minútu (na ploche 100 cm2). Odstránenie je veľmi ťažké a vyžaduje výmenu rúrok.
Treba mať na pamäti, že jednoduché vypnutie plynového zariadenia nestačí na odstránenie toxických účinkov a na úľavu od chemicky citlivých pacientov. Plynové zariadenia musia byť úplne odstránené z priestorov, pretože aj nefunkčný plynový sporák naďalej vypúšťa aromatické zlúčeniny, ktoré absorboval počas rokov používania.
Kumulatívne účinky zemného plynu, účinky aromatických látok, splodín horenia na ľudské zdravie nie sú presne známe. Predpokladá sa, že účinky viacerých zlúčenín sa môžu množiť a odozva na účinky viacerých znečisťujúcich látok môže byť vyššia ako súčet jednotlivých účinkov.
Charakteristiky zemného plynu, ktoré vyvolávajú obavy o zdravie ľudí a zvierat, sú: \\ t
- horľavé a výbušné;
- asfixové vlastnosti;
- znečistenie priestorov znečistením ovzdušia;
- prítomnosť rádioaktívnych prvkov (radón);
- obsah vysoko toxických zlúčenín v produktoch spaľovania;
- prítomnosť stopových množstiev toxických kovov;
- obsah toxických aromatických zlúčenín pridaných do zemného plynu (najmä pre ľudí s viacerými chemickými citlivosťami);
- schopnosť zložiek plynu senzibilizovať.
A.S. Isserlin
Základom procesu spaľovania sú chemické reakcie spájania paliva s oxidačným činidlom. Pre proces horenia plynu musia byť vytvorené špeciálne podmienky. Po prvé, je potrebné dodať dostatočné množstvo okysličovadla (najčastejšie vzduchu) a zmiešať ich. Po druhé, zmes plynu a vzduchu by mala mať koncentračné limity horľavosti a mal by sa vytvoriť zdroj vznietenia. Po tretie, je potrebné vytvoriť podmienky pre rozvoj procesu spaľovania, teda určitej teploty.
Tvorba zmesi (rovnomerné miešanie plynu so vzduchom) je jedným z hlavných stupňov celého procesu spaľovania. Všetky ďalšie stupne, ktorými palivo prechádza počas premeny chemickej energie na tepelnú energiu, vo veľkej miere závisia od procesu miešania. Pretože v spaľovacej zóne je vždy stanovená vysoká teplota, čas strávený chemickými spaľovacími reakciami je vždy podstatne nižší ako čas potrebný na proces miešania.
Spaľovanie plynných palív, podobne ako akékoľvek iné, v prúdení vzduchu podľa moderných pohľadov je možné na základe princípov kinetiky a difúzie.
Celkový čas spaľovania plynu, ktorý určuje rýchlosť spaľovania, \\ t
TP TS ~ 1 "~ X1
Kde ts je čas miešania potrebný na zmiešanie plynu s oxidačným činidlom; mx je čas chemických reakcií.
Ak mc<Стх, то практически тп«т*. В этом случае процесс протекает в кинетической области. Если же, наоборот, Тс^-Тх, то Тп»тс и, следовательно, процесс протекает в диффузионной области.
Počas procesu spaľovania v kinetickej oblasti rýchlosť spaľovania závisí od vlastností tejto horľavej zmesi, teploty v reakčnom objeme a koncentrácie činidiel v spaľovacej zóne, t.j. je riadená zákonmi chemickej kinetiky. Zároveň rýchlosť procesu v kinetickej oblasti nezávisí od hydrodynamických faktorov, to znamená od rýchlosti prietoku, geometrických rozmerov reakčnej komory atď.
Naopak, v difúznej oblasti je rýchlosť procesu určená hydrodynamickými faktormi a nezávisí od kinetických. V tejto oblasti rozhodujúcu úlohu zohrávajú vlastnosti horľavej zmesi a teplotný faktor. Pomerne jednoduché hydrodynamické prostriedky môžu ovplyvniť intenzitu miešania, čo povedie k zmene vlastností difúzneho oblaku.
Pri kinetickom princípe sa v horáku vytvára homogénna zmes plynu a vzduchu, ktorá sa privádza do spaľovacej komory. Preto spaľovanie takejto zmesi prebieha pri konštantnej hodnote všetkých hlavných charakteristík (tepelný tlak, prebytočný vzduch atď.). Čisto kinetické pálenie sa vyskytuje len za podmienok ^ ^ 1,0. Na a<1 кинетическое горение протекает лишь на первой стадии, т. е. до тех пор, пока не израсходован весь кислород смеси. Остаток горючих компонентов, разбавленных продуктами сгорания, может быть сожжен только при условии подвода дополнительного окислителя (воздуха).
Princíp difúzie spaľovania znamená vytvorenie takých podmienok pre vznik procesu, v ktorom zmes horí bezprostredne pri svojom vzniku, to znamená, keď palivo a okysličovadlo prichádzajú do styku vo vhodných kvantitatívnych pomeroch. Proces difúzneho spaľovania je regulovaný zmenou intenzity tvorby zmesi zmenou konštrukcie a prevádzkových parametrov horáka. V dôsledku toho je možné v závislosti od technologických požiadaviek dosiahnuť skrátenie zmiešavacej zóny alebo jej predĺženie.
V praxi sa často používa spaľovanie plynu, ktoré kombinuje oba tieto princípy. V tomto prípade sa časť vzduchu predzmieša s plynom v horáku a zvyšok, ktorý je potrebný na úplné spaľovanie, sa privádza priamo do spaľovacej zóny. Zmenou tohto pomeru môžete ovplyvniť dĺžku plynového horáka. Vo väčšine horákov sa plyn privádza v určitom uhle k prúdu vzduchu.
Mnohé štúdie boli venované štúdiu procesu miešania. To nám umožňuje formulovať niektoré všeobecné vzorce.
Pre plynové horáky s priamym prúdením je miešanie tým lepšie, čím väčšia časť prierezu horáka pokrýva plynové prúdy, t.j. čím väčší je rozsah prúdov plynu. V horákoch s vysoko vírivými prúdmi by sa nemal usilovať o dlhé plynové trysky.
Zvýšenie skrútenia prúdu vzduchu vedie k prerozdeleniu plynu a vzduchu cez prierez horáka, k zvýšeniu intenzity miešania plynu so vzduchom a k zvýšeniu strednej zóny spätných prúdov v horáku.
Povaha vplyvu skrúcania prúdenia vzduchu na proces miešania sa líši v závislosti od ďalších určujúcich parametrov. Keď sa teda plyn privádza do periférnych zón horáka (bez ohľadu na jeho typ), zvýšenie prúdového krútenia vedie k znateľnému zlepšeniu tvorby zmesi. Naopak, keď sa plyn privádza do centrálnej zóny horáka, rast zákrutu spravidla nevedie k zlepšeniu procesu, “riešenie.
Kombinácia javov, ktoré nazývame pálením, môže pokračovať len v určitom poradí, z jednej fázy do druhej. GF Knorre uvádza nasledujúce diagramy ustáleného procesu spaľovania plynných a kvapalných palív s pevným jadrom, ktoré nazýva in-line (obr. 1). Najjednoduchšia schéma prúdenia sa vyskytuje pri spaľovaní plynného paliva pozostávajúceho z jednoduchých molekúl (napríklad vodíka), ktoré nevyžadujú predbežný komplexný pyrogénny rozklad (obr. 1, A).Ak sa spaľuje plynné alebo kvapalné uhľovodíkové palivo, \\ t A 6
Proces in-line spaľovania je komplikovaný: existuje ďalší medzistupeň - rozklad pyrogénu. V prípade kvapalných palív tomuto stupni predchádza stupeň odparovania (Obr. 1.6). Na realizáciu prietokovej schémy je v spaľovacej komore potrebná dostatočná teplota, ku ktorej sa palivo a oxidačné činidlo dodávajú v kontinuálnych prúdoch. Produkty spaľovania po ukončení reakcií sa tiež kontinuálne odstraňujú zo zdroja spaľovania.
Je známe, že zmesi plyn-vzduch sa zapaľujú len v prípade, keď je obsah plynu vo vzduchu v rámci určitých limitov (pre každý plyn). Pri nízkom obsahu plynu množstvo tepla uvoľnené počas spaľovania nestačí na privedenie susediacich vrstiev zmesi do teploty vznietenia. To isté sa pozoruje, keď je obsah plynu v zmesi plyn-vzduch príliš vysoký. Nedostatok kyslíka v spaľovacom vzduchu vedie k poklesu teploty, v dôsledku čoho sa priľahlé vrstvy zmesi nezohrievajú na
Bod vzplanutia Tieto dva prípady zodpovedajú dolným a horným limitom horľavosti (tabuľka 1). Okrem toho, okrem miešania plynu so vzduchom, musia byť v určitých pomeroch vytvorené počiatočné podmienky pre zapálenie zmesi.
|
Tabuľka / Limity horľavosti a vznietenia rôznych plynov vo vzduchu
|
Oxidácia horľavých plynov je možná pri nízkych teplotách, ale potom prebieha veľmi pomaly v dôsledku nízkej reakčnej rýchlosti. Ako stúpa teplota, rýchlosť oxidačnej reakcie sa zvyšuje pred nástupom samovznietenia (namiesto pomalej oxidácie začína proces spontánneho spaľovania). To znamená, že horľavá zmes zahrievaná na teplotu vznietenia má takú energiu, ktorá nielenže kompenzuje stratu tepla pre životné prostredie, ale tiež poskytuje ohrev a prípravu zmesi plynu a vzduchu vstupujúcej do spaľovacej zóny na zapálenie.
Teplota vznietenia plynu závisí od mnohých faktorov, vrátane obsahu horľavého plynu v zmesi plynu a vzduchu, tlaku, spôsobu ohrevu zmesi atď., A preto nie je presnou hodnotou. V záložke. 1 ukazuje teploty vznietenia niektorých horľavých plynov vo vzduchu.
V praxi existujú dva spôsoby vznietenia horľavých zmesí: samovznietenie a zapálenie.
na Samovznietenie Celý objem horľavej zmesi plyn-vzduch sa postupne privádza na teplotu vznietenia, po ktorej sa zmes zapáli bez vonkajšej tepelnej expozície.
Technika je široko používaná druhá metóda, tzv Zapaľovanie. Pri tejto metóde nie je nutné ohrievať celú zmes plynu a vzduchu na teplotu vznietenia, stačí, aby sa studená zmes zapálila na jednom mieste v objeme s niektorým zdrojom vysokej teploty (iskra, horúce teleso, pilotný plameň atď.). V dôsledku toho sa zapálenie prenáša spontánne na celý objem zmesi šírením plameňa, ku ktorému nedochádza okamžite, ale s určitou priestorovou rýchlosťou. Táto rýchlosť sa nazýva Rýchlosť plameňa v zmesi plyn-vzduch je to najdôležitejšia charakteristika určujúca podmienky pre prietok a stabilizáciu spaľovania. Stabilita horákov, ako bude ukázané nižšie, súvisí s rýchlosťou šírenia plameňa.
Proces spaľovania plynného paliva sa teda skladá zo zmiešavania plynu so vzduchom, zohrievania získanej zmesi na teplotu vznietenia, zapaľovania a uskutočňovania reakcií spaľovania, sprevádzaných uvoľňovaním tepla. Okrem toho miešanie plynu so vzduchom a zahrievanie zmesi zaberá väčšinu času počas procesu spaľovania, pretože reakcie horenia prebiehajú takmer okamžite.
V závislosti od technologického procesu (výroba pary a teplej vody v kotlovej jednotke, ohrev výrobkov v zariadení pece a pod.) Je potrebné ovplyvniť proces spaľovania zmenou jeho konečných vlastností. To sa dosahuje rôznymi konštrukčnými technikami, ktoré sú uvedené v kapitole. III.
Orientačné porovnanie teplotných polí v objeme horáka počas spaľovania plynu s rôznymi koeficientmi prebytku vzduchu. Príklad takéhoto porovnania je uvedený na obr. 2 pre horák s priemerom výstupu dýzy 35 mm ako závislosť
|
|
kde a - aktuálna hodnota teploty v erupe, ° С; £ max - maximálna teplota v horáku (merané), ° C; X- vzdialenosť od meracieho bodu po začiatok horáka, m; v - vzdialenosť od meracieho bodu k osi horáka, m; TH - priemer dýzy horáka, m.
Na obr. 2 grafy rozloženia teploty pre tri koeficienty prebytku vzduchu. A súradnice X / d= O zodpovedá výstupnej časti dýzy horáka a súradnice U / d= 0 - os horáka.
Ako je zrejmé z obrázku, rozloženie teploty vo voľnom horáku je nerovnomerné. Pri malých prebytkoch primárneho vzduchu, napríklad a = 0,5, prítomnosť vnútorného jadra v oblaku značne skresľuje teplotné pole a je zarovnaná len pri x / s / = 10, zatiaľ čo pri a = 0,75 sa vyrovnanie vyskytuje už pri X / d= 2,5, a = 1,0 ešte skôr - s X / d = 1,0.
Najvyššie teploty v otvorených horákoch sú pozorované v počiatočných úsekoch vo vzdialenosti od osi horáka Y / d =0,5 a potom v strede horáka. Okrem toho, so zvýšením koeficientu prebytku vzduchu, sa maximálna teplota posúva smerom k ústiu horáka. Takže najvyššia teplota pri a = 0,75 meraná vo vzdialenosti X / d= 2,5 a keď a = 1,0 - vo vzdialenosti X / d = 1,0.
 Keď spoločne zvážime rozloženie teplôt a koncentrácií C02 v oblaku, maximá sa zhodujú.
Keď spoločne zvážime rozloženie teplôt a koncentrácií C02 v oblaku, maximá sa zhodujú.
Teploty a obsah C02. V dôsledku toho maximálna úroveň teploty v erupcii tiež zodpovedá maximálnej hodnote stupňa horenia horľavého materiálu.
Strata časti tepla uvoľneného spaľovaním plynu je nevyhnutná. Pri správnom riadení procesu spaľovania sa však dajú znížiť na minimum. Zvážte, z čoho. týchto strát.
Pri spaľovaní plynných palív dochádza k nasledujúcim tepelným stratám: s odchádzajúcimi plynmi, chemickým neúplným spaľovaním a do životného prostredia. Na základe stanovenia jednotlivých tepelných strát v reverznom zostatku možno vypočítať účinnosť jednotky, ° / o:
kde<72 - потери тепла с уходящими газами, %; - потери тепла
Z chemického neúplného spaľovania,%; Q5 - tepelné straty pre životné prostredie,%.
Tepelné straty s odchádzajúcimi plynmi - fyzikálne teplo produktov spaľovania opúšťajúcich jednotku sú hlavnými. Nie je možné ich úplne odstrániť, ale je potrebné usilovať sa o ich zníženie. Tepelné straty s výfukovými plynmi závisia od teploty plynov a ich množstva. Čím nižšia je teplota spalín, tým menej tepla sa stráca, takže by ste sa mali snažiť znížiť teplotu spalín v primeraných medziach. Vplyv teploty spalín na tepelné straty je možné vidieť z tabuľky. 2.
Tabuľka 2
|
Tepelné straty s odchádzajúcimi plynmi pri spaľovaní zemného plynu,%
|
Strata tepla z odchádzajúcich plynov sa obyčajne vyjadruje ako percento z celkového dostupného tepla, t.j. zo spaľovacieho tepla paliva. Napríklad, ak je tepelná strata 700 kcal / m3 pri spaľovaní zemného plynu, potom
700-100 ___ „24 ° /
Počet plynov opúšťajúcich jednotku závisí od koeficientu prebytku vzduchu, s ktorým horák pracuje, a od prísaviek.
Vzduch cez netesnosti v jednotke. Čím väčší je koeficient prebytku vzduchu na výstupe horáka a nasávanie vzduchu do jednotky, tým vyššia je tepelná strata s výstupnými plynmi. Z karty. 2 je možné vidieť, že zmena celkového pomeru prebytočného vzduchu v produktoch spaľovania s aa = 1,2-5-1,6 zvyšuje tepelnú stratu spalín z 10,5 na 13,2% (pri konštantnej teplote spalín 240 ° C).
Aby sa znížili tepelné straty pomocou spalín, je potrebné uskutočniť proces spaľovania s najnižším prípustným pomerom prebytočného vzduchu, zabezpečiť najvyššiu hustotu jednotky a dosiahnuť zníženie teploty spalín.
Tepelné straty vznikajúce pri chemickom neúplnom spaľovaní plynu vznikajú pri nedostatku vzduchu, slabom miešaní v plynovom horáku a prudkom poklese teploty v spaľovacej zóne. V dôsledku toho spaľovanie plynu prebieha neúplne a horľavé zložky (napríklad vodík, oxid uhoľnatý atď.) Opúšťajú produkty spaľovania. To vedie k nedostatočnému využitiu chemickej energie paliva a zníženiu účinnosti jednotky. Aj malý obsah horľavých zložiek v produktoch spaľovania vedie k významným tepelným stratám z chemického neúplného spaľovania. Predpokladajme, že produkty spaľovania obsahovali 0,7% vodíka a 0,5% oxidu uhoľnatého. Zemný plyn bol spaľovaný v jednotke s pomerom prebytočného vzduchu za zariadením a = 1,5. Tepelné straty z chemického neúplného spaľovania boli ~ 450 kcal / m3 alebo
A ___ 450-100 poo /
Z vyššie uvedeného príkladu je teda zrejmé, že horľavé zložky v produktoch spaľovania musia byť úplne neprítomné alebo musia byť minimálnou hodnotou.
Tepelné straty do životného prostredia sú spôsobené tým, že steny jednotky majú vyššiu teplotu ako okolitý vzduch. Veľkosť týchto strát závisí najmä od rozdielu teplôt medzi vonkajšími stenami jednotky a okolitým vzduchom, veľkosti povrchu steny, tepelnej vodivosti muriva a jeho hrúbky. Straty do životného prostredia sú vypočítané teoreticky alebo sú prevzaté z noriem tepelného výpočtu v závislosti od konštrukcie a výkonu jednotky.
Ak zhrnieme všetky tepelné straty, ktoré vznikajú pri spaľovaní plynu v jednotke, a odpočítame ich od 100, potom získame účinnosť jednotky. Použite napríklad vyššie uvedené čísla<75 равным 3,60%, тогда к. п. д. агрегата
T] = 100- (8,24 + 5,28 + 3,60) = 82,88% *
Spaľovanie plynu je kombináciou nasledujúcich procesov:
· Miešanie horľavého plynu so vzduchom,
· Zahrievanie zmesi
· Tepelný rozklad horľavých zložiek,
· Zapálenie a chemická kombinácia horľavých zložiek s kyslíkom zo vzduchu, sprevádzaná tvorbou horáka a intenzívneho vytvárania tepla.
Pri reakcii dochádza k spaľovaniu metánu:
CH4 + 2O2 = C02 + 2H20
Podmienky požadované pre spaľovanie plynu:
· Zabezpečenie potrebného pomeru horľavého plynu a vzduchu,
· Zahrievanie na teplotu vznietenia.
Ak je zmes plynov a plynov nižšia ako dolná hranica zapaľovania, nebude horieť.
Ak je v zmesi plynu a vzduchu viac plynu ako horná hranica zapaľovania, nebude úplne horieť.
Zloženie produktov úplného spaľovania plynu:
CO2 - oxid uhličitý
H20 - vodná para
* N 2 - dusík (nereaguje s kyslíkom počas spaľovania)
Zloženie produktov nedokonalého spaľovania plynu:
· CO - oxid uhoľnatý
· C - sadze.
Na spaľovanie 1 m3 zemného plynu je potrebných 9,5 m3 vzduchu. V praxi je prietok vzduchu vždy väčší.
postoj skutočnú spotrebuvzduchu teoreticky potrebné nákladynazývaný koeficient prebytku vzduchu: α = L / L t.,
Kde: L - skutočná spotreba;
Lt - teoreticky potrebný prietok.
Pomer prebytočného vzduchu je vždy väčší ako jeden. Pre zemný plyn je to 1,05 - 1,2.
2. Účel, zariadenie a hlavné charakteristiky prietokových ohrievačov vody.
Prúdové ohrievače vody. Navrhnuté na ohrev vody na určitú teplotu počas odberu vody Prietokové ohrievače vody sú rozdelené podľa zaťaženia tepelným výkonom: 33600, 75600, 105000 kJ, podľa stupňa automatizácie - do najvyššej a prvej triedy. efektívnosť ohrievače vody sú 80%, obsah oxidu nie je vyšší ako 0,05%, teplota produktov spaľovania za rezačom je najmenej 180 ° C. Princíp je založený na ohreve vody počas odberu vody.
Hlavnými uzlami prietokových ohrievačov vody sú: plynový horák, výmenník tepla, automatizačný systém a výstup plynu. Do vstrekovacieho horáka sa privádza nízkotlakový plyn. Spaľovacie produkty prechádzajú cez výmenník tepla a sú odvádzané do komína. Spaľovacie teplo sa prenáša do vody prúdiacej cez výmenník tepla. Na ochladenie požiarnej komory slúži ako cievka, cez ktorú prúdi voda cez ohrievač. Plynové prietokové ohrievače vody sú vybavené zariadeniami na odvod spalín a tlmičmi nárazov, ktoré v prípade krátkodobého porušenia ťahu zabraňujú zániku plameňa zariadenia na spaľovanie plynu. Na vstup do komína sa nachádza vývod dymu.
Plynový ohrievač vody –VPG.Na prednej stene skrine sa nachádza: ovládací gombík na plynový kohútik, tlačidlo na napájanie elektromagnetického ventilu a pozorovacie okienko na monitorovanie zapaľovania a plameňa hlavného horáka. Zariadenie na odvod dymu sa nachádza v hornej časti zariadenia a odbočky na pripojenie zariadenia k systému plynu a vody sú umiestnené v spodnej časti. Plyn vstupuje do solenoidového ventilu, plynový blokovací ventil plynového plynového horáka postupne zapína pilotný horák a dodáva plyn do hlavného horáka.
Blokovanie prívodu plynu k hlavnému horáku s povinnou prevádzkou zapaľovača sa vykonáva elektromagnetickým ventilom ovládaným termočlánkom. V závislosti od prítomnosti prívodu vody je prívod plynu do hlavného horáka blokovaný ventilom poháňaným cez driek z membrány ventilu vodného bloku.
Spaľovanie plynných palív je kombináciou nasledujúcich fyzikálno-chemických procesov: zmiešavanie horľavého plynu so vzduchom, ohrievanie zmesi, tepelný rozklad horľavých zložiek, vznietenie a chemická kombinácia horľavých prvkov so vzdušným kyslíkom.
Stabilné spaľovanie zmesi plynu a vzduchu je možné kontinuálnym prívodom potrebného množstva horľavého plynu a vzduchu do spaľovacej prednej časti, dôkladným zmiešaním a zahriatím na teplotu zapálenia alebo samovznietením (tabuľka 5).
Zapálenie zmesi plyn - vzduch sa môže vykonať:
- zahrievanie celého objemu zmesi plyn-vzduch na teplotu samovznietenia. Táto metóda sa používa v spaľovacích motoroch, kde sa zmes plynu a vzduchu zahrieva rýchlym stlačením na určitý tlak;
- použitie cudzích zdrojov zapálenia (zapaľovače atď.). V tomto prípade nie je všetka zmes plyn / vzduch zahrievaná na teplotu vznietenia, ale jej časť. Táto metóda sa používa pri spaľovaní plynov v plynových horákoch;
- nepretržite v procese horenia.
Na spustenie spaľovania plynných palív je potrebné určité množstvo energie na rozbitie molekulárnych väzieb a vytvorenie nových.
Chemický vzorec na spaľovanie plynného paliva, ktorý označuje celý reakčný mechanizmus spojený so vznikom a zánikom veľkého počtu voľných atómov, radikálov a iných aktívnych častíc, je zložitý. Preto na zjednodušenie používajú rovnice vyjadrujúce počiatočné a konečné stavy reakcií spaľovania plynu.
Ak uhľovodíkové plyny označujú C m Hn, potom má formu chemickej reakcie spaľovania týchto plynov v kyslíku
CmHn + (m + n / 4) 02 = mCO2 + (n / 2) H20,
kde m je počet atómov uhlíka v uhľovodíkovom plyne; n je počet atómov vodíka v plyne; (m + n / 4) - množstvo kyslíka potrebné na úplné spálenie plynu.
Rovnice pre spaľovanie plynov sú odvodené podľa vzorca:
- metán CH4 + 2O2 = С02 + 2N20
- etán C2H6 + 3,5O2 = 2O2 + + H20
- bután C4H10 + 6,52 = 4С02 + 5N20
- propán C3H8 + 5O3 = ЗСО 2 + 4N20.
V praktických podmienkach spaľovania plynu sa kyslík neprijíma v čistej forme, ale je zahrnutý v zložení vzduchu. Pretože vzduch pozostáva v objeme 79% dusíka a 21% kyslíka, každý objem kyslíka vyžaduje 100: 21 = 4,76 objemu vzduchu alebo 79: 21 = = 3,76 objemu dusíka. Potom je možné zapísať spaľovaciu reakciu metánu vo vzduchu nasledovne: \\ t
CH4 + 2O2 + 2 x 3,76N2 = C02 + 2H20 + 7,52N2.
Z rovnice je zrejmé, že na spaľovanie 1 m3 metánu je potrebných 1 m3 kyslíka a 7,52 m3 dusíka alebo 2 + 7,52 = 9,52 m3 vzduchu.
V dôsledku horenia 1 m3 metánu sa získa 1 m3 oxidu uhličitého, 2 m3 vodnej pary a 7,52 m3 dusíka. Nižšie uvedená tabuľka uvádza tieto údaje pre najčastejšie horľavé plyny.
Pre proces spaľovania zmesi plynu a vzduchu je potrebné, aby množstvo plynu a vzduchu v zmesi plynu a vzduchu bolo v určitých medziach. Tieto limity sa nazývajú horľavé limity alebo výbušné limity. Existujú nižšie a horné limity horľavosti. Minimálny obsah plynu v zmesi plynu a vzduchu, vyjadrený v objemových percentách, pri ktorom dochádza k vznieteniu, sa nazýva dolný limit horľavosti. Maximálny obsah plynu v zmesi plynu a vzduchu, nad ktorou sa zmes nezapáli bez dodatočného tepla, sa nazýva horný limit horľavosti.
Množstvo kyslíka a vzduchu pri spaľovaní niektorých plynov
|
Na spaľovanie 1 m 3 potrebného plynu, m 3 |
Pri horení sa uvoľňuje 1 m3 plynu, m3 |
Spaľovacie teplo He, kJ / m 3 |
|||||
|
kyslík |
dioxid uhlík |
||||||
|
Oxid uhoľnatý |
|||||||
Ak zmes plyn-vzduch obsahuje menej plynu ako dolná hranica horľavosti, nebude horieť. Ak v zmesi plyn-vzduch nie je dostatok vzduchu, spaľovanie sa nepokračuje úplne.
Inertné nečistoty v plynoch majú veľký vplyv na veľkosť výbušných limitov. Zvýšenie obsahu predradníka v plyne (N2 a CO 2) zužuje limity horľavosti a pri zvýšení obsahu predradníka nad určité limity sa zmes plynu so vzduchom nezapaľuje pri žiadnom pomere plynu a vzduchu (tabuľka nižšie).
Množstvo objemov inertného plynu k 1 objemu horľavého plynu, v ktorom zmes plynu a vzduchu prestáva byť výbušná
Najmenšie množstvo vzduchu potrebné na úplné spaľovanie plynu sa nazýva teoretické prúdenie vzduchu a označuje ho Lt, to znamená, ak je výhrevnosť plynového paliva 33520 kJ / m 3 , potom teoreticky potrebné množstvo vzduchu na spaľovanie 1 m 3 plyn
L T= (33 520/4190) / 1,1 = 8,8 m3.
Skutočný prietok vzduchu však vždy prekračuje teoretický prietok. To je vysvetlené tým, že je veľmi ťažké dosiahnuť úplné spaľovanie plynu s teoretickým prúdením vzduchu. Preto akékoľvek plynové zariadenie na spaľovanie plynu pracuje s prebytočným vzduchom.
Praktické prúdenie vzduchu
Ln = aLT,
kde Ln - praktické prúdenie vzduchu; α - koeficient prebytku vzduchu; L T - teoretické prúdenie vzduchu.
Pomer prebytočného vzduchu je vždy väčší ako jeden. Pre zemný plyn je to α = 1,05 - 1,2. faktor α Zobrazuje, koľkokrát skutočný prietok vzduchu prekračuje teoretickú hodnotu na jednotku. ak α = 1, potom sa nazýva zmes plyn-vzduch stechiometrický.
na α = 1.2 sa spaľovanie plynu vykonáva s prebytkom vzduchu o 20%. Spravidla sa musí spaľovanie plynov uskutočňovať s minimálnou hodnotou a, pretože pri znižovaní prebytku vzduchu sa znižujú tepelné straty so spalinami. Vzduch zúčastňujúci sa na spaľovaní sa deje primárne a sekundárne. primárny volal vzduch vstupujúci do horáka, aby sa zmiešal s plynom; sekundárne - vzduch vstupujúci do spaľovacej zóny nie je zmiešaný s plynom, ale samostatne.


 Horľavé látky a materiály
Horľavé látky a materiály Prenášajte údaje plynomeru do Nizhegorodenergogazraschen na plyne č
Prenášajte údaje plynomeru do Nizhegorodenergogazraschen na plyne č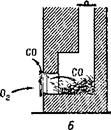 Hlavná chemická reakcia spaľovacieho procesu
Hlavná chemická reakcia spaľovacieho procesu Litmus test - meranie pH
Litmus test - meranie pH