बर्निंग म्हणतात. दहन दरम्यान रासायनिक प्रक्रिया
काही मूलभूत व्याख्या
परमाणु आणि अणूंची संख्या सहजपणे व्यक्त केली जाते पदार्थांची मात्रा एकतर पदार्थ च्या moles संख्या. पदार्थाचा एक तारा 6.023 ∙ 10 23 कण (परमाणु आणि रेणू) शी जुळतो. संख्या ए = 6.023 ∙ 10 23 एमओएल -1 याला एवोगद्रो क्रमांक असे म्हणतात. मोल अपूर्णांक एक्स मीघटक मी moles संख्या गुणोत्तर आहे मी घटक मी एकूण संख्या n = Σ n moles मी मिश्रण ( एक्स मी = एन मी / एन).
मास मी पदार्थाचे मूलभूत गुणधर्म (एसआय सिस्टीम मधील मोजण्याचे एकक किलोग्राम आहे). वस्तुमान अपूर्णांक वायू हा गुणोत्तर आहे मी मी घटक मी मिश्रण एकूण वस्तुमान m = Σ मी मी (वाय = एम मी / एम).
आण्विक वजन (किंवा आण्विक वजन) एम मी(जी / एमओएल) घटक मी - या घटकाच्या एक तळाचा वस्तुमान आहे. तर, आण्विक कार्बन, आण्विक हायड्रोजन, ऑक्सिजन आणि मीथेनसाठी आपल्याकडे: एम सी = 12 ग्रॅम / एमओएल, एमएन 2 = 2 ग्रॅम / एमओएल, मो 2 = 32 ग्रॅम / एमओएल, एमएन 4 = 16 ग्रॅम / एमओएल. मिश्रण एम (जी / एमओएल) च्या मिश्रणाचा सरासरी चक्रीय वस्तु घटकांच्या दाहक अंशांच्या संदर्भात व्यक्त केला जाऊ शकतो (एम = एक्स मी एम).
दहन प्रक्रिया निश्चित करणे
जळणे - ही एक जटिल भौतिक-रासायनिक प्रक्रिया आहे ज्यात ज्वलनशील पदार्थ आणि उच्च तापमानाच्या प्रभावाखाली असलेले साहित्य ऑक्सिडायझिंग एजंट (हवेमध्ये ऑक्सिजन) सह रासायनिक परस्परसंवादात प्रवेश करतात, दहन उत्पादनांमध्ये रुपांतरीत होतात आणि ज्यामध्ये तीव्र ताप आणि प्रकाश उत्सर्जन होते.
दहन प्रक्रिया घडण्यासाठी आवश्यक परिस्थिती:
दहनशील पदार्थ (जीव्ही) ची उपस्थिती;
ऑक्सिडायझिंग एजंट (ओ) - हवा ऑक्सिजनची उपस्थिती;
इग्निशन (आयझेड) स्त्रोताची उपस्थिती.
दहनशील पदार्थ विशिष्ट तापमानाला गरम करणे आवश्यक आहे ज्यामध्ये ऑक्सीकरण प्रक्रिया सुरू होईल;
विशिष्ट तापमानात दहनशील पदार्थ उष्णता करण्यासाठी, विशिष्ट इग्निशन स्त्रोत शक्ती आवश्यक असते;
दहन प्रक्रियेची देखभाल करण्यासाठी, इंधन आणि ऑक्सिडायझरचे विशिष्ट प्रमाण आवश्यक आहे.
सर्वात महत्वाची दहन प्रक्रिया ही उष्ण आणि वस्तुमान हस्तांतरण असते. बर्निंगची सर्वात सामान्य मालमत्ता म्हणजे ज्वाळाची घटना आणि उष्णता हस्तांतरण करून किंवा दहन क्षेत्रापासून सक्रिय कणांवर ताजे दहनशील मिश्रण करून ते दहनशील मिश्रणांमधून हलवित आहे.
फ्लेम - हे बर्णिंगचे दृश्यमान रूप आहे. याला बर्निंग झोन देखील म्हटले जाते. हा त्या जागेचा भाग आहे जिथे संपूर्ण आणि अपूर्ण कणांच्या उत्पादनांमध्ये दहनशील मिश्रण बदलते.
दहन प्रक्रियेचे मुख्य घटक, मृत्यूस कारणीभूत ठरतात आणि सामग्रीस नुकसान पोहोचवतात:
मोठ्या प्रमाणात उष्णता;
उच्च तपमान;
दहन उत्पादनांची विषारी रचना.
गॅसच्या आण्विक किनेटिक सिद्धांतांच्या दृष्टिकोनातून दहन प्रक्रिया
अंजीर 2.1. तपमानावर अवलंबून सक्रिय रेणूंचे प्रमाण: टी 2\u003e टी 1
गरम गॅस ज्वलनशील मिश्रण जास्त ऊर्जा वाढविते.
सक्रिय स्थितीतील अणुंचे सरासरी ऊर्जा पातळी आणि निष्क्रिय स्थितीचा सरासरी स्तर यांच्यातील फरक याला सक्रियकरण ऊर्जा म्हटले जाते. हे ग्राफिकल (आकृती 2) दर्शविले जाऊ शकते.

अंजीर 2.2. प्रतिक्रिया कोर्सचे ऊर्जा आरेख जी. व्ही. + ओ. ® पीजी: ई एक्ट - सक्रियकरण ऊर्जा; प्रश्न xr - दहन प्रतिक्रिया च्या थर्मल प्रभाव
"प्रथम" प्रतिक्रियायुक्त अणूंच्या परस्परसंवादामुळे उद्भवलेली ऊर्जा शेजारच्या अणूंना हस्तांतरित केली जाते. ते उत्साहित आहेत, प्रक्रिया वारंवार वारंवारता आणि तीव्रतेने प्रतिक्रिया असलेल्या रेणूंच्या आसपास पुनरावृत्ती होते. रासायनिक क्रियाकलापांची संपूर्ण प्रतिक्रिया मिश्रण (2 एच 2 + ओ 2) प्रक्रियेची स्वयंपूर्णता, स्वयंपूर्ण करणे, पाण्यातील अणूंचा निर्मिती आणि वातावरणात उष्णता सोडणे यासह आणि लुमनेससेन्ससह, उदा. उद्भवते आणि बर्णिंग प्रक्रिया पसरते.
ई-एक्टचे संख्यात्मक मूल्य जितके जास्त असेल तितकेच हे घटक घटकांना रासायनिक परस्परसंवादात समाविष्ट करणे अधिक कठीण आहे. म्हणून, ई कायद्याचे मूल्य ही रासायनिक प्रणालीच्या अग्नि धोक्याची पातळी अप्रत्यक्ष सूचक आहे.
प्रकार आणि दहन च्या पद्धती
खालील घटकांद्वारे दहन वर्गीकृत केले जाऊ शकते:
1. दहनशील घटकांचे मिश्रण मिसळण्याच्या स्थितीनुसार:
ए) किनेटिक - पूर्व-मिश्रित गॅस किंवा वाष्प-एअर मिश्रणांचे दहन. इंधन आणि ऑक्सिडंट यांचे मिश्रण जळजळ होईपर्यंत दहनसाठी तयार आहे, दहन प्रक्रियेचा एकूण दर केवळ दहनच्या रासायनिक प्रतिक्रियाच्या दरावर अवलंबून असतो. जर एखादा दहन बंद किंवा मर्यादित प्रमाणात झाला तर विस्फोट होऊ शकतो. मिश्रण दहन प्रक्रियेत सोडल्या गेलेल्या उर्जामध्ये या खंडापेक्षा जास्त काळ सोडला जाणार नाही, दबाव वाढवून संरचनांचे नाश होऊ शकते;
बी) प्रसार, प्रसार संयोग याला दहन म्हणतात, जेव्हा दहनशील माध्यम (ईंधन आणि ऑक्सिडायझर यांचे मिश्रण) दहन क्षेत्र किंवा दहन क्षेत्रापूर्वी होते.
2. रासायनिक प्रतिक्रिया क्षेत्रातील दहनशील घटक मिळवण्याच्या तीव्रतेनुसार:
अ) लमिनेर, तर दहनशील मिश्रण घटक घटकांच्या तुलनेत शांतपणे दहन करतात. या प्रकरणात, रेनॉल्ड्सच्या निकषांचे संख्यात्मक मूल्य, ज्या थर्मोडायनामिक व्यवस्थेचे वर्णन करतात, महत्त्वपूर्ण (आणि पुन्हा<2300).
ब) अशक्तपणा, दहनयुक्त मिश्रण घटकांसह हाय स्पीडवर दहन क्षेत्र प्रविष्ट करते. या प्रकरणात रेनॉल्ड्स क्रमांक 2300 पेक्षा अधिक आहे.
3. दहनशील मिश्रण घटकांच्या एकत्रीकरणाच्या स्थितीनुसार:
अ) एकसमान इंधन आणि ऑक्सिडायझर समान समृद्ध अवस्थेत (वायू) आहेत;
बी) विषमता (मल्टीफेस) - इंधन आणि ऑक्सिडंट वेगवेगळ्या समृद्ध अवस्थांमध्ये आहेत.
4. दहनच्या रासायनिक अभिक्रियाच्या क्षेत्राच्या प्रचाराच्या वेगानुसार:
अ) रासायनिक प्रतिक्रिया झोन (0.5 ते 50 मीटर / सेकंद वेग) च्या डिफ्लॅग्रेशन (मंद) वितरण;
ब) विस्फोटक (स्फोटक द्रव्य), जेव्हा दहनच्या रासायनिक प्रतिक्रियाचा झटका शॉक वेव्हच्या वेगाने (काही शंभर मीटर प्रति सेकंदापासून प्रति सेकंद प्रति सेकंदापर्यंत) वेगाने पसरतो.
वाफ किंवा वायू जळत असलेल्या जागेस म्हणतात ज्वाला करून .
लमिनासारखी पूर्व-मिश्रित ज्वाला पूर्व-मिश्रित मिश्रणाच्या लमिनेरच्या ज्वालांमध्ये दहन सुरू होण्याआधी इंधन आणि ऑक्सिडंट मिश्रित होतात आणि प्रवाह लमिनेर आहे.
पूर्व मिश्रित मिश्रण ज्वालामुखी म्हणतात stoichiometric जर इंधन (हायड्रोकार्बन) आणि ऑक्सिडायझर (ऑक्सिजन - ओ 2) एकमेकांना पूर्णपणे उपभोगतील तर कार्बन डाय ऑक्साईड (सीओ 2) आणि पाणी (एच 2 ओ) तयार करतात. जर जास्त प्रमाणात इंधन असेल तर ते म्हणतात की मिश्रण समृद्ध आहे आणि जर ऑक्सिडंट जास्त प्रमाणात असेल तर ते म्हणतात की मिश्रण खराब आहे.
सर्वात सोपा उदाहरणे विचारात घ्या:
1) 2 एच 2 + ओ 2 → 2 एच 2 ओ - स्टॉइचोमेट्रिक मिश्रण,
2) ЗН 2 + О 2 → 2 एच 2 ओ + एन 2 - समृद्ध मिश्रण (जास्त 2)
3) सीएच 4 + झॉ 2 2 → 2 एच 2 ओ + सीओ 2 + ओ 2 - पातळ मिश्रण (ओ 2 अतिरिक्त).
अशा रासायनिक प्रतिक्रिया समीकरण मधील प्रत्येक चिन्ह पदार्थाच्या एका तळाशी जुळतो. अशाप्रकारे, या समीकरणातील प्रथम म्हणजे एच 2 च्या दोन छिद्रे H 2 ओच्या दोन छिद्रे बनविण्यासाठी O च्या एक तळाशी प्रतिक्रिया देतात.
जर रासायनिक प्रतिक्रिया समीकरण अशा प्रकारे लिहीले जाते की ते केवळ इंधनाच्या एका छिद्रांच्या प्रतिक्रियाचे वर्णन करते, तर स्टॉइचियोमेट्रिक मिश्रणात इंधनचा तळाचा भाग सहजपणे संबंधांमधून निश्चित केला जाऊ शकतो.
एक्स पर्वत, stokh = 1 / ((1 + वी)
येथे विसीओ 2 आणि एच 2 ओ निर्मितीसह प्रतिक्रिया समीकरणांमधील ओ 2 च्या मॉलची संख्या दर्शवते. एक उदाहरण म्हणजे प्रतिक्रिया
एच 2 + 0.5 ओ 2 → एच 2 ओ, व्ही = 0.5, एक्स एच 2, स्टॉच = 2/3
जर ऑक्सिडायझर हवा असेल तर त्यामध्ये कोरड्या वायुमध्ये केवळ 21% ऑक्सिजन तसेच 78% नायट्रोजन आणि 1% उत्कृष्ट वायू असतात. म्हणून, हवेसाठी, एक्स एन 2 = 3.762 एक्स ओ 2. येथून स्टॉइकोमेट्रिक मिश्रण साठी हवेच्या फळाचे प्रमाण समान असेल
एक्स पर्वत, stokh = 1 / (((1 + v ∙ 4.762), ![]() ,
,
कुठे वि आधी म्हणजे सीओ 2 आणि एच 2 ओला इंधनाच्या एका तळाशी पूर्ण रूपांतरणाच्या प्रतिक्रिया समीकरणांच्या प्रतिक्रिया समीकरणांच्या ओ 2 च्या मॉलची संख्या. मूल्यांच्या काही उदाहरणे वि आणि इंधन असलेल्या स्टॉइकोमेट्रिक मिश्रणांच्या इंधनाच्या दागिन्यांची भिन्नता सारणी 1 मध्ये दर्शविली आहे.
ईंधन आणि हवेचे पूर्व-मिश्रित मिश्रण (या प्रकरणात, प्रतिक्रिया समीकरणांमध्ये एन 2 ची योग्य रक्कम जोडावी लागेल, तक्ता 1 पहा) हवा साठी समतुल्य प्रमाणानुसार दर्शविले जाते:
λ = (x डब्ल्यू / एक्स पर्वत) / (एक्स डब्ल्यू, स्टॉच / एक्स पर्वत, स्टोह) = (डब्ल्यू डब्ल्यू / डब्ल्यू पर्वत) / (डब्ल्यू डब्लू, स्टॉच / डब्ल्यू पर्वत, स्टोच)
किंवा पारंपारिक - इंधन साठी समतुल्य गुणोत्तर एफ (एफ = 1 / λ). या सूत्राचे मिश्रण मूल्याने मिश्रण असलेल्या दगडी भेदांचे प्रमाण निर्धारित करण्यात सक्षम होण्यासाठी बदलले जाऊ शकते एफ:
एक्स पर्वत = 1 / ((1+ (4,762 ∙ वी) / एफ), x डब्ल्यू = 1 - एक्स पर्वत,
एक्स वजन / 4,762, = ∙ 3,762
वी व्हॅल्यूज आणि फ्यूल फ्लेक्शन ऑफ इंधन एक्स हवेबरोबर इंधन च्या stoichiometric mixtures साठी पर्वत, stoichi
सिंचन नेहमीच रासायनिक परिवर्तनांमुळे होते. हवेतील दहन - ऑक्सिजनसह दहनशील पदार्थाचा संवाद. तथापि, हे लक्षात घ्यावे की नायट्रोजन, हेलिड्स आणि ओझोनचे ऑक्साइड दहन प्रक्रियेत ऑक्सिडायझर्स म्हणून कार्य करू शकतात. ज्ञात दहन प्रक्रिया उत्पादनाच्या केवळ एकाच स्त्रोताच्या सहभागास होत आहे - वेगवान अपघटन करण्यास सक्षम यौगिक. अशा यौगिकांचे उदाहरण म्हणजे ऍसिटिलीन आणि हायड्राझिन.
दहन दरम्यान होणार्या रासायनिक प्रक्रिया अत्यंत जटिल आहेत. सर्वात सोपा बाबतीतही - ऑक्सिजनमधील हायड्रोजनचा दहन, सामान्यीकृत समीकरण ज्याचा फॉर्म असतो
2 एच 2 + 2 2 = 2 एच 2 0,
अनेक डझन प्राथमिक चरण स्थापन आणि अभ्यास केले गेले आहेत.
आजपर्यंत, हायड्रोजन, कार्बन मोनोऑक्साइड, मिथेन आणि इथेनसारख्या काही पदार्थांच्या दहनवेळी रासायनिक बदलांचे तंत्र पुरेसे तपशील घेत आहेत. या ज्ञानाचा वापर अनेक पदार्थांच्या प्रज्वलन आणि दहनच्या परिस्थितीची पूर्तता करण्यासाठी केला जातो.
2.1. चेन प्रतिक्रिया
सामान्य रासायनिक परिवर्तनांच्या विरूद्ध चेन प्रतिक्रियांमध्ये सक्रिय कणांच्या प्रत्येक प्राथमिक क्रियामध्ये दिसून येते: अणुभट्टित इलेक्ट्रॉनसह एक परमाणु, एक मुक्त रेडिकल किंवा आयन. सक्रिय कणांचे स्वरूप प्रारंभीच्या वस्तूंच्या प्रतिक्रियेच्या उत्पादनांच्या परिवर्तनाची श्रृंखला बनवते. अणू, मुक्त रेडिकल आणि आयन व्हॅलेंस-सेटेरेटेड रेणूंपेक्षा अधिक प्रतिक्रियाशील असतात. म्हणूनच, रासायनिक बंधनांना आणि सक्रिय कणांच्या निर्मितीस आवश्यक ऊर्जा खर्च आवश्यक असला तरी, प्रतिक्रियेचे शृंखला विकास अणुभट्ट्यांमधील थेट परस्परसंवादापेक्षा ऊर्जावानरित्या अधिक फायदेशीर ठरते.
दहन प्रक्रिया प्रामुख्याने शृंखला यंत्रणाद्वारे घडतात. चेन प्रतिक्रियां - अनेक अवस्थांमध्ये होणार्या जटिल प्रतिक्रिया जे दर्शविते:
साखळी (आरंभ), ज्यामध्ये सक्रिय कण तयार होतात;
साखळीची सुरूवात, ज्यामध्ये सक्रिय कण प्रारंभ सामग्रीसह रासायनिक परस्परसंवादात प्रवेश करतात, ज्यामुळे नवीन सक्रिय कण तयार होतात;
अंतिम प्रतिक्रिया उत्पादनांच्या निर्मितीसह सक्रिय कणांची "मृत्यू" ज्या साखळ्यांचा समावेश आहे
साखळीचे मूळ विविध परिस्थितीत येऊ शकते. उदाहरणार्थ, विद्युत् डिस्चार्जमध्ये थर्मल एनर्जी किंवा आयओनीकरण किरणोत्सर्गाच्या क्रिया अंतर्गत रेणूंचे विघटन झाल्यामुळे. जेव्हा सक्रिय कण ठोस घनता (विषुववृत्त साखळी खंड) किंवा दहन अवरोधकांच्या त्यांच्या प्रतिक्रियांच्या परिणामासह परस्परसंवाद साधतात तेव्हा ते सक्रिय कणांचे पुनरुत्थान होते तेव्हा, जेव्हा ते मुक्त रेडिकलस् (समशीतोष्ण शृंखला तोडणे) संवाद करतात तेव्हा ते सक्रिय होतात.
अनबँचे आणि ब्रॅंच चेन प्रतिक्रियां आहेत. साखळीच्या सुरूवातीच्या प्रतिसादात वापरल्या जाणार्या प्रत्येक सक्रिय कणांच्या अनबंधात, पुन्हा एक उदय होत आहे. प्रति प्रारंभिक सक्रिय कण तयार केलेल्या उत्पादनांच्या रेणूंची संख्या शृंखलाची लांबी म्हटली जाते. दहन प्रक्रियेतील साखळीची लांबी शेकडो ते दहा लाखांपर्यंत आहे. नॉन-ब्रॅन्डेड चेन रिअॅक्शनचे दर पदार्थांच्या किरकोळ प्रवेशांमुळे प्रभावित होऊ शकतात जे सक्रिय कणांसारखे प्रभावीपणे कार्य करु शकतात, जसे दहन अवरोधक.
काही पदार्थ - आरंभक - सक्रिय कणांच्या निर्मितीस सुलभ करतात आणि त्यामुळे अनैच्छिक साखळी प्रतिक्रिया वाढवतात.
ब्रँडेड चेन प्रतिक्रियांमध्ये एक सक्रिय कण, साखळीच्या सातत्याने वापरली जाणारी खाणी, दोन किंवा अधिक सक्रिय कण तयार केली जातात. त्यापैकी एक प्राथमिक शृंखला सुरू ठेवते, तर इतर ब्रँकिंग तयार करुन नवीन साखळी सुरू करतात (अंजीर 2.1).
"पुनर्मूल्यांकन ही चार्ज कणांपासून तटस्थ परमाणु किंवा रेणूंच्या निर्मितीची प्रक्रिया आहे. पुनर्मूल्यांकन दरम्यान तयार झालेले परमाणु आणि रेणू जमिनीत किंवा उत्साहित अवस्थेत असू शकतात.
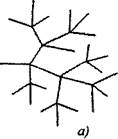
अंजीर 2.1. प्रतिक्रिया साखळीचे योजनाबद्ध प्रतिनिधित्व:
अ) शृंखलाच्या प्रत्येक दुव्यामध्ये शाखाबद्ध करणे
6) दुर्मिळ शाखा
उदाहरणार्थ, शृंखला आरंभ प्रक्रियेमध्ये हायड्रोजनच्या दहनवेळी:
एक सक्रिय परमाणु तयार होतो. साखळीच्या निरंतर प्रतिक्रिया मध्ये:

नवीन साखळीच्या सुरूवातीस सक्रिय परमाणुंच्या संख्येत वाढ झाली आहे.
ब्रान्चेड चेन प्रतिक्रिया स्थिर मोडमध्ये पुढे जाऊ शकतात, ज्यामध्ये ब्रांचिंगची गती सक्रिय कणांच्या मृत्यूच्या दरापेक्षा कमी असते आणि स्थिर नसतात, ज्यामध्ये शाखापेक्षा शाखा अधिक धीमे होते. नंतरच्या प्रकरणात, साखळीची प्रतिक्रिया वेगाने वाढते आणि केवळ प्रारंभिक सामग्रीच्या वापरामुळे मर्यादित असते. स्टेशनरीपासून नॉन-स्टँडरी मोडमधील संक्रमण अचानक होणाऱ्या प्रक्रियेच्या स्थितीत थोड्या बदलामुळे होते: तापमान, दाब किंवा reactants पैकी एकाग्रता. अशा तीव्र प्रवेगांना प्रतिक्रिया मिश्रण किंवा साखळी स्फोटाचा आत्म-इग्निशन म्हणून मानला जातो.
दहन प्रक्रियेच्या सिद्धांतासाठी ब्रंच्ड चेन रिएक्शनचे शोध महत्त्वपूर्ण होते. हे सिद्ध झाले आहे की दोन प्रकारच्या प्रज्वलन आहेत: थर्मल आणि चेन. नमुने सेट
धडा 2. रासायनिक प्रक्रिया येथे बर्निंग
साखळी प्रक्रियेचा सिद्धांत, आग दरम्यान दहन प्रक्रियांचा विकास आणि दडपण प्रभावीपणे प्रभावित करू शकतो.
साखळी मूळ.सुरुवातीच्या सक्रिय केंद्राच्या न्यूक्लियेशनची प्रक्रिया अनबंधाग्रस्त साखळी क्रियांच्या विकासात मोठी भूमिका बजावते. हे शृंखला संपुष्टात आणलेल्या क्रियांच्या दरम्यान सक्रिय केंद्राच्या नुकसानीस भरपाई देते. सक्रिय यंत्रणांच्या प्रारंभीच्या कालावधीमध्ये स्थिर शासनाच्या स्थापनेसाठी या अटी निर्धारित करतात. दीक्षा कमी दराने, हा कालावधी महत्त्वपूर्ण असू शकतो.
ज्वाळांमधील बहुतेक रासायनिक अभिक्रियांमध्ये सक्रिय केंद्राचे महत्त्वपूर्ण ऊर्जा आरक्षित असते. या परिस्थितीत, सक्रिय केंद्राची दीक्षा महत्त्वपूर्ण उर्जा अडथळावर आक्रमण करण्याशी संबद्ध आहे.
या प्रकरणात, महत्त्वपूर्ण भूमिका अशा घटकांद्वारे खेळली जाते जी सक्रिय केंद्रे उदयास येण्याचे महत्त्वपूर्ण दर निश्चित करतात: रासायनिकदृष्ट्या सक्रिय ऍडिटीव्ह, रेडिएशन, इलेक्ट्रिकल डिस्चार्ज, रेडिओएक्टिव क्षीण उत्पादने.
सक्रिय केंद्रांच्या निर्मितीस मोठ्या प्रमाणात सुविधा पुरवणार्या घटकांमधे, विषम प्रतिक्रियांची नोंद घ्यावी. ज्वलनशील पदार्थांवर घन पदार्थांच्या अणूंच्या अणूंमध्ये, इंटरटॉमिक बाँड कमकुवत होतात आणि त्यांच्या ब्रेकिंगला कमी ऊर्जा खर्च आवश्यक असतो. या परिस्थितीत, सक्रिय केंद्राची निर्मिती दर गॅसच्या प्रमाणापेक्षा लक्षणीय आहे. दहनशील मिश्रणाच्या घटकांच्या विषम परस्परसंवादातील सक्रियता उर्जा देखील एकसमान परिस्थितीपेक्षा कमी असते. प्रत्यक्ष दहन प्रक्रियेच्या स्थितीत सक्रिय केंद्राच्या भेदक दीक्षा अखंडित शृंखला प्रक्रियेसह स्थिर शासनाच्या त्वरित उपलब्धतेमध्ये एक महत्त्वपूर्ण घटक आहे.
काही वैशिष्ट्ये ऍटोमिक घटकांच्या सहभागाने उद्भवलेल्या अनैच्छिक साखळी प्रतिक्रिया दर्शवतात. पुनरुत्पादनाशिवाय सक्रिय केंद्राशी संवाद साधण्याच्या अशुद्धतेच्या अनुपस्थितीत, जेव्हा परमाणु ट्रायबल टक्कर आणि पृष्ठभागावर अणुंचे पुनरुत्थान होते तेव्हाच शृंखला संपुष्टात येते.
कोणत्याही तपमानावर, सर्व वायू पदार्थ अंशतः विलग होतात. काही रेणू अणूंचा नाश करतात. या प्रकरणात, विच्छेदनाची प्रक्रिया आणि अणूंचे अणूंचे मिश्रण यांच्यातील एक समतोल आहे. विघटन पदवी वेगाने तापमानावर अवलंबून असते.
ज्वलनशील मिश्रणात कोणतेही दोष नसल्यास साखळी तोडल्यास, प्रतिक्रियेच्या परमाणु घटकांची सघनता प्रत्यक्षरित्या अपरिवर्तित राहते. प्रतिक्रिया मध्ये आणलेले परमाणु ताबडतोब त्याचं पुनरुत्पादन करतात
कोरोलचेन्को ए. य. दहन आणि स्फोट प्रक्रिया
लिची प्रारंभीची दीक्षा अणु-विरोधी प्रणालीसारख्या प्रमाणात समान प्रतिक्रिया असलेल्या अणूंची पूर्तता करते. स्थिर प्रतिक्रिया या प्रक्रियेस प्रभावित करत नाही. रेणूच्या घटकांपैकी एक शिल्लक अणूतील अणूंच्या दरम्यान कमीतकमी मजबूत बंधनाद्वारे ओळखले जाते, ही या वैशिष्ट्याची वैशिष्ट्यपूर्ण वैशिष्ट्य आहे. या प्रकरणात इतर परमाणु घटकांचे एकाग्रता हे क्वासिस्टेशनरी आहे, परंतु अधिक समतोल आहे.
दहन प्रतिक्रियांच्या एकसमान दीक्षा सह, स्थिर शासन निश्चित कालावधीनंतरच स्थापित केले जाईल, कारण विलग करण्यासाठी मोठ्या सक्रियतेची ऊर्जा आवश्यक असते. या कालावधी दरम्यान, विघटन दर पुनर्संयोजन दरापेक्षा जास्त आहे आणि सक्रिय केंद्रे प्रतिक्रिया प्रणालीमध्ये एकत्र होतात. सक्रिय केंद्राच्या एकाग्रतेत संतुलन वाढविल्यानंतर दोन्ही प्रक्रियेची दर केवळ तुलना केली जाते. या कालावधीला प्रेरण कालावधी म्हणतात.
प्रतिक्रिया क्षेत्रातील उत्प्रेरक म्हणून घन पृष्ठभागाची उपस्थिती थर्मोडायनेमिक समतोल स्थिती बदलत नाही. उत्प्रेरक अग्रेसर आणि उलट प्रतिक्रियांवर तितकेच प्रभावित करते. सक्रिय केंद्रे केवळ घन पृष्ठभागावरुन उद्भवतातच असे नाही तर त्यावरील विघटन देखील करतात. तथापि, उत्प्रेरकांची उपस्थिती समतोल पृथक्करण स्थितीची उपलब्धि वाढवते.
ज्वलनशील मिश्रणमध्ये सक्रिय पदार्थ उपस्थित असल्यास, जो शृंखला ब्रेकेज प्रतिक्रियांमध्ये भाग घेण्यास सक्षम असतात, ते सक्रिय केंद्राच्या एकाग्रतेस कमी करतात. या प्रकरणात, आरंभिक घटकांपैकी एक समतोल विघटन विचलित झाला आहे, जो प्रतिक्रिया कमी करते आणि त्याचे निरसन होऊ शकते.
प्रयोगाने दर्शविले आहे की बाहेरील स्त्रोताद्वारे (उदाहरणार्थ, एक प्रकाश स्रोत) अनबंधाग्रस्त साखळीची प्रतिक्रिया सुरू करताना दहन प्रक्रियेच्या विकासाच्या सुरुवातीच्या चरणात सक्रिय केंद्राचे एकाग्रता लक्षणीय समतोलापेक्षा मोठी असू शकते.
ब्रंच केलेल्या साखळी प्रतिक्रिया दरम्यान, प्रारंभीच्या प्रारंभीच्या परिस्थितीचा प्रतिक्रियेच्या विकासावर मोठा प्रभाव पडतो. मंद-चालणार्या प्रक्रियेमध्ये, आरंभिक एक आंशिक प्रतिक्रिया असलेल्या मिश्रणाचा समावेश प्रेरण कालावधी कमी करते आणि ज्वाला दहनच्या क्षणाला गतिमान करते.
साखळीची सुरूवातअखंडित साखळी क्रियांची वैशिष्ट्यपूर्ण वैशिष्ट्य सक्रिय केंद्राच्या एकाग्रतेची अर्ध-स्थिरता आहे. ओपन सर्किटच्या अनुपस्थितीत, सक्रिय कण तयार होतात
धडा 2. दहन दरम्यान रासायनिक प्रक्रिया
ते ज्या प्रमाणात खर्च केले जातात त्याच प्रमाणात. नवीन प्रारंभिक प्रारंभीच उद्भवतो. सक्रिय केंद्राच्या निर्मितीच्या समान दर आणि शृंखला संपुष्टात येण्यासह, सक्रिय केंद्रांचे स्थिर एकाग्रता आणि स्थिर प्रतिक्रिया मोड स्थापित केले जातात. आरंभिक घटकांचा वापर केल्याने प्रतिक्रिया दर कमी होईल.
ब्रंच्ड चेन प्रतिक्रियेच्या बाबतीत, प्रतिक्रियेच्या प्रक्रियेतील सक्रिय केंद्रांचे प्रमाण त्यांच्या प्रारंभिक कार्याच्या अटींच्या पर्वा न करता वाढते. स्व-प्रवेगक प्रतिक्रिया मोड कार्यान्वित केला आहे, ज्यामध्ये हिमवर्षाव वर्ण आहे. या प्रकरणात, प्रारंभीच्या घटकाची संपूर्ण प्रतिक्रियांमध्ये प्रतिक्रियेच्या अंतिम उत्पादनांमध्ये एक प्रारंभिक सक्रिय केंद्र पुरेसे आहे.
खालीलप्रमाणे ब्रान्न्शियल मूल्यवान प्रतिक्रियाचे किनेटिक समीकरण आहे. कालांतराने स्थिर प्रारंभ होणार्या घटकाच्या संसर्गातील बदल प्रथम अंदाजापेक्षा दुर्लक्षित केला जाऊ शकतो आणि सक्रिय केंद्राच्या एकाग्रतेत फक्त वेगवान बदल लक्षात घेता येऊ शकतात. पी.या वेगाने केलेले बदल प्रारंभिक दीक्षा दर आणि शाखा आणि शृंखला संपुष्टात येणार्या प्रतिक्रियांच्या दरांचे प्रमाण निर्धारित करतात. प्रारंभिक आरंभिक दर प्रणालीमध्ये उपस्थित असलेल्या सक्रिय केंद्राच्या एकाग्रतेवर अवलंबून नाही. शाखा आणि ब्रेकिंग प्रक्रियेची दर सक्रिय केंद्राच्या सांद्रतेच्या प्रमाणात आनुपातिक असतात. या परिस्थितीत, सक्रिय केंद्राच्या निर्मिती आणि खर्चाची संपूर्ण शिल्लक दीक्षा, शाखा, आणि खंडणीच्या प्रक्रियेच्या दराच्या बेरजेनुसार निर्धारित केली जाते:
![]() (2.1)
(2.1)
शाखा आणि ब्रेकिंग प्रतिक्रियांची दर स्थिर आणि कोठे आहेत. नाकारणे, आम्हाला मिळते:
![]() (2.2)
(2.2)
सक्रिय केंद्राच्या एकाग्रतेची व्युत्पन्न वेळ
सकारात्मक आहे. प्रतिक्रिया दर वेळ वाढते. ब्रंच्ड चेन रिऍक्शनचे हे वैशिष्ट्य अशा शाळांमध्ये सक्रिय केंद्राच्या गुणामुळे झाले आहे जेव्हा ब्रॅंचिंग रिअॅक्शनचा दर शृंखला संपुष्टात येण्याच्या प्रक्रियेच्या दरापेक्षा अधिक आहे.
कोरोलचेन्को ए. य. दहन आणि स्फोट प्रक्रिया
प्रतिक्रिया प्रारंभाच्या आधी सिस्टममध्ये सक्रिय केंद्र नसतात, म्हणजे येथेटी= 0, एन = 0 समीकरण (2.2) एकत्रीकरण देते:
![]() (2.3)
(2.3)
सीओची एकूण प्रतिक्रिया दर शाखा प्रक्रियेच्या दराने निर्धारित केली जाते. अंतिम उत्पादनांची प्रतिक्रिया या प्रक्रियेदरम्यान केली जाते. प्रत्येक प्राथमिक शृंखला ब्रांचिंग कार्यक्रमासाठी, अंतिम उत्पादनाचे रेणू तयार केले जातात. हे खालीलप्रमाणे आहे:
![]() (2.4)
(2.4)
वेळेत साखळीच्या प्रतिक्रिया विकासाची शाखा आणि साखळीच्या समाप्त होण्याच्या प्रतिक्रियांच्या दर स्थिरतेच्या प्रमाणात निर्धारित केली जाते आणि जेव्हा समीकरणातील एक्सपोनेंट (2.4) सकारात्मक आणि पुन्हा-
क्रिया अमर्यादित वेगवान आहे. प्रतिक्रिया विकासाच्या सुरुवातीच्या काळात खालील संबंध खरे आहेत:
प्रारंभिक आरंभिक दराचा दर लहान असल्यामुळे, प्रारंभिक कालावधीत लक्षणीय रासायनिक परिवर्तन नाही. काही काळानंतर, मूल्य एकापेक्षा जास्त मोठे होते. त्यानंतर, समीकरण (2.4) नुसार प्रतिक्रिया दर वेगाने वाढू लागते आणि खूप मोठी मूल्ये गाठते, जरी तो आधी प्रत्यक्षात अयोग्य होता.
साखळीच्या प्रतिक्रियेच्या प्रक्रियेदरम्यान विलंब कालावधी (प्रेरण कालावधी) ची उपस्थिती प्रतिक्रिया प्रक्रियेत सक्रिय केंद्रे निश्चित संख्या जमा करण्याच्या आवश्यकतेमुळे आहे. या रासायनिक परिवर्तनानंतर केवळ लक्षात येईल.
साखळीच्या प्रतिक्रियांमधील प्रेरण कालावधीची परिमाण ब्रांचिंग आणि शृंखला संपुष्टात येण्याच्या प्रक्रियेचे प्रमाण ठरवते, प्रारंभिक दीक्षा दर नाही. परिणामी, ब्रॅकिंग आणि ब्रेकज रिअॅक्शनचे दर प्रत्येक प्रतिक्रिया प्रक्रियेच्या रासायनिक वैशिष्ट्यांमुळे आहेत; ते अवलंबनांवर अवलंबून असतात आणि प्रारंभिक घटकांच्या सांद्रतेवर अवलंबून असतात. चेन प्रतिक्रियांचे वैशिष्ट्य
ब्रांचिंग प्रक्रियांमध्ये महत्त्वपूर्ण सक्रियकरण उर्जेची आवश्यकता असते, परंतु ब्रेक प्रक्रिया प्रक्रियेचे तापमान गुणांक शून्य असेल. सर्व तीन प्रकारांच्या साखळीच्या संपुष्टात येण्याच्या प्रतिक्रियांमध्ये: मोठ्या आणि विषम रीकोम्बिनेशनच्या बाबतीत, सक्रिय अशुद्ध असणा-या रेडिकल्सच्या परस्परसंवादामध्ये सक्रियकरण ऊर्जा शून्य असते.
तपमान वाढणे, मिश्रणांचे एकूण दाब किंवा प्रतिक्रिया घटकांच्या एकाग्रतामध्ये बदल होणे, शाखा आणि ब्रेकिंगचे प्रमाण स्थिर होणे हे बदल शक्य आहे, ज्यामुळे प्रतिक्रिया स्थिर ते स्थिर न होण्यास बदलते. या प्रक्रियेची खासियत एका मोडपासून दुसऱ्या मार्गावर अचानक बदलत आहे, परिणामी नगण्य मूल्यापासून प्रतिक्रिया वाढवून अमर्यादित वाढते.
काही साखळी क्रियांच्या प्रवाहासह मध्यवर्ती उत्पादनांची निर्मिती करणे तुलनेने स्थिर असते परंतु सक्रिय केंद्रे तयार करण्याची क्षमता असते. अशा प्रतिक्रियांमध्ये उदाहरणार्थ, हायड्रोकार्बन दहन प्रतिक्रिया, मध्यवर्ती भागांमध्ये पेरोक्साईड्स आणि अॅल्डेहायड्स तयार होतात. हे साखळी branching ठरतो. तथापि, मध्यवर्ती उत्पादनांची सापेक्ष स्थिरता असल्यामुळे, प्रतिक्रिया त्वरेने वाढते. अशा मंद ब्रांचिंग चेनला डीजेनेरेट म्हणतात.
रेडिकलच्या उच्च क्रियाकलापांमुळे, नियम म्हणून सामान्य रेडिकल ब्रांचिंग यंत्रणा सह साखळी प्रतिक्रिया, त्वरीत पुढे जा. परिणामी रेडिकल एकतर वेगवान प्रवेगक प्रतिक्रिया देतात किंवा प्रक्रिया पुन्हा करतात आणि प्रक्रियेतून बाहेर पडतात.
ओपन सर्किट कोणताही वायू रेणू सारख्या सक्रिय कण, प्रतिक्रिया प्रक्रियेमध्ये यादृच्छिक हालचाल करतो आणि इतर रेणूंसह टक्कर मारतो. त्याच वेळी, दुसर्या सक्रिय कण किंवा रेणूबरोबर परस्परसंवादाच्या काही टप्प्यावर आणि मागील सक्रिय मार्गाच्या सुरूवातीस नवीन सक्रिय कण तयार होण्याची शक्यता निश्चित आहे. प्रतिक्रिया श्रृंखलेचे विकास अक्रिय अणूंच्या ब्राउनीयन हालचालीसारखेच आहे, तथापि सक्रिय केंद्रांचे हस्तांतरण रासायनिक प्रतिक्रियासह केले जाते. शृंखलांच्या विकासाच्या मार्गावर दोन किंवा त्यापेक्षा जास्त प्रकारच्या वैकल्पिक सक्रिय केंद्रांवर.
कोरोलचेन्को ए. य. दहन आणि स्फोट प्रक्रिया
प्रतिक्रियांची श्रृंखला सतत चालू होते जेव्हा सक्रिय कण पुनर्जन्म न घेता प्रतिक्रिया देत नाही. या प्रकरणात, तथाकथित ओपन सर्किट आढळते. ब्रेनज प्रोसेस चेन रिएक्शनच्या किनेटिक्समध्ये मोठी भूमिका बजावते. सक्रिय केंद्राच्या मृत्यूस कारणीभूत असे दोन प्रकारचे परिणाम आहेत:
एकसमान ब्रेक (प्रतिक्रिया मिश्रण च्या खंड मध्ये मृत्यू);
विषाणूजन्य ब्रेक (सॉलिड पृष्ठभागावर मृत्यू) दोन प्रक्रियांपैकी एकच्या सहाय्याने समवयस्कांचे ब्रेक होणे शक्य आहे:
जेव्हा रेडिकल रीकॉम्बाइन करतात किंवा जेव्हा विभिन्न रासायनिक सक्रिय घटक त्यानंतरच्या पुनर्जन्माशिवाय सक्रिय केंद्राशी संवाद साधतात.
दहन दरम्यान तयार होणा-या सूक्ष्म कणांवर किंवा घनदाट बर्निंगच्या पृष्ठभागावर हेट्रोजेनेझस चेन ब्रेकेज उद्भवते. घन पृष्ठभागावर खुले सर्किटला गॅस मिश्रणपासून ते ज्या पृष्ठभागावरून गायब होतात अशा सक्रिय केंद्राच्या प्रसारांमुळे प्रसारित केले जाऊ शकते. सघन पृष्ठभागावर पुनर्संयंत्रणाची प्रक्रिया अशी आहे की सक्रिय कण ज्यामध्ये वाढीव प्रतिक्रिया वाढली आहे, त्या पृष्ठभागावर सोरड * आहे. या प्रक्रियेसाठी उर्जा आणि स्थानिक अडथळे नसल्यामुळे, समीपस्थ साइट्सवर चक्रीवादळ करणारे रेडिकल एकमेकांना पुन्हा जोडतात. रीकॉम्बिनेशनच्या परिणामस्वरूप तयार केलेल्या स्थिर यौगिकांचे रेणू यापुढे साखळीच्या प्रतिक्रियांच्या विकासात सहभागी होत नाहीत.
तथापि, सॉलिड पृष्ठासह सक्रिय कणांच्या प्रत्येक टक्करमुळे त्याचे शोषण होऊ शकत नाही. कदाचित पृष्ठभागावरून त्याचे प्रतिबिंब. सॉलिड पृष्ठाद्वारे सक्रिय केंद्राच्या शोषणांची संभाव्यता निवास गुणांक म्हणून ओळखली जाते. हे गुणांक सक्रिय कण आणि पृष्ठभागाच्या रासायनिक संबंधांची एक वैशिष्ट्य आहे. व्यावहारिकदृष्ट्या महत्त्वपूर्ण प्रकरणांमध्ये, भिंतीवरील प्रतिबिंबानंतर सक्रिय कण दूरपासून दूर जात नाही. त्याच्या निवासस्थानी येईपर्यंत भिंतीसह नवीन टकरावांची शक्यता आहे. या प्रक्रियेमुळे, विशिष्ट परिस्थितींत, प्रतिक्रिया दर निवास गुणांकांपासून प्रत्यक्षपणे स्वतंत्र असते. प्रक्रिया ईयू म्हणून अशा प्रकारे मिळते
* सॉर्पशन - वातावरणातील पदार्थ हेक्टरच्या घन शरीरात (किंवा द्रव) शोषून घेणे. शोषक शरीरांना शोभेस म्हटले जाते- sorbate. सोरबेंट (अवशोषण) आणि पृष्ठभागाचे (शोषण) संपूर्ण वस्तुमान शोषण वेगळे करा. सॉलिड सोरबेंट आणि सॉर्बेटच्या पृष्ठभागाच्या दरम्यान रासायनिक प्रकाराच्या परस्परसंवादामुळे सांसशन कोमोसोर्शन म्हणतात.
__________________________ धडा 2. दहन दरम्यान रासायनिक प्रक्रिया
प्रत्येक टकराव वर एक खुला सर्किट आली तर. पृष्ठभागावर सक्रिय केंद्रे एकाग्रता शून्य असू शकतात.
प्रतिक्रियायुक्त मिश्रणांमध्ये सक्रिय अशुद्धता नसल्यास, साखळीचे तुटणे एकतर ठोस घन किंवा एकसमानपणे मोठ्या प्रमाणात रेडिकल्सच्या पुनर्संरचनाद्वारे येऊ शकते. वास्तविक आग मध्ये, दुसरा मार्ग प्रामुख्याने लागू केला जातो.
साखळी प्रतिक्रियांच्या गतिशीलतेवर काही प्रभाव जड वायूंच्या प्रतिक्रिया प्रक्रियेत समावेश करतात. आर्ट ऍडिटीव्ह सक्रिय कणांसह टक्करांची संख्या वाढवतात, साखळी तोडण्याची शक्यता वाढवते आणि त्यानुसार, संपूर्ण प्रतिक्रिया प्रतिबंधित करते.
प्रतिक्रिया प्रक्रियेमध्ये प्रतिक्रियाशील ऍडिटिव्ह्ज-इनहिबिटरच्या परिचयाने साखळी क्रियांची अधिक प्रभावी प्रतिबंध. अवरोधक शृंखला तोडण्यासाठी, प्रतिक्रिया अग्रगण्य, सक्रिय केंद्रे संवाद. व्यस्त केंद्रामध्ये परस्परसंवादाच्या प्रक्रियेची गतिशीलता नियंत्रकांमधील प्रतिस्पर्धाची स्थिती आणि सक्रिय केंद्राशी संवाद साधताना प्रतिक्रियांचे मुख्य भाग ठरवते. अवरोधकांच्या उच्च क्षमतेसह आणि नवीन सक्रिय केंद्राच्या निर्मितीच्या मध्यम दरामुळे, प्रतिबंधकांचे आधीपासूनच छोटे अॅड्रिव्हिव्ह चेन रिअॅक्शनचा कोर्स पूर्णपणे दाबू शकतात.
आग आणि स्फोटक सुरक्षेच्या प्रक्रियेत प्रतिबंधनाची प्रक्रिया महत्त्वपूर्ण आहे. इनहिबिटरचा वापर प्रभावीपणे दहन प्रक्रियांवर प्रभाव पाडण्यास आपल्याला परवानगी देतो.
2.2. हायड्रोजन च्या दहन दरम्यान रासायनिक प्रक्रिया
ऑक्सिजन रेणूसह हायड्रोजन रेणूचा परस्पर क्रिया सतत टप्प्यांत एक जटिल मार्गाने होतो. आता हे दृढपणे स्थापित केले गेले आहे की हायड्रोजनचा दहन एका शृंखला यंत्रणाद्वारे होतो, कण सक्रिय केंद्राची भूमिका बजावतात. हायड्रोजनच्या दहनवेळी प्राथमिक प्रतिक्रियांचे अनुक्रम आणि महत्त्व हायड्रोजनच्या ज्वालांच्या उदय आणि विकासासाठी विविध परिस्थितींसाठी मोठ्या प्रमाणात वर्णन केले आहे.
प्रायोगिक आणि संगणकीय पद्धतींचा वापर करून ऑटोग्निशन मोडमध्ये हायड्रोजन दहन प्रक्रियेचा सर्वात विस्तृत विश्लेषण प्राध्यापक ए. एन. बारातोव्ह यांनी केला. त्यांनी 14 मूलभूत प्राथमिक प्रतिक्रियांसह प्रक्रियेच्या खालील योजनेचा प्रस्ताव ठेवला.
कोरोलचेन्को ए. य. दहन आणि स्फोट प्रक्रिया
सक्रिय केंद्राची उत्पत्ती प्रतिक्रिया द्वारे होते
![]()
प्रतिक्रियांच्या साखळीची सुरूवात
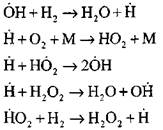
शाखा साखळी
 |
ओपन सर्किट
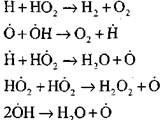 |
ऑटोगिनिशन प्रक्रियेच्या प्रारंभिक अवस्थेमध्ये हायड्रोजन अणूंचे प्रमाण प्रारंभिक हायड्रोजन सामग्रीचा एक महत्त्वाचा भाग आहे. साखळीच्या प्रतिक्रियेमुळे, आण्विक हायड्रोजनचे रूपांतरण इतके उच्च होते की ते सेकंदाच्या शंभर मध्ये वापरले जाते.
2.3. कार्बन मोनोऑक्साइड बर्न करताना रासायनिक प्रतिक्रिया
ऑक्सिजनसह कार्बन मोनोऑक्साइडचा संवाद दहन प्रक्रियांसाठी एक प्रमुख प्रतिक्रिया आहे. दरम्यान या प्रतिक्रिया कोर्स
__________________________ धडा 2. रासायनिक प्रक्रियाजळत आहे
बर्याच प्रकरणात कार्बन-युक्त पदार्थांचे दहन करण्याचे नियम ठरवतात. प्रतिक्रिया एक ब्रँंच चेन यंत्रणा द्वारे दर्शविले जाते. यात अनेक वैशिष्ट्ये आहेत.
बर्याच काळापासून सीओ आणि 0 चे पूर्णपणे सूक्ष्म मिश्रण प्रज्वलित आणि बर्न करू शकले नाही असा विश्वास होता. तथापि, द्रव्य मिश्रणाने वापरल्या जाणार्या पाण्याच्या अनुपस्थितीवर लक्षपूर्वक निरीक्षण करा जेणेकरुन कोरड्या मिश्रणाने इग्निशन देखील शक्य होईल. हे लक्षात घेतले पाहिजे की सीओ +0 2 पाणी वाष्प किंवा हाइड्रोजन प्रणालीतील विद्युत् सक्रिय क्रियांची संख्या वाढवून इग्निशन आणि दहन प्रक्रियेस सक्रिय करते. पाण्याचा वेग वाढणे कमी सांद्रतेवर विशेषतः लक्षणीय आहे.
जल वाष्प किंवा हायड्रोजनच्या लहान जोडीच्या उपस्थितीत कार्बन मोनोऑक्साइडचा दहन खालील प्राथमिक प्रक्रियेच्या सहभागासह होतो:

रेडिकल, H0 2, जे प्रतिक्रियेद्वारे (6) तयार केले गेले आहे, चेन (प्रतिक्रीया VIII) चालू ठेवू शकतात किंवा प्रतिक्रियेने (9 -12) त्याच्या खंडित होऊ शकतात.
साखळी स्फोटात सीओच्या मंद ऑक्सिडेशनच्या संक्रमणासाठी असलेल्या परिस्थितीचे आकलन करण्यासाठी, रेडिकल एच 0 2 च्या माध्यमातून शृंखला ब्रेकची संभाव्यता आपण अनुमानित करूया; येथे आपण लक्षात घेतो की शृंखला संपुष्टात येणार्या प्रतिक्रिया (एक्स) आणि (XI) ची भूमिका महत्त्वपूर्ण असेल
प्रतिक्रिया (आयएक्स) च्या तुलनेत, 1000 के के ऑर्डरच्या तापमानात (IX-XI) प्रक्रियेच्या दर स्थिरांक एकमेकांच्या जवळ आहेत, परंतु रेडिकलचा उच्च रासायनिक क्रियाकलाप असल्याने, रेडिकलचे प्रमाण हायड्रोजन अणूंच्या एकाग्रतेपेक्षा बरेच कमी आहे. म्हणून, रेडिकल एच0 2 द्वारे ओपन सर्किटची संभाव्यता ही स्वरूपात लिहिली जाऊ शकते:
1000 के तापमानावर
म्हणून, प्रदान केले
![]()
![]()
परिमाण प्रभाव
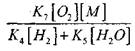
समीकरण निराकरण (2.7) कमकुवत होईल.
धडा 2. दहन दरम्यान रासायनिक प्रक्रिया
बाबतीत ![]() किंवा
किंवा ![]() (काय मनाई आहे
(काय मनाई आहे
वास्तविक फ्लेम), समीकरण (2.7) फॉर्ममध्ये रूपांतरित केले आहे:
![]() (2.8)
(2.8)
अशा प्रकारे, हवेमध्ये कार्बन मोनोऑक्साइड बर्न करण्याची स्थिती मुख्यत्वे हायड्रोजन बर्निंगची उपस्थिती आणि नमुने द्वारे निर्धारित केली जाते. प्रतिक्रिया द्वारे सीओचे ऑक्सीकरण (I) हायड्रोजनसह होणाऱ्या प्रतिक्रियांमध्ये तयार केलेल्या ओएच रेडिकलच्या एकाग्रतेवर अवलंबून असते.
कार्बन मोनोऑक्साईडच्या दहन प्रक्रियेची विशिष्टता त्याच्या वेगवान अवरोधात असते जेव्हा हायड्रोजन अणूंसाठी उच्च संबंध असलेल्या द्रव पदार्थांच्या प्रतिक्रियाशील प्रक्रियेमध्ये लहान पदार्थांचा समावेश केला जातो. सीओच्या दहनमध्ये अडथळा आणणारे पदार्थ हायड्रोकार्बन्सचे हॅलाइड आणि हेलो-डेरिव्हेटिव्स असतात. प्रतिक्रियेद्वारे हायड्रोजन अणूंशी संवाद साधताना प्रतिक्रिया साखळीची समाप्ती झाल्यामुळे त्यांचा आघातविषयक प्रभाव
2.4. हायड्रोकार्बन बर्निंग
हायड्रोजन आणि कार्बन मोनोऑक्साइडच्या दहन प्रक्रियेची तपासणी दहन प्रतिक्रिया प्रक्रियाची जटिलता दर्शवते. एच 2 आणि सीओच्या बाबतीत, प्रतिक्रिया अनेक प्राथमिक टप्प्या आणि मध्यवर्ती उत्पादनांच्या सहभागाने शृंखला म्हणून मिळते. म्हणूनच, अधिक जटिल पदार्थांच्या दहन प्रतिक्रियांची प्रक्रिया - हायड्रोकार्बन्स - या यौगिकांच्या इग्निशन आणि दहन प्रक्रियेच्या प्रक्रियेसह प्रभाव अधिक विविध आहेत याची अपेक्षा करणे नैसर्गिक आहे.
हायड्रोकार्बन्सच्या रासायनिक उन्नतीच्या स्वरूपावरील सध्या उपलब्ध माहिती त्यांच्या दहन प्रक्रियेत आम्हाला काही अंदाजासह सापेक्ष प्रभावांची व्याख्या करण्यास अनुमती देते.
हे सिद्ध झाले की हायड्रोकार्बनच्या ज्वालांमध्ये, आधीपासूनच ज्ञात सक्रिय कणांसह, अधिक जटिल संरचनांच्या मध्यवर्ती उत्पादनांची संख्या आहे. काही बाबतीत, ते नवीन साखळीच्या उदयांच्या स्त्रोता बनतात. हायड्रोकार्बन्सचे इग्निशन आणि दहन प्रक्रियेत मुख्य भूमिका खालील प्रकारच्या मध्यवर्ती संयुगेद्वारे खेळली जाते:
कोरोलचेन्को ए. य. दहन आणि स्फोट प्रक्रिया
1. हायड्रोकार्बन रेडिकल, ज्याचा रेणू आहे
लेवोडोरोडा, ज्याने एक किंवा अधिक हायड्रोजन अणू काढले. हे
अवशेषांना अल्किल म्हणतात (सीएच 3 - मिथाइल; सी 2 एच 5 - एथिल; सी 3 एच 7 - प्रोपिल आणि
वगैरे). त्याच्या उच्च प्रतिक्रियाशीलता, मुक्त alkyls कारण
बर्याच काळासाठी अस्तित्वात नाही. मध्यवर्ती म्हणून flames उपस्थित
उत्पादने इतर अणुभ्रंशांशी संवाद साधताना वागतात
एक स्वतंत्र संरचनात्मक गट म्हणून. हायड्रोकार्बन रेडिकल
सहसा अक्षर आर प्रतिनिधित्व.
2. पेरोक्साइड्स - सामान्य फॉर्मूला आर -00-आरचे मिश्रण ".
3. आल्डेहायड्स - प्रकार कंपाऊंड्स
![]()
सर्वात सोपा अल्डेहायड्स फॉर्मिक (फॉर्मेल्डेहायडे) आणि एसिटिक (एसीटाल्डेहायड) आहेत. ![]() . हे पदार्थ सर्व आहेत
. हे पदार्थ सर्व आहेत
हायड्रोकार्बन्स अपूर्ण दहन उत्पादनांमध्ये उपस्थित आहे.
हायड्रोकार्बन्सच्या दहन दरम्यान चेन निर्मिती कोणत्याही प्रतिक्रिया असू शकते ज्यामध्ये हायड्रोकार्बन रेडिकल तयार होतात. इथॅन रेणूची दोन मुक्त मिथाइल गटांच्या निर्मितीसह ही एक अपघटन प्रतिक्रिया असू शकते:
![]()
किंवा ऑक्सिजनसह हायड्रोकार्बनची प्रतिक्रिया:
![]()
साखळीची सुरूवात निर्मिती प्रतिक्रियांच्या परिणामस्वरूप होते पेरोक्साइड किंवा हायड्रोपेरॉक्साइड:
![]()
हायड्रोपेरॉक्साईडच्या विघटनानंतर चेनिंग शाखा सुरू केली जाते:
धडा 2. दहन दरम्यान रासायनिक प्रक्रिया
प्रतिक्रियेच्या दिलेल्या क्रमाने प्रतिक्रिया प्रक्रियेतील पेरोक्साइड संयुगेच्या एकाग्रतेमध्ये हळूहळू वाढ झाली आहे.
एकाच वेळी पेरोक्साइड्स, रेडिकल आणि प्रारंभीच्या संचयनासह
समांतर प्रतिक्रिया आहेत:

ही प्रतिक्रिया एक्स्ट्रोथिक आहे; जेव्हा ते मोठ्या प्रमाणात उष्णता वाहतात.
प्रतिक्रिया मिश्रण तापमानात वाढ झाल्यामुळे, सक्रिय केंद्रांची भूमिका एका मध्यवर्ती उत्पादनाच्या दुसर्या क्रमाने पुढील क्रमाने पास केली जाते: अॅल्केल हायड्रोपिरोक्साइड, एसील हायड्रोपिरोक्साईड्स, फॉर्मेल्डेहायडेस.
उच्च तपमान क्षेत्रात (600-800 डिग्री सेल्सिअस) वेळोवेळी प्रतिक्रिया मिश्रण तयार करण्याच्या प्रायोगिक अभ्यासातून असे दिसून येते की प्रारंभिक हायड्रोकार्बनचे अंतिम दहन उत्पादनांमध्ये रुपांतर करण्याची प्रक्रिया दोन अवस्थांमध्ये विभागली गेली आहे: प्रथम, अतिशय उच्च दराने उद्भवणारी, हायड्रोकार्बन सीओला ऑक्सिडिझिझ करते. दुस-या, मंद, अवस्थेत, सीओ ऑक्सिडायझेशन केले जाते. एक अत्यंत महत्त्वाचा निष्कर्ष खालीलप्रमाणे आहे: हायड्रोकार्बन्सचे दहन करण्याचे अनेक नियम कार्बन मोनोऑक्साईडच्या दहनाने स्पष्ट केले जाऊ शकतात.
2.5. कार्बन बर्निंग
कार्बन बर्निंग एक वेगळ्या प्रक्रियेच्या पद्धतीनुसार मिळते, याची विशिष्टता म्हणजे आसपासच्या जागेपासून गॅस ऑक्सिडंट (हवेचा ऑक्सिजन) हस्तांतरित करण्याच्या प्रक्रियेपासून ज्वलनशील घनतेच्या पृष्ठभागावर हस्तांतरित करण्याच्या प्रक्रियेपासून रासायनिक अवस्थेचा विलग मानला जाऊ शकत नाही. बर्निंग रेट कार्बनच्या रासायनिक गुणधर्मांवर आणि इंधन पृष्ठभागावर ऑक्सिजन पुरवण्याची प्रक्रिया निर्धारित करणार्या वैशिष्ट्यांवर अवलंबून असते. दहन क्षेत्राला ऑक्सिजन पुरवठा प्रसार आणि म्हणूनच केला जातो
कोरोलचेन्को ए. य. दहन आणि स्फोट प्रक्रिया
बर्याच घटकांवर अवलंबून असते: बर्निंग बॉडीचे आकार आणि आकार, वायूमागचे हालचाल, ऑक्सिजनचे प्रसार गुणांक आणि इंधन पृष्ठभागावरील जागा आणि कोळशाचे आणि कोकमध्ये मोठ्या प्रमाणातील क्रॅक आणि छिद्रांमध्ये प्रतिक्रियांचे उत्पादन.
विषम कार्बन बर्निंगच्या वैशिष्ट्यांचे वर्णन करण्यासाठी आम्ही भट्टीत ठेवल्या जाणार्या कोळशाच्या वेगळ्या कोळशाचे 9 00 डिग्री सेल्सियस तपमान मानतो. सुरुवातीच्या काळात कोळशाचे दहन त्याच्या पृष्ठभागाजवळ असलेल्या ऑक्सिजनच्या खर्चावर होईल. त्याचा वापर केल्यावर, दहन उत्पादनांचा एक थर गरम पृष्ठभागाच्या जवळ बनतो. बर्निंग रेट कमी होईल आणि गॅस स्पेसच्या दूरच्या भागातील ऑक्सिजन नसल्यास प्रक्रिया थांबू शकते.
हा प्रवाह प्रसारणाद्वारे होतो आणि बर्निंग रेट प्रसारणाद्वारे निश्चित केला जाईल. प्रसरण तीव्रता प्रामुख्याने जळणार्या पृष्ठभागाजवळ गॅस माध्यमाच्या हालचालीच्या तीव्रतेवर आणि निसर्गवर अवलंबून असते. रासायनिक प्रतिक्रिया दर प्रामुख्याने तापमानात निर्धारित केले जाते. विषाणूजन्य प्रतिक्रिया तसेच समशीतोष्ण, अरे-नीयस नियमांचे पालन करा.
उच्च तापमानात कार्बनची ऑक्सिडेशनची प्रतिक्रिया त्वरेने मिळते आणि प्रक्रियेची एकूण गती ऑक्सिजनच्या पृष्ठभागावर पसरवून मर्यादित असेल.
अशाप्रकारे, कार्बन बर्ण करण्याच्या प्रक्रियेत वेगवेगळ्या प्रकारची दोन प्रक्रिया असतात: वायूच्या ऑक्सिजनला गॅसच्या स्थानापासून त्याच्या जागी स्थानांतरित करण्याची प्रक्रिया आणि घन कार्बनच्या पृष्ठभागासह त्याचे रासायनिक परस्परसंवादाची प्रक्रिया. ही दोन्ही प्रक्रिया एकमेकांशी संबंधित आहेत, परंतु प्रत्येकाची स्वतःची कायदे आहेत. या प्रक्रियेतील सर्वात महत्वाची प्रक्रिया ऑक्सिजन खपण्याची प्रक्रिया आहे, ज्याचे विविध रासायनिक अभिक्रियांद्वारे वर्णन केले जाते.
कार्बनसह ऑक्सिजन संयोजित करण्याच्या जटिल प्रक्रियेची यंत्रणा सी. सी 0 0 वाईच्या इंटरमीडिएट भौतिकदृष्ट्या कॉम्प्लेक्समधून सीओ आणि सी 2 2 च्या दोन ऑक्साईड्सच्या एकाचवेळी तयार केली जाते जी नंतर सीओ आणि विभागात विभागली जाते. या ऑक्साइडमधील गुणोत्तर जळण्याची स्थिती अवलंबून असते. तदनुसार, बर्ण केलेल्या कार्बनच्या प्रतिक्रियेचे समीकरण खालीलप्रमाणे लिहीले जाऊ शकते:
धडा 2. दहन दरम्यान रासायनिक प्रक्रिया
मग बर्निंग कार्बन मोनोऑक्साइड उत्पन्नाची एक समृद्ध प्रतिक्रिया:
ज्या पद्धतीची विभागणी 2.3 मध्ये चर्चा केली आहे.
ही प्रतिक्रिया कार्बनच्या पृष्ठभागाजवळ येऊ शकते, म्हणूनआणि कोळसा द्रव आत, त्याच्या pores आणि cracks मध्ये.
आणखी एक प्रतिक्रिया म्हणजे उष्ण कार्बन आणि कार्बन डाय ऑक्साईडमध्ये एक वेगळी प्रतिक्रिया.
![]()
ऑक्सिजनची कमतरता असलेल्या ठिकाणी ते वेगाने वेगाने वाहते परंतु कार्बनचे तापमान पुरेसे असते.
वर्णित प्रतिक्रियांचे मिश्रण कार्बन दहन च्या उत्पादनांची रचना ठरवते.
कॉम्बोशन प्रक्रियेचे उद्भव
| आर |
ज्वलनशील मिश्रणातील सिंचन त्यांच्या स्वत: च्या प्रज्वलन, बाह्य स्त्रोताद्वारे किंवा स्वयंस्फूर्त दहनमुळे उद्भवू शकते. स्वयं-इग्निशन आणि इग्निशनची प्रक्रिया गॅसिस, द्रव किंवा घन अवस्थेत असलेल्या पदार्थांची वैशिष्ट्ये असल्यास, स्वयंचलित स्फोटक द्रव पदार्थ (विशेषत: बारीक विभाजित अवस्थेत असलेल्या) किंवा विकसित पृष्ठभागावर असलेल्या सामग्रीवर वितरीत केलेल्या उकळत्या द्रवांचे वैशिष्ट्य आहे.
3.1. आत्म-इग्निशन स्थिर सिद्धांत
अग्नि एक अनियंत्रित बर्न आहे जी वेळ आणि स्थानामध्ये विकसित होते, लोकांना धोकादायक आणि सामग्रीचे नुकसान होऊ शकते.
मनुष्यांसाठी अग्निशामक धोके खुली आग, चमक, ताप, ज्वलनशील पदार्थ, धुम्रपान, कमी ऑक्सिजन, इमारतींचे संकुचित होणे किंवा स्थापना यासारखे आहेत.
दमटपणा वेगाने कार्यरत आहे, भौतिक-रासायनिक प्रतिक्रिया, उष्णता आणि धुम्रपान, ज्वाला किंवा स्मोल्डिंगच्या प्रकाशासह. सामान्य परिस्थितीत, दहन हे ऑक्सिडायझिंग किंवा वायुमंडलीय ऑक्सिजनसह दहनशील पदार्थ एकत्र करण्याची प्रक्रिया आहे. तथापि, काही पदार्थ (उदाहरणार्थ, संकुचित ऍसिटिलीन, नायट्रोजन क्लोराईड, ओझोन) ऑक्सिजन शिवाय उष्णता आणि ज्वाला तयार करण्यासाठी विस्फोट करू शकतात. परिणामी, दहन केवळ संयुगाचीच नव्हे तर विघटित होण्याच्या प्रतिक्रियांच्या परिणामामुळे होऊ शकते. हे देखील ज्ञात आहे की हायड्रोजन आणि अनेक धातू क्लोरीनच्या वातावरणात, सल्फर वाष्प मध्ये तांबे, कार्बन डाय ऑक्साईडमधील मॅग्नेशियम इ. मध्ये बर्न करू शकतात.
हवेत ऑक्सिजन असलेल्या दहनशील पदार्थांच्या ऑक्सिडेशन दरम्यान उद्भवणारी सर्वात धोकादायक दहन. त्याच वेळी, इंधन प्रणालीला आवश्यक प्रमाणात ऊर्जा पुरवण्यास इग्निशन स्रोत असणे आवश्यक आहे. इग्निशनचे सर्वात सामान्य स्त्रोत असे आहेत: विद्युत् उपकरणांचे नुकसान, धातूचे धातू, वेल्डिंग, फोर्जिंग काम करते तेव्हा दिसणारे स्पार्क; घर्षण द्वारे उत्पन्न गर्मी; तांत्रिक ताप यंत्रे; अग्निशामक उपकरणे; अॅडियॅबेटिक कॉम्प्रेशनची उष्णता; स्थिर वीजेचा स्पार्क डिस्चार्ज; विद्युतीय संपर्कांची उष्णता उष्णतेच्या प्रकाशासह कार्यरत रासायनिक अभिक्रिया.
या स्त्रोतांचा उष्णता तापमान भिन्न आहे. तर, धातूच्या शरीरावर पडलेल्या चमकांचा तापमान 1 9 00 डिग्री सेल्सिअस पर्यंत असू शकतो, तर सामन्याची ज्वाळा जवळपास आहे. 800 डिग्री सेल्सिअस, स्लिपेज दरम्यान बेल्ट कन्व्हेयरचा अग्रगण्य ड्रम 600 अंश सेल्सिअस पर्यंत आहे आणि विद्युत् डिस्चार्जच्या उष्णतेमध्ये तापमान तात्काळ रासायनिक प्रतिक्रियांसह 10,000 डिग्री सेल्सियसपर्यंत पोहोचते.
बर्निंग पूर्ण आणि अपूर्ण असू शकते. संपूर्ण दहन, ऑक्सिजन जास्त प्रमाणात होत असल्याने, प्रतिक्रिया उत्पादने कार्बन डायऑक्साइड, पाणी, नायट्रोजन, सल्फर डाय ऑक्साईड असतात. ऑक्सिजनच्या कमतरतेमुळे अपूर्ण दहन उद्भवते, या प्रकरणात दहन करणारे पदार्थ विषाणू आणि दहनशील पदार्थ असतात - कार्बन मोनोऑक्साइड, अल्कोहोल, केटोन्स, अॅल्डेहायड्स इत्यादी. दहनशील पदार्थाच्या संपूर्ण दहनसाठी विशिष्ट प्रमाणात हवा आवश्यक असते: लाकूड 1 किलो - 4.18, पीट - 5 , 8, प्रोपेन - 23.8 एम 3.
खालीलप्रमाणे दहन प्रक्रिया कल्पना केली जाऊ शकते. उष्णता प्रक्षेपित होण्याच्या प्रक्रियेसह एक थंड दहनशील माध्यम गरम होते, त्यात ऑक्सिजनसह दहनशील माध्यमांचे गहन ऑक्सिडेशन असते आणि अतिरिक्त उष्णता सोडते. यामुळे, दहनशील द्रवपदार्थाच्या समीप लेयरचे तापमान वाढते, ज्यामध्ये तीव्र रासायनिक प्रतिक्रिया देखील होते. ज्वलनशील पदार्थांच्या अशा स्तर-बाय-लेयर दहनमुळे, दहन क्षेत्र हलते; या चळवळीची गती दहन प्रक्रियेची तीव्रता निर्धारित करते आणि ही सर्वात महत्वाची वैशिष्ट्ये आहे. संपूर्ण ज्वलनशील पदार्थ संपुष्टात येईपर्यंत लेयर बाय बाय लेदर हीटिंग, ऑक्सीकरण आणि दहन चालू राहील.
पदार्थाचा उष्णता आणि रासायनिक प्रतिक्रिया झाल्यास अरुंद क्षेत्राला ज्वाळा समोर म्हणतात.
दहनशील प्रणाली रासायनिक रूपाने एकसमान आणि विषम असू शकतात. रासायनिकदृष्ट्या एकसमान प्रणाली म्हणजे दहनशील वायू, वाष्प किंवा हवेसह धूळ यांचे मिश्रण, ज्यामध्ये दहनशील पदार्थ आणि हवा समान मिश्रित असतात. अशा प्रणाल्यांना बर्न करणे एकसारखे म्हणतात. रासायनिक रूपाने इनोमोजिनियस सिस्टीममध्ये, दहनशील पदार्थ आणि हवा मिसळलेले नाहीत आणि इंटरफेस आहेत. हे बर्याचदा घन दळण्यायोग्य पदार्थ असतात आणि त्यांच्या दहनांना विषमता म्हणतात.
दहनशील मिश्रण टीजीचे दहन करण्याची संपूर्ण वेळ दहनशील पदार्थ आणि ऑक्सिजन τ क दरम्यानच्या संपर्कासाठी लागणार्या वेळेची बेरीज आहे आणि ज्या वेळेस रासायनिक स्वतःचे होते, ऑक्सीकरण प्रतिक्रिया τ x
या दोन पदांच्या प्रमाणानुसार, प्रसार आणि किनेटिक दहन वेगळे केले जातात. घन दहनशील पदार्थ जळताना, पदार्थाच्या पृष्ठभागावर ऑक्सिजनला (विरघळणे) प्रवेश करणे आवश्यक असते. रासायनिक प्रतिक्रिया प्रक्रियेपेक्षा बरेच जास्त वेळ असते; म्हणूनच बर्निंग रेट ज्वलनशील पदार्थास ऑक्सिजनच्या प्रसाराने दराने पूर्णपणे ठरवले जाते. अशा पदार्थांचा जळजळ बर्याचदा अग्नीवर आढळतो आणि त्याला भ्रामक म्हणतात. दहन, ज्याचे प्रमाण रासायनिक प्रतिक्रिया दराने निश्चित केले जाते त्याला कोनेटिक म्हणतात. हा प्रकार दहन एकसमान दहनशील प्रणालींचे वैशिष्ट्य आहे.
बर्निंग कॅलोरिमेट्रिक, सैद्धांतिक आणि वास्तविक तापमान वेगळे करा.
दहनयुक्त कॅलरीमीट्रिक तापमान तपमानास संदर्भित करते ज्यांचे संपूर्ण दहन तपमान गरम होते, सर्व उष्णता सोडल्यास ते गरम करण्यासाठी खर्च केला जातो, हवेची मात्रा सैद्धांतिकदृष्ट्या आवश्यक असते, पदार्थ पूर्णपणे जळून जातात आणि प्रारंभिक तापमान 0 डिग्री सेल्सियस असते. उष्णता नुकसान शून्य असल्याचे मानले जाते. जर इंधन आणि हवा यांचे प्रारंभिक तापमान 0 अंश सेल्सिअस असेल, तर दहनयुक्त कॅलरीमीट्रिक तपमान
![]()
जिथे दहनशील पदार्थ, केकिल / किलो यांचे शुद्ध कॅलोरिफ मूल्य आहे. व्ही हा दहन उत्पादनांचा आकार आहे, एम 3 / किलो; क) दहन उत्पादनांची सरासरी व्होल्मेट्रिक ताप क्षमता, केकेसी / एम 3 डिग्री आहे.
परिणामी, कॅलोरिमेट्रिक बर्निंग तापमान केवळ दहनशील पदार्थांच्या गुणधर्मांवर अवलंबून असते आणि त्याचे प्रमाण अवलंबून नसते. सैद्धांतिक दहन तपमान दहन प्रक्रियेत उष्णता नष्ट होणे लक्षात घेते. कॅलोरिमेट्रिक बर्न्सिंग तापमान दहनशील पदार्थासाठी सर्वाधिक असते आणि गुणात्मक मूल्यांकनासाठी वापरले जाते. प्रत्यक्षात, जळताना, विकिरण, अतिरिक्त हवेचा उष्णता आणि वातावरण यामुळे ताप कमी होतो.
वास्तविक ज्वलनशील तापमान आग तापमान आहे. अंतर्गत आणि बाह्य आग तापमान वेगळे. बाह्य अग्नीचे तापमान ज्योतिषाचे तापमान असते आणि आंतरिक तापमान खोलीतील धूर तपमानाचे असते. वातावरणातील उष्णता कमी झाल्यामुळे, दहन उत्पादनांची आणि संरचनांची उष्णता यामुळे आग लागल्यास वास्तविक तापमान वाढते
नेहमी 30 पेक्षा 50% सैद्धांतिक पेक्षा कमी. उदाहरणार्थ, गॅसोलीनचा सैद्धांतिक जळण्याची तापमान 1730 डिग्री सेल्सिअस आहे आणि वास्तविक तापमान 1400 डिग्री सेल्सियस आहे.
ऑक्सिडायझिंग एजंटसह दहनशील वाष्प आणि वायू यांचे मिश्रण केवळ त्यातल्या इंधनाच्या विशिष्ट सामग्रीसह बर्न करू शकते.
दहनशील गॅसचे सर्वात कमी एकाग्रता ज्यात दहन शक्य आहे तेच इग्निशन (एलईएल) चे कमी सांद्रता मर्यादा म्हटले जाते. दहन सर्वात जास्त एकाग्रतेवर आहे ज्याला उच्च इग्रेशन मर्यादा इग्निशन (एआयपीडब्ल्यू) म्हटले जाते. या सीमांच्या आत असलेल्या एकाग्रतेचा प्रदेश म्हणजे इग्निशनचा प्रदेश. इग्निशन म्हणजे अग्नीच्या स्वरुपाचा अग्नि (जळण्याची सुरूवात). हे एक सतत दीर्घ बर्ण आहे, जे इग्निशन स्त्रोत काढल्यानंतरही थांबत नाही. इग्निशनच्या खालच्या आणि वरच्या मर्यादेचे मूल्य वायू मिश्रणाचे वायू, वाष्प आणि धूळ यांच्या गुणधर्मांवर अवलंबून असते, दहनक्षम मिश्रणात निष्क्रिय घटकांची सामग्री. ज्वलनशील मिश्रणाने इनरेट गॅसच्या जोडणीने इग्निशनच्या क्षेत्राचा संक्षेप केला आणि अखेरीस ते नॉन-दहनशील बनवते. इग्निशनची मर्यादा महत्त्वपूर्ण असते, दहन प्रतिक्रिया कमी करते की काही अशुद्धता. यापैकी सर्वात सक्रिय हलोजनयुक्त हायड्रोकार्बन्स आहेत. बर्ण थांबविण्यासाठी दोन्ही चिन्हांकित गुणधर्मांचा वापर केला जातो. वातावरणाचा दाब खालील मिश्रणाचा दबाव कमी करणे इग्निशनच्या क्षेत्रास देखील कमी करते आणि विशिष्ट दाबाने मिश्रण गैर-दहनशील बनते. दहनशील मिश्रणांच्या दाब वाढणे इग्निशनचे क्षेत्र विस्तृत करते, परंतु, नियम म्हणून किंचित. दहनशील मिश्रण तापमान वाढवणे इग्निशनचे क्षेत्र विस्तृत करते. प्रज्वलन स्त्रोताच्या शक्तीमुळे इग्निशनचे प्रमाण देखील प्रभावित होते.
केवळ एकाग्रता नसून इग्निशनची तापमान मर्यादा देखील असते.
वायुमध्ये वाष्पांच्या प्रजोत्पादनासाठी तापमान मर्यादा ही दहनशील पदार्थाची तपमान असते ज्यामध्ये त्याचे संतृप्त वाष्प इग्निशनच्या निम्न किंवा उच्च एकाग्रता मर्यादेशी संबंधित सांद्रता तयार करतात. इग्निशन तापमान हे सर्वात कमी तपमान असते ज्यामध्ये पदार्थ जळते किंवा स्मोल्डर सुरू होते आणि इग्निशनचे स्त्रोत काढून टाकल्यानंतर बर्न किंवा स्मोल्डर चालू ठेवते. इग्निशन तापमान स्वयं-दहन करण्यासाठी पदार्थाची क्षमता दर्शविते. जर एखाद्या पदार्थाचे प्रज्वलन तपमान अनुपस्थित असेल तर ते मंद-बर्निंग किंवा नॉन-दहनशील असे म्हटले जाते.
तपमानाच्या कृती अंतर्गत ऑक्सिडेशनची प्रवेग त्वरेने स्वत: ची प्रज्वलन करते. इग्निशन प्रक्रियेव्यतिरिक्त, ज्यामध्ये केवळ खंडांचा मर्यादित भाग असतो - पृष्ठभागाच्या संपूर्ण खंडात पृष्ठभाग - इग्नाइज, स्व-इग्निशन होतो. स्वयं-प्रज्वलन तपमान सर्वात कमी तापमान मानले जाते, ज्याला पदार्थ गरम करणे आवश्यक आहे, जेणेकरुन पुढील स्वयं-ऑक्सीकरण परिणामी ते दाबले जाईल. ऑक्सिडेशन प्रक्रियेदरम्यान उष्णताची मात्रा वातावरणास उष्णता सोडविण्यापेक्षा ओलांडल्यासच स्वयं-इग्निशन शक्य आहे.
स्वयं-इग्निशन तापमान पदार्थासाठी स्थिर नसते कारण ते मोठ्या प्रमाणावर त्याच्या दृढतेच्या अटींवर अवलंबून असते. तुलनात्मक डेटा प्राप्त करण्यासाठी, चाचणी यंत्रे आणि वायू आणि वाष्पांच्या स्वयं-प्रज्वलन तपमानाचे निर्धारण करण्याच्या पद्धतीचे प्रमाणीकरण केले जाते (GOST 13 920-68). प्रमाणित पद्धतीने ठरविलेले सर्वात कमी तापमान, ज्यामध्ये वायू आणि वाष्पांचा हवा वायूचा मिश्रण समानपणे गरम करणे आवश्यक आहे जेणेकरून त्यामध्ये बाह्य इग्निशन स्त्रोत न आणता अग्निशामक बनवावे, त्याला मानक स्वयं-इग्निशन तपमान म्हणतात.
एक प्रकारचा सहजगत्या प्रज्वलन म्हणजे स्वयंस्फूर्त दहन आहे, म्हणजे इग्निशन स्त्रोताच्या प्रभावाशिवाय स्वत: ची गरम होणारी दहन. आपोआप इग्निशन आणि आपोआप दहन यांच्यातील फरक तपमानाचे प्रमाण आहे. आपोआप दहन घनतेच्या वातावरणात होते आणि स्वयं-इग्निशनसाठी बाह्य पदार्थ बाहेरून तापविणे गरजेचे असते.

 गरम आणि थंड पाण्याची पुरवठा करणाऱ्या काउंटरच्या संकेतांचे स्वागत
गरम आणि थंड पाण्याची पुरवठा करणाऱ्या काउंटरच्या संकेतांचे स्वागत विविध आकार आणि फिटिंगच्या हवेच्या नलिका क्षेत्राची गणना
विविध आकार आणि फिटिंगच्या हवेच्या नलिका क्षेत्राची गणना दहन प्रक्रियांची रसायनशास्त्र. स्फोट शक्ती
दहन प्रक्रियांची रसायनशास्त्र. स्फोट शक्ती आपण मीटर रीडिंग्स प्रसारित न केल्यास काय होईल
आपण मीटर रीडिंग्स प्रसारित न केल्यास काय होईल